Clear Sky Science · nl
Twee codes van RNA-bewerking door deaminatie bij menselijke ziekten
Hoe cellen hun eigen boodschappen herschrijven
Elke cel in je lichaam leest voortdurend instructies uit DNA om je op te bouwen en te onderhouden. Decennialang gingen we ervan uit dat die instructies naar RNA werden gekopieerd en vervolgens trouw in eiwitten werden vertaald. Dit overzichtsartikel laat zien dat het verhaal veel minder rigide is: cellen "herschrijven" veel RNA-boodschappen nadat ze zijn gemaakt, waarbij ze enkele chemische letters verwisselen op manieren die subtiel of ingrijpend kunnen veranderen hoe ons lichaam functioneert. Begrip van deze verborgen laag van bewerking helpt verklaren waarom mensen auto-immuunziekten, neurologische aandoeningen, stofwisselingsproblemen, infecties en kanker ontwikkelen — en hoe we die mogelijk uiteindelijk kunnen behandelen.
Twee manieren om een enkele letter te veranderen
De auteurs richten zich op twee hoofdtypen RNA-bewerking die bij mensen voorkomen. De ene wordt A-naar-I-bewerking genoemd, uitgevoerd door enzymen die bekendstaan als ADARs. Zij veranderen de base adenosine (A) in inosine (I), die cellulair machinerie meestal leest alsof het guanosine (G) is. De andere is C-naar-U-bewerking, behandeld door enzymen uit de APOBEC-familie, die cytidine (C) in uridine (U) omzetten. Beide processen verwijderen een kleine chemische groep van een enkele base, maar ze verschillen in waar ze actief zijn, welke RNA's ze prefereren en hoe sterk ze de RNA-structuur hervormen. A-naar-I-bewerking verandert vaak hoe RNA-strengen zich vormen en kan eiwitten diversifiëren of veranderen hoe andere moleculen aan RNA binden. C-naar-U-bewerking is structureel vaak subtieler, maar kan toch stopcodes invoegen, eiwitsequenties aanpassen of regulerende gebieden van RNA fijnregelen.
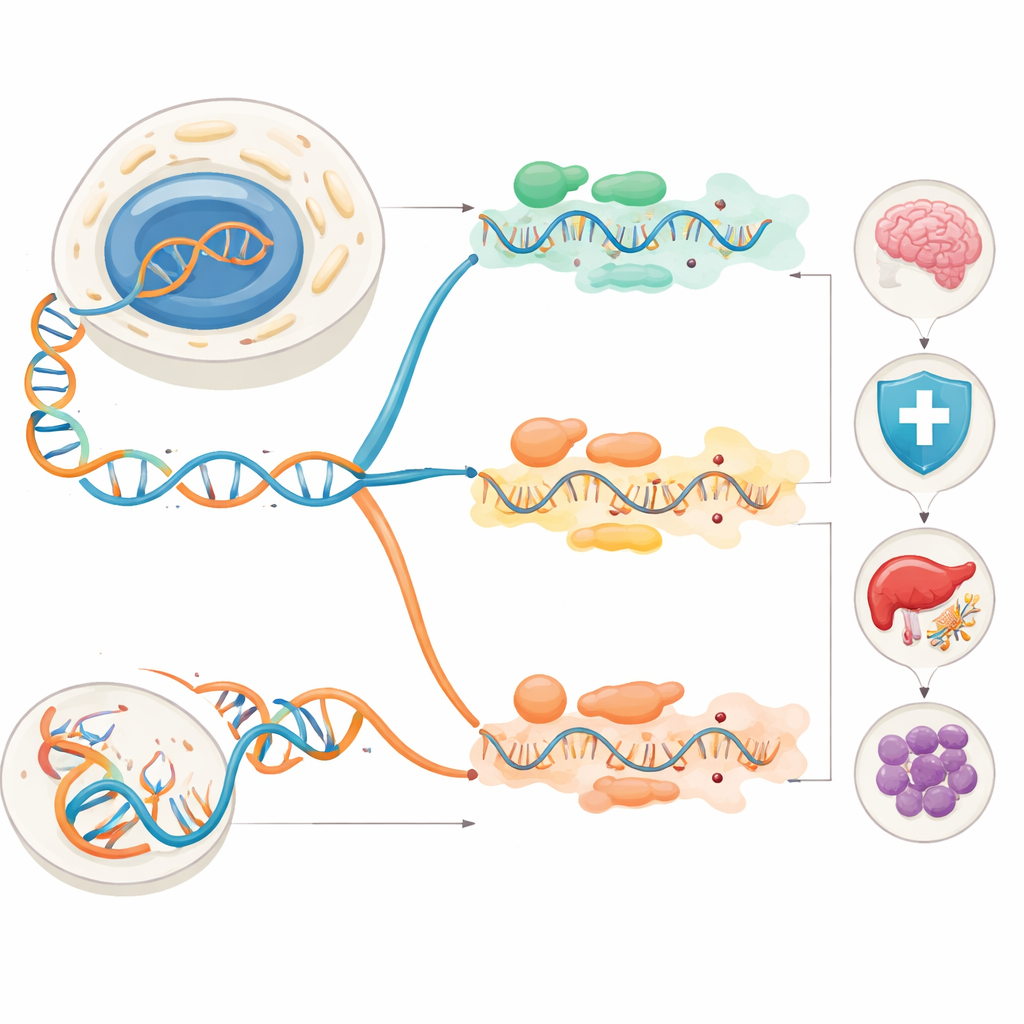
Van bewerkte boodschappen naar gezondheid en ziekte
Omdat deze bewerkingsevenementen eiwitdelen of de regulerende regio's eromheen kunnen veranderen, raken ze veel aspecten van de normale biologie. In het immuunsysteem bewerkt ADAR1 zelfgemaakte dubbelstrengs RNA zodat virussensoren ze niet voor vreemd afval aanhouden. Als ADAR1 faalt, blijven immuunsignalen vast "aan" staan, wat leidt tot chronische interferonresponsen en auto-immuunziekten zoals het Aicardi–Goutières-syndroom. APOBEC-enzymen bewerken ook RNA in immuuncellen, en vormen hoe macrofagen reageren op stress en ontsteking en dragen mogelijk bij aan aandoeningen zoals systemische lupus. In het zenuwstelsel is ADAR2-bewerking cruciaal voor het afstemmen van hersenreceptoren die de calciumstroom regelen; zonder die bewerking krijgen muizen toevallen en overlijden ze vroeg. APOBEC-gedreven bewerking van bepaalde receptor-RNA's in neuronen kan hun gevoeligheid vergroten en wordt gekoppeld aan epilepsie, degeneratie en cognitieve problemen.
Virussen, metabolisme en de link met kanker
RNA-bewerking beïnvloedt ook hoe we met virussen omgaan, energie beheren en kanker ontwikkelen. ADAR1 kan virale genomen direct bewerken, soms het virus verzwakkend en soms, zoals bij het hepatitis-delta-virus, juist helpend voor de voltooiing van de levenscyclus. APOBEC-enzymen, bekend om het aanvallen van retrovirussen, laten een sterk C-naar-U-handtekening achter in het RNA van SARS-CoV-2, waarmee ze het virus beperken maar tegelijk mutaties genereren die virale evolutie kunnen bevorderen. In het metabolisme helpt ADAR2 pancreatische bètacellen hun insulinesecretie aan te passen aan dieet, terwijl de activiteit van ADAR1 en ADAR2 het risico op diabetes en leververvetting beïnvloedt. De klassieke rol van APOBEC1 is het bewerken van het RNA voor apolipoproteïne B, waardoor een verkorte eiwitvorm ontstaat die essentieel is voor het transport van voedingsvetten; ontbreekt deze bewerking, dan ontwikkelen muizen ernstige lipiden- en cholesterolproblemen.
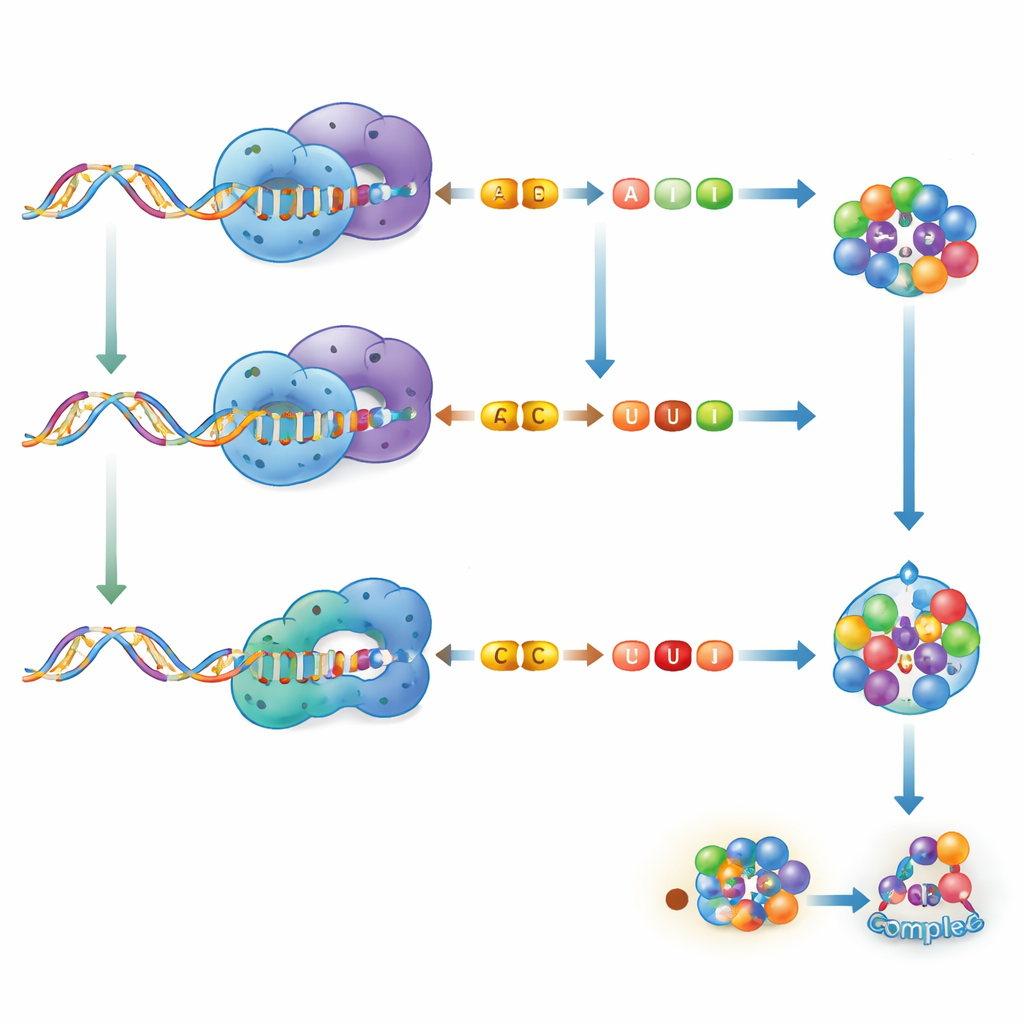
Hoe bewerkt RNA tumoren vormt
Dezelfde enzymen die ons beschermen, kunnen ook kanker aansturen wanneer ze verkeerd gereguleerd zijn. Grote kanker-sequencingprojecten hebben tienduizenden A-naar-I-bewerkingssites en wijdverspreide APOBEC-gerelateerde mutaties blootgelegd. Bij borstkanker kan ADAR1-bewerking het tumorgedrag aanzetten of afremmen, afhankelijk van het doel-RNA, en invloed hebben op celinvasie, metastase en overleving. Bij glioblastoom, een dodelijke hersentumor, ondersteunt ADAR1 kankerstamcellen, terwijl ADAR2 over het algemeen als rem fungeert door zowel eiwitcoderende RNA's als kankerbevorderende microRNA's te bewerken. Bij leukemieën bevordert ADAR1 vaak maligne, stamcelachtige cellen en dempt tumor-suppressieve microRNA's, terwijl ADAR2 specifieke doelen bewerkt op manieren die de ziekte vertragen. APOBEC-gemedieerde C-naar-U-bewerking van bepaalde RNA's in bloedkankers kan ofwel de uitkomst van patiënten verslechteren of verbeteren, wat onderstreept hoe contextafhankelijk deze veranderingen zijn.
Onbeantwoorde vragen en toekomstige mogelijkheden
Ondanks een explosie aan gecatalogiseerde bewerkingssites worstelen wetenschappers nog steeds om betekenisvolle edits van achtergrondruis te scheiden. Veel gedetecteerde veranderingen hebben mogelijk weinig effect, maar een minderheid heeft duidelijk levens-of-doodsconsequenties voor cellen en organismen. De auteurs betogen dat toekomstig werk moet vaststellen welke enzymen en hulpproteïnen individuele sites controleren, en vervolgens testen wat er gebeurt wanneer die enkele basen gedwongen altijd of nooit te worden bewerkt. Dergelijke studies zullen verduidelijken hoe RNA-bewerking bijdraagt aan specifieke ziekten en laten zien of het aanpassen van bewerkingspatronen een nieuwe klasse van precisietherapieën kan worden — om een overactief immuunsysteem te kalmeren, hersencircuits af te stemmen, stofwisselingsonevenwichtigheden te corrigeren of kankers gevoeliger te maken voor behandeling.
Waarom dit van belang is voor alledaagse gezondheid
In eenvoudige bewoordingen toont dit artikel aan dat onze cellen niet alleen de genetische code lezen; ze proeflezen en herzien die actief op het RNA-niveau, met twee parallelle "bewerkingscodes". Wanneer deze kleine aanpassingen op de juiste plaats en in de juiste hoeveelheid plaatsvinden, helpen ze ons immuunsysteem in balans te houden, onze hersenen stabiel, ons metabolisme flexibel en onze afweer tegen virussen scherp. Wanneer de bewerkingsmachines overactief, verkeerd geplaatst of kapot zijn, kunnen diezelfde veranderingen ons naar auto-immuniteit, infectie, dementie, stofwisselingsziekten of kanker duwen. Door deze eenletterige herschrijvingen in kaart te brengen en te begrijpen, hopen wetenschappers ziekten eerder te diagnosticeren, te voorspellen wie risico loopt, en uiteindelijk behandelingen te ontwerpen die het bewerkingsproces weer in gezonde richting sturen.
Bronvermelding: Min, D.J., Lee, S., Lee, Ys. et al. Two codes of RNA editing by deamination in human diseases. Exp Mol Med 58, 382–395 (2026). https://doi.org/10.1038/s12276-025-01633-8
Trefwoorden: RNA-bewerking, ADAR, APOBEC, auto-immuniteit, kanker