Clear Sky Science · nl
Interferon-regulerend factor 5 draagt bij aan de pathogenese van emfyseem via NLRP3 en Ly6C-expressing cellen
Waarom deze longstudie ertoe doet
Chronische obstructieve longziekte (COPD) en emfyseem beroven miljoenen mensen van hun adem, vaak nog lang nadat ze zijn gestopt met roken. Huidige geneesmiddelen kunnen de luchtwegen helpen openen, maar ze doen weinig om de smeulende ontsteking te kalmeren die de longen langzaam blijft aantasten. Deze studie onthult een moleculaire "ringleider" van die schade en suggereert een nieuwe manier om kwetsbare luchtzakjes te beschermen en de achteruitgang van de longfunctie te vertragen.
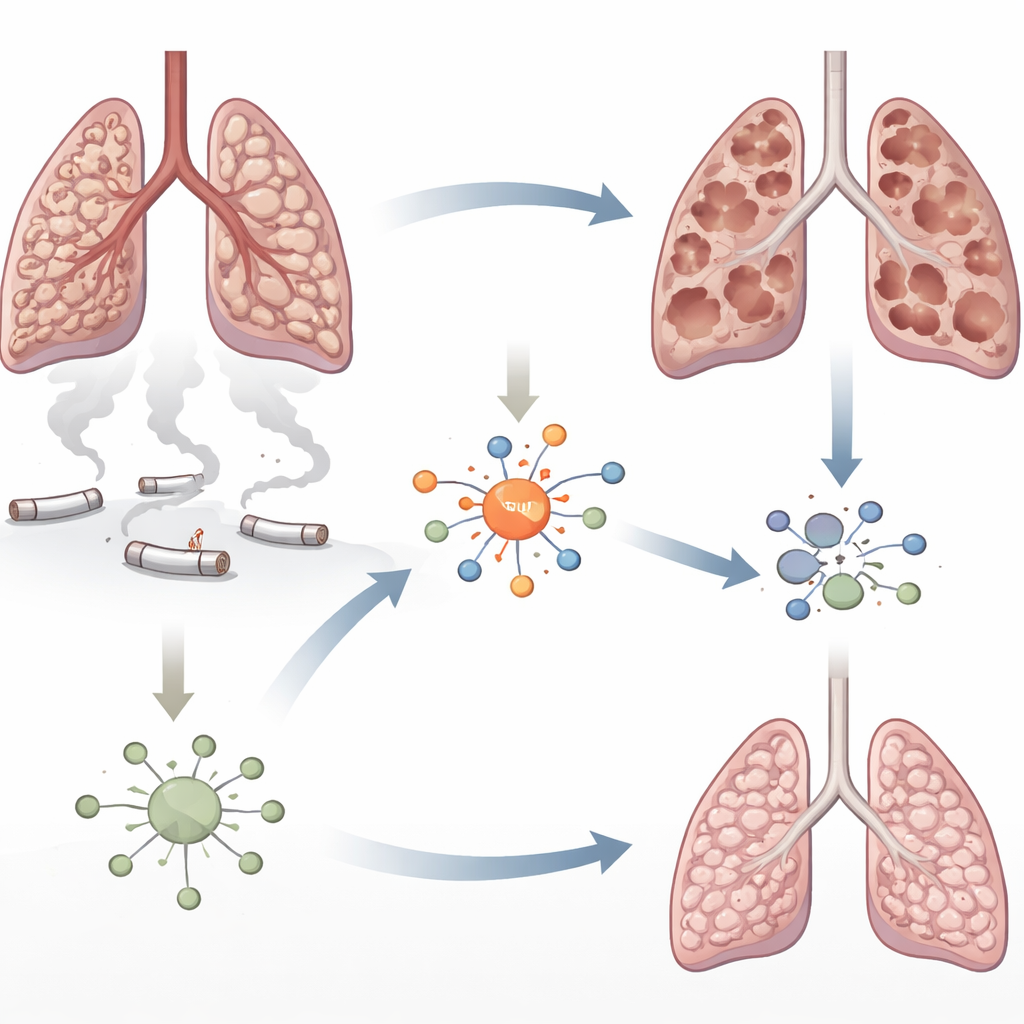
Een nadere blik op door rook beschadigde longen
Emfyseem wordt gekenmerkt door de geleidelijke afbraak van de kleine luchtzakjes waaruit de gasuitwisseling van zuurstof en kooldioxide plaatsvindt. Sigarettenrook legt de longen bloot aan toxische deeltjes die cellen beschadigen en golven van immuuncellen aantrekken. De auteurs richtten zich op een eiwit genaamd interferon-regulerend factor 5 (IRF5), dat bekendstaat als aanjager van ontsteking bij auto-immuunziekten maar weinig bestudeerd is bij COPD. Eerder onderzoek suggereerde dat IRF5-niveaus stijgen in aan rook blootgestelde longen. Hier wilden de onderzoekers nagaan of IRF5 slechts met de ontsteking meeloopt of daadwerkelijk bijdraagt aan de vernietiging van longweefsel.
Een belangrijke schakel uitschakelen bij muizen
Om de rol van IRF5 te onderzoeken, maakten de onderzoekers muizen die het gen voor dit eiwit volledig misten. Ze stelden vervolgens normale en IRF5‑deficiënte dieren gedurende enkele weken aan sigarettenrook bloot en vergeleken de staat van hun longen. Bij normale muizen veroorzaakte rook duidelijke tekenen van emfyseem: de wanden tussen aangrenzende luchtzakjes gingen verloren, met grote, overgeblazen ruimten als gevolg. Daarentegen bleken muizen zonder IRF5 grotendeels beschermd tegen deze structurele schade, ook al trok rook nog steeds immuuncellen naar de luchtwegen en steeg de concentratie van vele ontstekingsmoleculen. Dit wees op IRF5 als een cruciale schakel tussen rookblootstelling en de daadwerkelijke afbraak van de longarchitectuur.
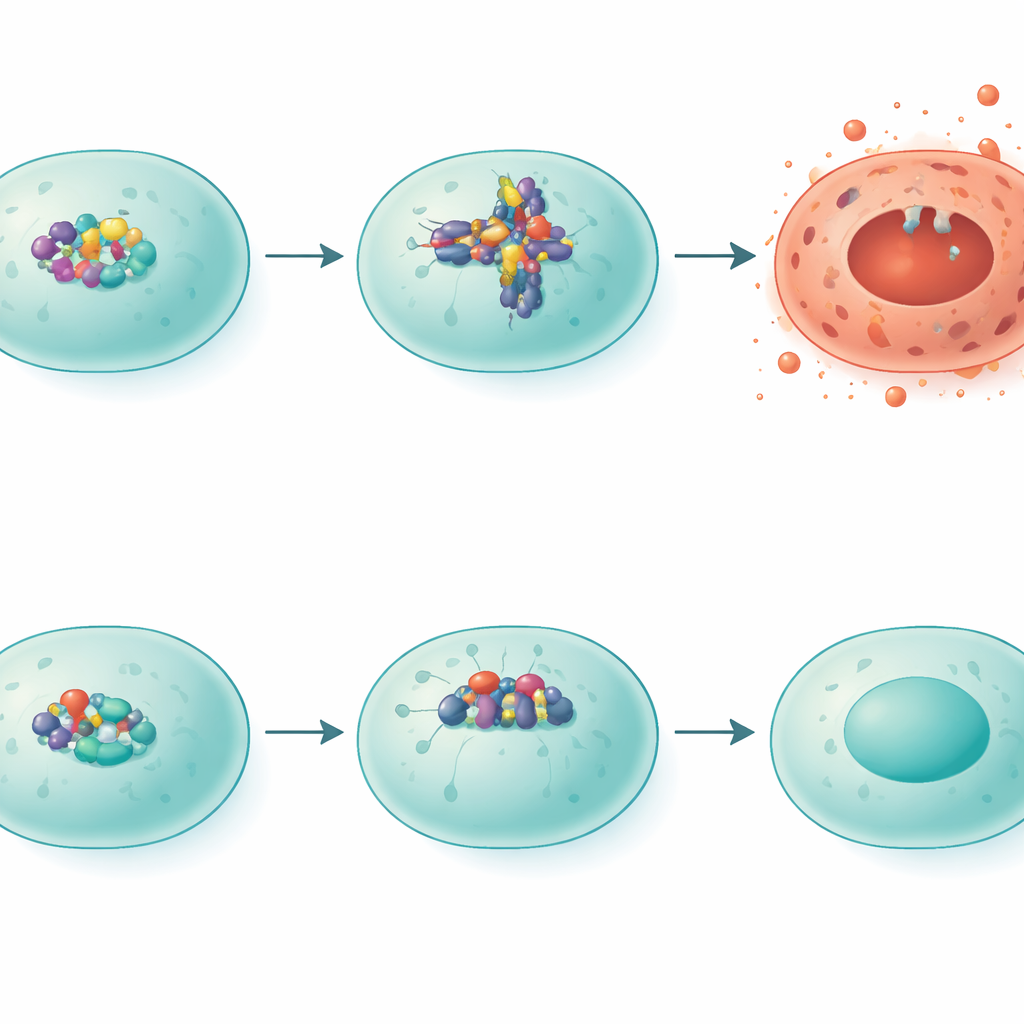
Hoe IRF5 cellen naar een brandende dood stuurt
De onderzoekers zoemden vervolgens in op een specifieke vorm van gewelddadige celdood, pyroptose, die gaten in celmembranen blaast en ontstekingsbevattende inhoud in het omliggende weefsel verspreidt. Een eiwitcomplex dat bekendstaat als NLRP3 vormt het hart van dit proces. Bij normaal aan rook blootgestelde muizen stegen de NLRP3-niveaus en vertoonden patronen van een ander eiwit, gasdermine D, een toestand die op pyroptose lijkt. Bij IRF5‑deficiënte muizen waren de NLRP3-niveaus veel lager en werd gasdermine D in alternatieve vormen geknipt die met minder destructieve uitkomsten geassocieerd zijn. Toen het team IRF5 kunstmatig verhoogde in longgerelateerde cellen in het laboratorium, stegen de NLRP3-niveaus, waarmee werd bevestigd dat IRF5 fungeert als een transcriptionele schakelaar die dit schadelijke pad aanzet.
Beschermende immuuncellen stappen het toneel op
IRF5 veranderde ook de samenstelling van immuuncellen in de long. Bij muizen zonder IRF5 nam een subset van in het bloed afkomstige cellen sterk gemarkeerd door het oppervlaktemolecuul Ly6C duidelijk toe. Deze Ly6C‑hoge cellen omvatten zowel monocyten als T-cellen en kwamen in grotere aantallen voor na rookblootstelling. Toen de wetenschappers Ly6C‑hoge cellen uit IRF5‑deficiënte muizen zuiverden en in gewone aan rook blootgestelde dieren transfuseerden, ontwikkelden de ontvangers minder afbraak van luchtzakjes en toonden ze verlaagde NLRP3-niveaus in de long. Aanvullende experimenten lieten zien dat IRF5 direct de activiteit van het Ly6C-gen dempt, wat suggereert dat wanneer IRF5 aanwezig is, van deze potentieel beschermende cellen minder wordt geproduceerd of in stand gehouden.
Menselijke longen bevestigen het signaal
Om te onderzoeken of deze bevindingen relevant kunnen zijn voor mensen, bekeken de auteurs longweefsel van patiënten die een operatie voor longkanker ondergingen. Ze vergeleken monsters van personen met een goede gasuitwisselingscapaciteit met die van personen met aanzienlijk emfyseem. IRF5-eiwitniveaus waren aanzienlijk hoger in longen uit de emfyseemgroep. Hoewel deze studie niet groot genoeg was om IRF5 precies te koppelen aan symptomen of exacerbaties, sloot het patroon aan bij de muisgegevens: meer IRF5 in zieke longen, minder in gezondere longen.
Wat dit kan betekenen voor toekomstige behandelingen
Samen genomen portretteert het werk IRF5 als een centrale coördinator van rookgedreven longschade. Het versterkt een celdoodmotor rondom NLRP3 en stuurt immuuncellen weg van Ly6C‑hoge populaties die lijken bij te dragen aan het behoud van de structuur van luchtzakjes. Voor patiënten is de implicatie rechttoe rechtaan: een geneesmiddel dat de activiteit van IRF5 dempt, zou theoretisch de meest destructieve vormen van ontsteking kunnen verminderen zonder het immuunsysteem volledig uit te schakelen. Hoewel dergelijke therapieën voor COPD nog niet bestaan, biedt deze studie een duidelijk moleculair doel en een biologisch plausibel pad naar behandelingen die meer doen dan alleen vernauwde luchtwegen openen—ze zouden het fragiele raamwerk van de long daadwerkelijk kunnen beschermen.
Bronvermelding: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
Trefwoorden: emfyseem, COPD, ontsteking, longimmuniteit, celdood