Clear Sky Science · ja
計算と実験のギャップを埋める:学習モデル比較に基づき大型言語モデルを活用してアルツハイマー治療薬を優先化する
なぜ家族や患者にとって重要なのか
アルツハイマー病は記憶や自立性、生活の質を奪いますが、本当に効果的な治療はまだ限られています。本研究は、既存の薬を新たな目的で再活用する手法を、強力な計算モデルと大型言語モデル(現在の日常的なチャットボットにも使われているタイプのAI)を組み合わせて用いることで、膨大な医療データや研究論文から効率的に選別する、より迅速な治療探索の道を模索します。目的は、多数の候補薬を現実的に臨床で検証可能な少数の候補に絞り込むことです。
既存薬を新たな用途に再利用する
全く新しい薬を一から開発するには10年以上、数十億ドルを要し、成功の保証はありません。代替策の一つが「薬剤リポジショニング」で、パーキンソン病やうつ病など別の適応で既に承認されている薬をアルツハイマー治療に応用できないか探ります。これらの薬は安全性プロファイルが既に確立されているため、アルツハイマー向け臨床試験への移行が比較的速く進む可能性があります。しかし、生物学的データベースや医学文献をスキャンする現代の計算手法は膨大な候補リストを生成し、研究者が手作業で評価するには多すぎるという新たなボトルネックを生んでいます。
複数の高度なモデルを結集する
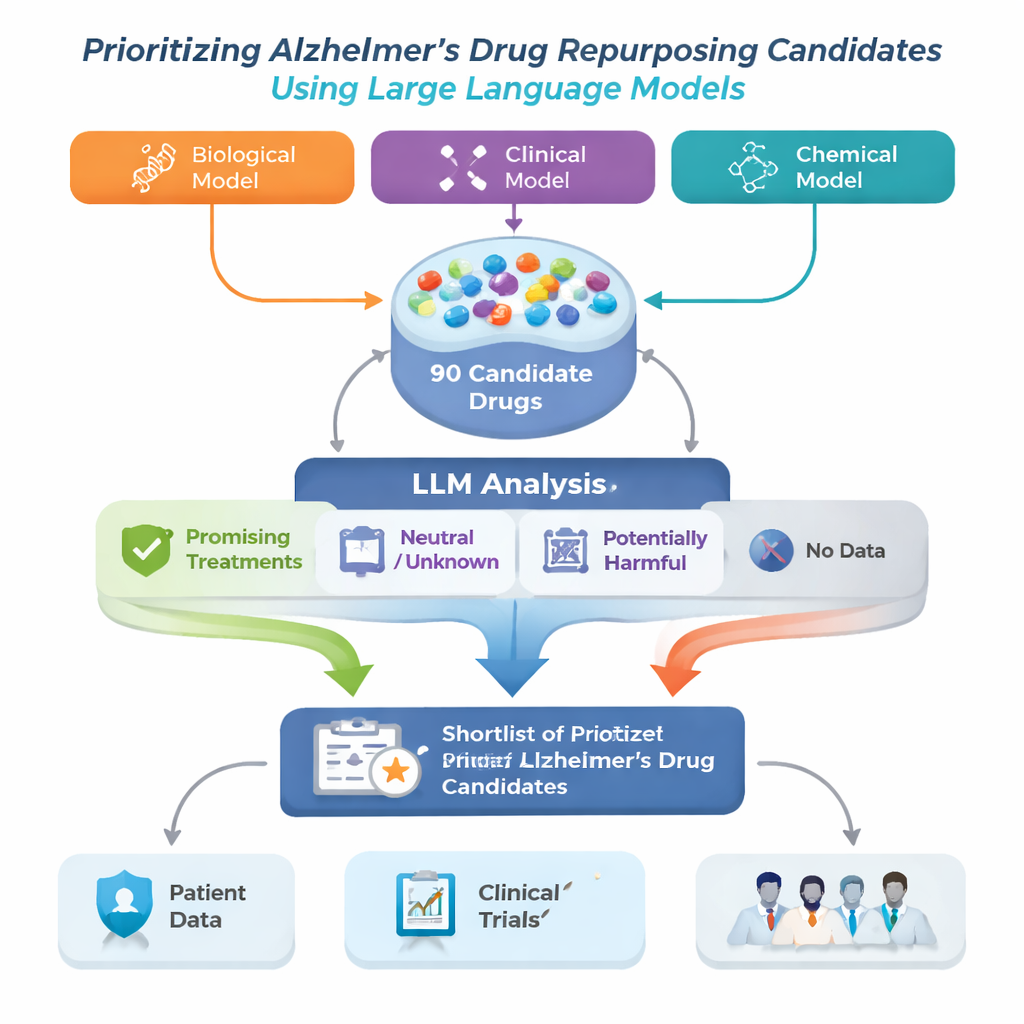
研究チームは、この問題に対処するために、アルツハイマー薬リポジショニングのフレームワークを構築しました。出発点として3種類の異なる高度な計算モデルを用います。各モデルは、疾病、薬、遺伝子などの医療概念を結び付ける大規模な生物医療「地図」であるナレッジグラフを解析し、アルツハイマーに有益でありそうな薬を提案します。各モデルはパターンの見え方が異なるため、提案リストは完全には重なりません。著者らは各モデルの上位30件ずつを合わせて90件の候補薬プールを作り、その後、大型言語モデル(LLM)を自動だが慎重なレビュアー役として用い、各薬に関する公表研究を読み、証拠が有益か中立か有害かを判定させました。
AIは医学文献をどのように読むか
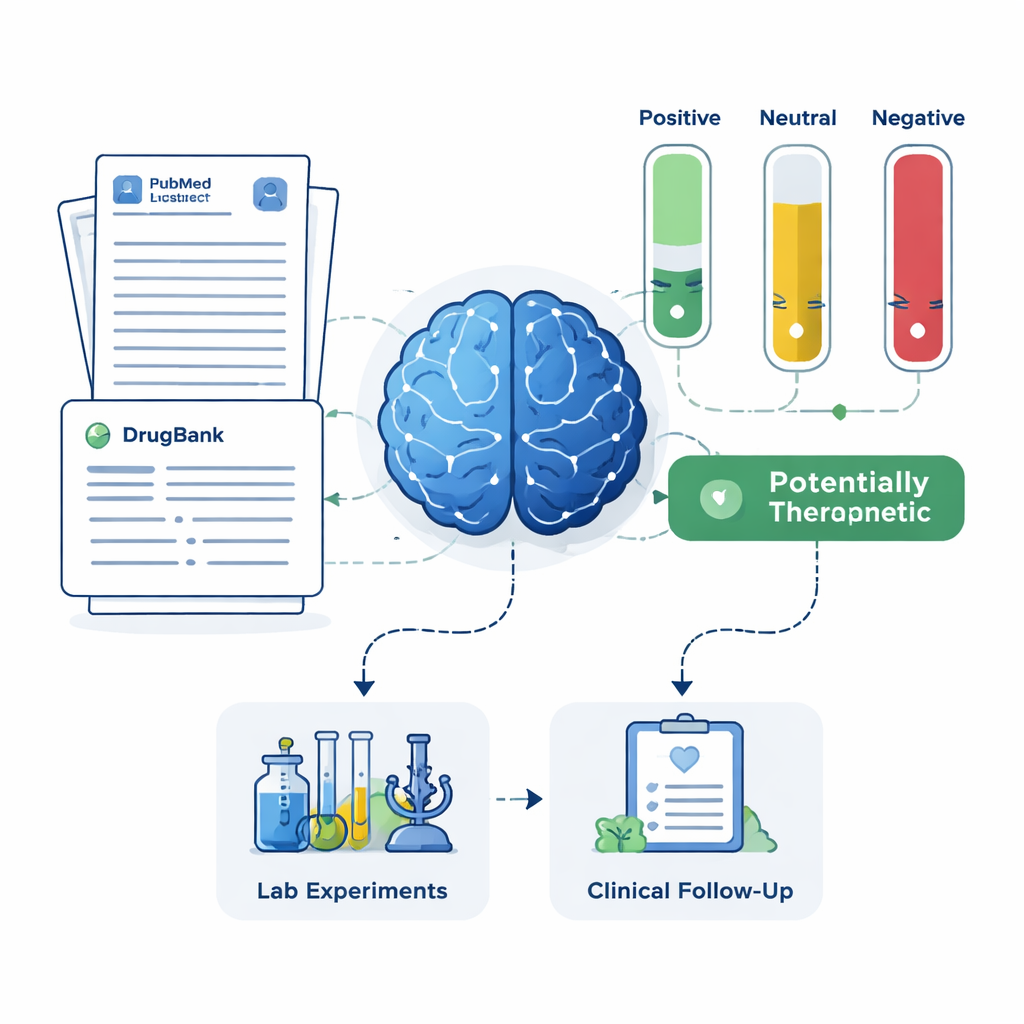
各候補薬について、システムはPubMedから最大200件の抄録と、医薬品データベースからの詳細な薬剤説明を取得しました。LLMには表示されたテキストのみに基づいて判断するよう指示し、各抄録をアルツハイマー治療に対して肯定的・中立的・否定的のいずれかにラベル付けさせました。これらのラベルは単純なスコアに変換され、肯定的・中立的・否定的の割合として表されます。明確な肯定的証拠を要求する厳しいルールと、わずかな利益の兆候でもフラグを立てる寛容なルールという2種類の規則を用いて、フレームワークは薬を4つのグループに分類しました:有望な治療候補、潜在的に有害、不明または中立、そしてアルツハイマー関連の論文がまったくない薬です。後者のグループは研究が少ないものの、特に新規の可能性を秘めているかもしれません。
実患者データと臨床試験との照合
AIの短縮リストが実世界で妥当かを確かめるため、チームは結果を二つの独立した情報源と比較しました:大規模なアルツハイマー患者登録データと登録された臨床試験の記録です。フレームワークは、患者データで強い保護的シグナルがあり豊富な試験歴を持つ既存のアルツハイマー薬メマンチンを高優先度候補として再発見しました。また、マグネシウム、ミノサイクリン、ピマバンセリン、テストステロン、ドキシサイクリンといった、支持する研究の程度は様々ながら専門医が有望と考えてきた薬も浮かび上がらせました。一方で、文献が有害性や有効性欠如を示唆する薬も特定され、それらは優先度を下げるか、副作用の調査対象とすることが推奨されました。
計算予測から実際の次の一手へ
日常語で言えば、このフレームワークは何千もの論文を読み、大規模医療データベースのパターンを照合し、人間の専門家にとってずっと短く整理されたアルツハイマー候補薬リストを提供する超高速で慎重な研究アシスタントのように機能します。本研究は、アイデアを生み出すグラフベースのモデルと、証拠を評価する言語モデルという異なるAIを組み合わせることで、十分に支持された薬剤も、検査に値する興味深い新しい選択肢もより速く見つけられることを示しています。このアプローチ自体がアルツハイマーを治すわけではありませんが、計算で得られた発見と実験室や臨床試験の地道な作業をつなぐ強力な新しい方法を提供し、より効果的な治療法への道を加速する可能性があります。
引用: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
キーワード: アルツハイマー病, 薬剤リポジショニング, 人工知能, 大型言語モデル, ナレッジグラフ