Clear Sky Science · ja
腫瘍微小環境における空間的に変化する関係性をモデル化するためのグラフに機能的エッジを符号化する手法
がんの“近隣”を写し取ることが重要な理由
がんは孤立して成長するわけではありません。腫瘍細胞は免疫細胞、支持細胞、血管、化学的シグナルなどが混在する賑やかな近隣環境の中に存在します。それらの配置や互いへの影響の強さが、がんが転移するか、治療に反応するか、あるいは制御されるかを左右します。本稿では、顕微鏡画像や腫瘍の分子マップをネットワークに変換し、どの細胞や経路の相互作用が疾患型や患者転帰と最も結びついているかを特定する手助けをする新しい人工知能フレームワーク、SPIFEEを紹介します。
組織をネットワーク地図に変換する
近年のがん研究は、顕微鏡での見た目以上の情報を計測できます。個々の細胞上の数十種類のタンパク質を可視化する手法、組織構造を詳細に示すカラー画像、あるいは腫瘍断片の何千ものスポットでどの遺伝子が活性化しているかを記録する新しいツールなどがあります。SPIFEEはこれらを同じ近隣の異なる視点とみなします。各サンプルをグラフとして表現し、ノードは細胞型、視覚的パターン、分子経路といった腫瘍微小環境の重要な要素を示し、エッジは空間におけるこれらの要素間の相互作用を捉えます。重要なのは、SPIFEEが相互作用を単一の数値(例えば「距離」)に還元しない点です。代わりに各エッジは、一定の距離範囲にわたって二つの要素がどの程度混ざり合うか、または反発するかを示す小さな曲線を格納し、より豊かな空間情報を保持します。
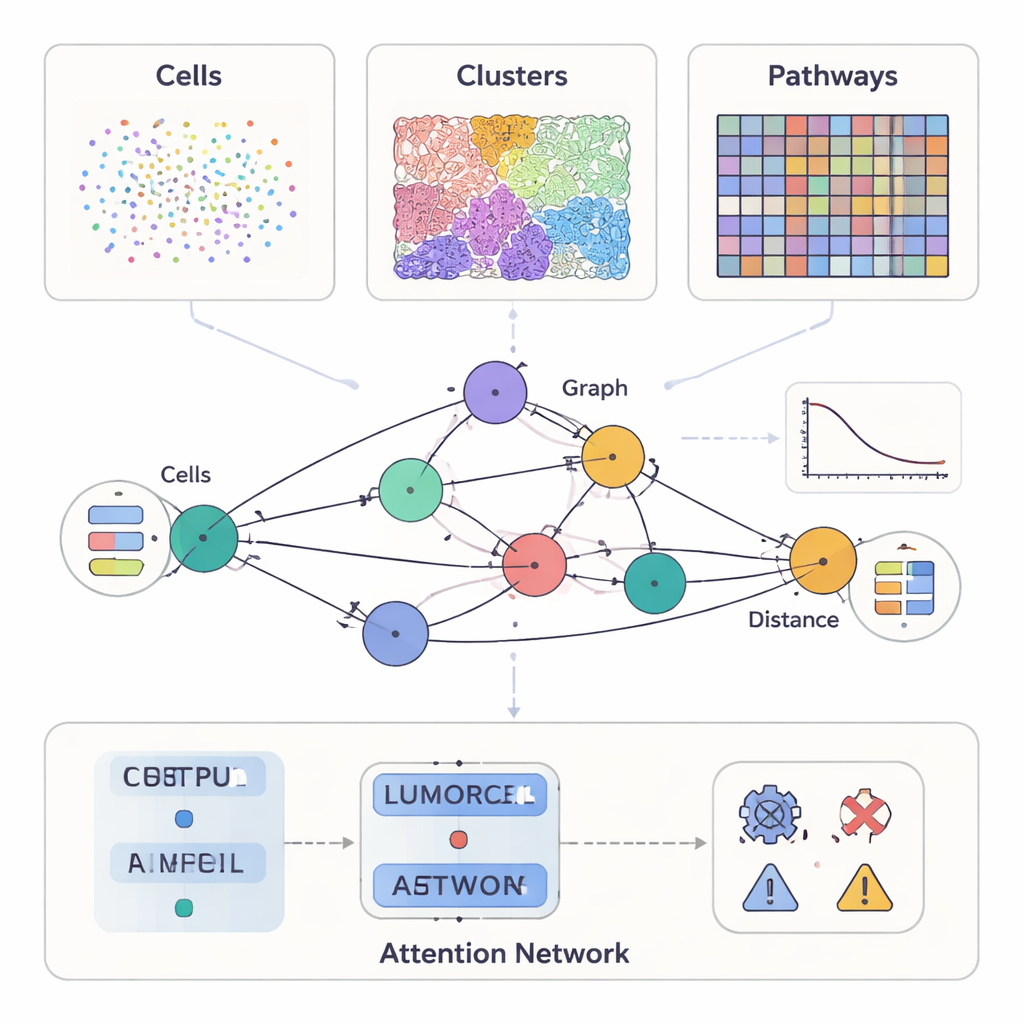
さまざまな種類のがんデータに対する柔軟なレンズ
著者らは、異なる技術・スケールにまたがる複数の大規模独立がんデータセットでSPIFEEを検証しました。多重免疫蛍光法で標識された膵臓疾患サンプルでは、グラフの各ノードが細胞型を表し、ノード特徴はそれらの細胞がどのようにコミュニケーションする傾向があるかを要約した単一細胞RNAシーケンシングから得られました。日常的なヘマトキシリン・エオシン染色の肺がんスライドでは、ノードは自己教師あり学習システムによって自動的に発見された反復的な視覚パターンを表しました。第三の設定では、標準的な肺がんスライドを深層学習ツールで仮想的な空間トランスクリプトミクスに変換し、SPIFEEのノードは低酸素、エストロゲン、JAK–STATシグナル伝達などの分子経路を表し、特徴は遺伝子活動から導出されました。これらすべての設定において、同一のフレームワークが異なるノードタイプを取り込みつつ比較可能な空間グラフを構築できました。
転帰を分ける相互作用を見つける
一度SPIFEEがグラフを構築すると、それをグラフアテンションネットワークに通します。これは、がんサブタイプや生存リスク、疾患と非がん性炎症の区別などの結果を予測するだけでなく、その予測に最も寄与したエッジを浮き彫りにすることを学習するニューラルネットワークの一種です。膵組織では、SPIFEEは慢性膵炎と膵管腺癌を従来のグラフベース手法より高い精度で識別しました。モデルは一貫して上皮様(腫瘍様)細胞と制御性T細胞、抗原提示細胞、ヘルパーT細胞を含む相互作用に注目し、炎症よりもがんで顕著な免疫抑制的な近隣環境を指摘しました。肺腺癌スライドでは、SPIFEEは生存と相関する特定の間質-腫瘍パターンを同定し、腫瘍と支持組織の“境界帯”が標準的解析では見落とされがちな重要な予後手がかりを符号化していることを示唆しました。
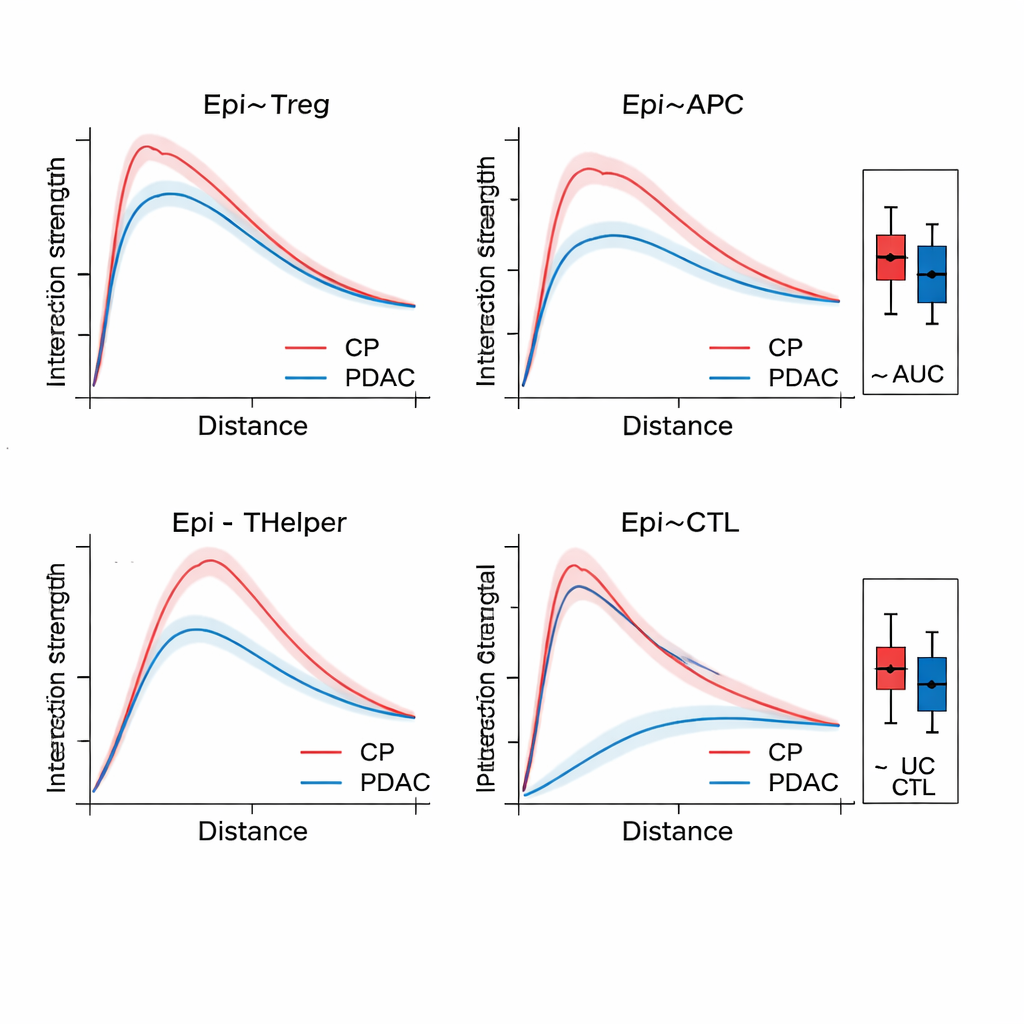
日常的なスライドから分子クロストークを読む
特に注目すべきは、SPIFEEが予測された遺伝子活性マップに翻訳された通常の病理画像から有意義な経路間相互作用を推定できた点です。経路をノード、空間的共起を機能的エッジとして扱うことで、手法は低酸素とEGFR、あるいはJAK–STATとPI3Kといった組み合わせを際立たせました。これらは既に肺がんにおける免疫回避や薬剤耐性を促進することが知られています。また、肺腺癌におけるエストロゲン関連経路や扁平上皮腫瘍における特定の免疫・ストレス経路を強調し、これらの所見はバルクRNAシーケンシングや独立した実際の空間トランスクリプトミクスデータセットで観察されたパターンと一致しました。分子計測が概算であっても、日常的なスライドの空間パターンには、生きた腫瘍内で主要な経路がどのように相互作用しているかに関する回復可能な信号が含まれていることを示唆します。
将来のがん医療にとっての意義
非専門家に向けた要点は、SPIFEEが画像や分子マップから直接、がん細胞の“社会的生活”を読み解く新しい手段を提供するということです。関係性を単一スコアに平坦化するのではなく、距離に応じてどのように変化するかを符号化し、注意機構を持つニューラルネットワークでどの相互作用が重要かをランク付けすることで、がんの種類を区別し生存を予測する細胞・組織パターン・経路の組み合わせを明らかにできます。これらの所見は依然として生物学的・臨床的な検証を必要としますが、SPIFEEのようなアプローチは、日常的な腫瘍検体が静的なスナップショットだけでなく、診断・リスク層別化・最終的には個別化治療の選択を導く相互作用のホットスポットの動的地図を提供する未来へと向かうことを示しています。
引用: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
キーワード: 腫瘍微小環境, 空間トランスクリプトミクス, グラフニューラルネットワーク, がん病理学, 細胞間相互作用