Clear Sky Science · ja
AI駆動の3D細胞内RPEマップが明らかにする上底-基底極性確立における細胞状態の遷移
なぜ眼の支持細胞が重要なのか
日々の鋭い視力は、眼の背面にある網膜色素上皮(RPE)と呼ばれる薄い支持細胞層に依存しています。これらの細胞が内部の秩序ある構造を失うと、加齢黄斑変性のような視力を奪う疾患が生じる可能性があります。本研究は、幹細胞生物学、高度な顕微鏡技術、人工知能、数学的モデリングを組み合わせて、RPE細胞の詳細な三次元「デジタルツイン」を構築し、成熟に伴って細胞内部の各部位がどのように再配列するか、またその過程が障害されると何が起きるかを明らかにします。
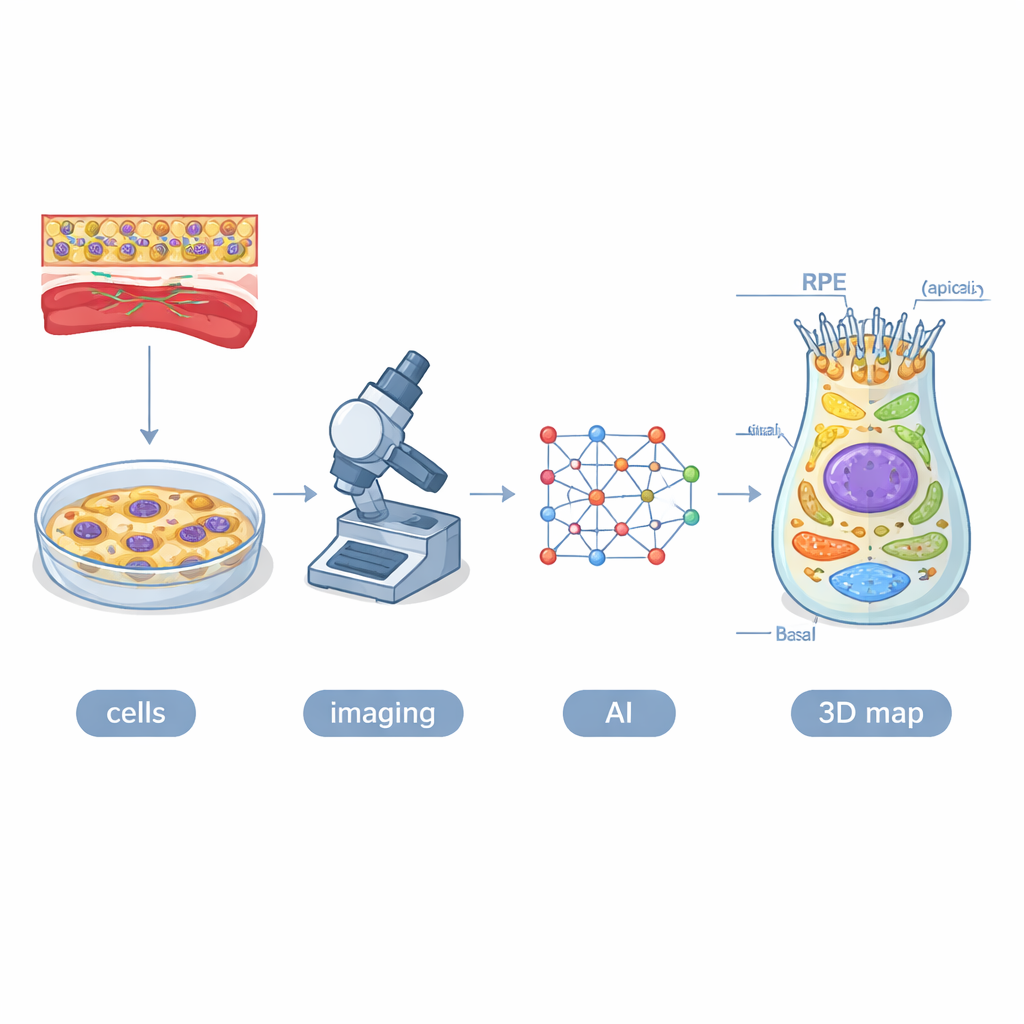
眼細胞のデジタルツインを構築する
研究者らはヒト誘導多能性幹細胞(胚細胞のように振る舞うよう再プログラムされた細胞)から出発し、それらをRPEへと分化させました。ミトコンドリアやリソソーム、細胞の外骨格など異なる細胞構造が顕微鏡下で緑に蛍光するように設計した16系統の細胞を用いました。4週間にわたり、高コンテント共焦点顕微鏡で約130万個の細胞を三次元で撮像しました。この膨大なデータセットを解析するために、POLARISと呼ばれるAIシステムを構築しました。これは各画像スライスで細胞、核、標識された細胞小器官を自動で輪郭抽出できるタイプのニューラルネットワークに基づきます。人間の専門家が機械の出力を検査・修正し、研究チームはその結果を各発達段階の代表的なRPE細胞の平均三次元モデル—デジタルツイン—に統合しました。
二つの経路:健康な成熟と極性の阻害
RPE細胞は、上側(頂端)と下側(基底)で異なる構造を持つ「極性」を獲得することで、栄養輸送、廃棄物の除去、網膜や血流とのやり取りを行います。これを促すために、研究チームは一部の培養にPGE2という分子を処理しました。PGE2は一次繊毛と呼ばれる小さな感覚構造の形成を促し、極性を強化します。他方でHPI4は繊毛に干渉して適切な極性形成を妨げます。POLARIS由来の測定により、健康な経路では細胞は高さを増して細くなり、核はよりコンパクトで丸みを帯びることが示されました。HPI4処理では細胞は平たく幅広いままで、形状はより不規則でした。統計モデルは、極性をうまく獲得する細胞ではこれらの形状変化が予測可能で非ランダムな順序に従うのに対し、極性が阻害された細胞はより変動が大きく無秩序な状態へと流れ込むことを明らかにしました。
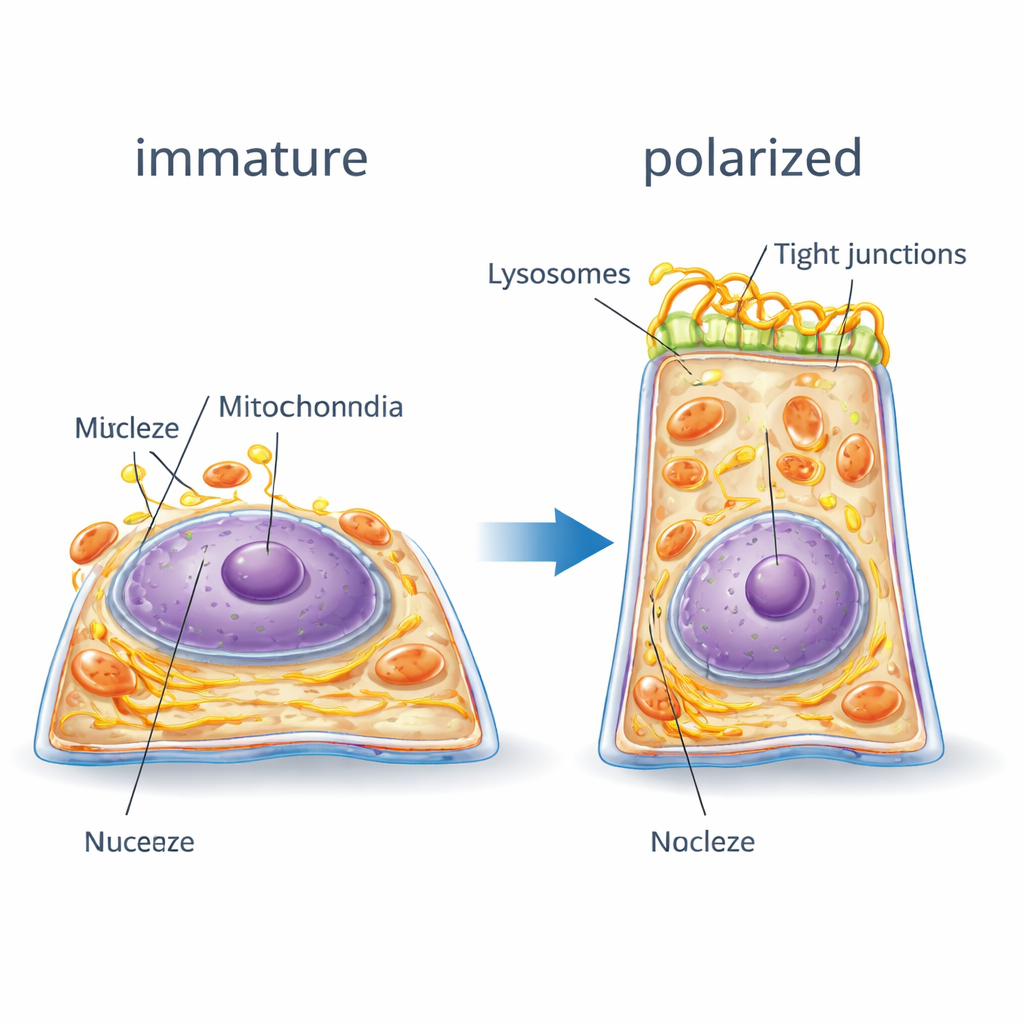
細胞内部はどのように再配置されるか
デジタルツインにより、細胞内部の構造がどのように再編されるかを追跡できました。RPE細胞が極性を獲得する過程で、アクチンやミオシンの繊維による内部の足場は多くの小断片から、細胞境界を取り巻くより少ない太い線維へと移行しました—ベルトを締めるように—新たな高い形状を支えます。核膜には深い折りたたみが現れ、核小体は減少する傾向があり、これはより成熟し安定した遺伝子発現プログラムの兆候です。隣接細胞をつなぐ接合タンパク質は細胞内部の散在した位置から側壁に沿った明瞭な帯へ移動し、バリアを強化しました。一方でエネルギーを生み出すミトコンドリアや、タンパク質・脂質の処理を助ける小胞体は拡大して核側へ移動し、より一貫したネットワークを形成しました。リソソーム(細胞のリサイクルセンター)は細胞の中央上部領域へと移動しました。極性が阻害されると、これらの再配置の多くは不完全か欠如し、小器官はよりランダムに分散したままでした。
小器官間の“対話”
研究チームはまた、どの小器官が細胞内の同じ近隣領域を占める傾向にあるかを調べ、機能的に相互作用している可能性を探りました。小器官のマップを平均細胞上に重ね、位置の相関の強さを算出したところ、よく極性化した細胞では構造が協調したクラスターにまとまっていることが分かりました。たとえば、ペルオキシソーム、ミトコンドリア、小胞体、特定の接合部位、および細胞骨格の一部が、エネルギー利用と膜再編成に関連する緊密に結びついたネットワークを形成していました。リソソームは細胞の中心的組織ハブである中心小体の近くに定着し、繊毛や表面更新の制御に関与していることを示唆しました。対照的に、極性が阻害された場合、これらの空間的関係は弱まり、小器官間の全体的な“対話”は断片化しているように見えました。これらの特徴で学習させた機械学習分類器は、ミトコンドリアの側方分布とタイトジャンクションの垂直配置が、細胞が適切に極性化されているかどうかを判定する際に特に強力な指標であることを示しました。
視力と疾患にとっての意義
AI、大規模イメージング、数学的解析を融合することで、本研究は健康なヒトRPE細胞が時間と空間の中でどのように自己組織化するか、そして極性が失われたときにその組織化がどのように崩れるかを詳細な3Dリファレンスとして提供します。専門外の読者への要点は、網膜の健康は単にどの分子が存在するかだけで決まるのではなく、各支持細胞内で細胞成分がどこに、いつ配置されるかによって左右されるということです。ここで作成されたデジタルツインは、患者由来RPEにおける微細な欠陥を定量的に検出するための物差しを提供し、網膜疾患における初期の細胞異常の診断や、視力が不可逆的に失われる前に正しい細胞構造を回復することを目指す治療法の評価に新たな道を開きます。
引用: Ortolan, D., Sathe, P., Volkov, A. et al. AI driven 3D subcellular RPE map discovers cell state transitions in establishment of apical-basal polarity. npj Artif. Intell. 2, 20 (2026). https://doi.org/10.1038/s44387-026-00074-6
キーワード: 網膜色素上皮, 細胞極性, 人工知能, 3D細胞マッピング, 加齢黄斑変性