Clear Sky Science · ja
拡散モデルによる相互作用制約付き3D分子生成は構造ベースのファーマコフォアモデリングを薬剤設計に可能にする
なぜより良い医薬品設計は難しいのか
現代の創薬はしばしば、小分子を鍵が錠に収まるようにタンパク質に合わせることに依存します。しかし鍵は単に収まるだけでは不十分で、弱い電気的引力や疎水的な領域の回避など、薬が強くかつ選択的に結合し続けるために必要な一連の微細な引き合いを形成しなければなりません。化学の宇宙は天文学的に広大で、現在のデータベースが収める範囲をはるかに超えているため、研究者はこれらの重要な接触パターンを保ちながらゼロから新しい鍵を賢く設計する方法を模索しています。
コンピュータに本当に重要なことを教える
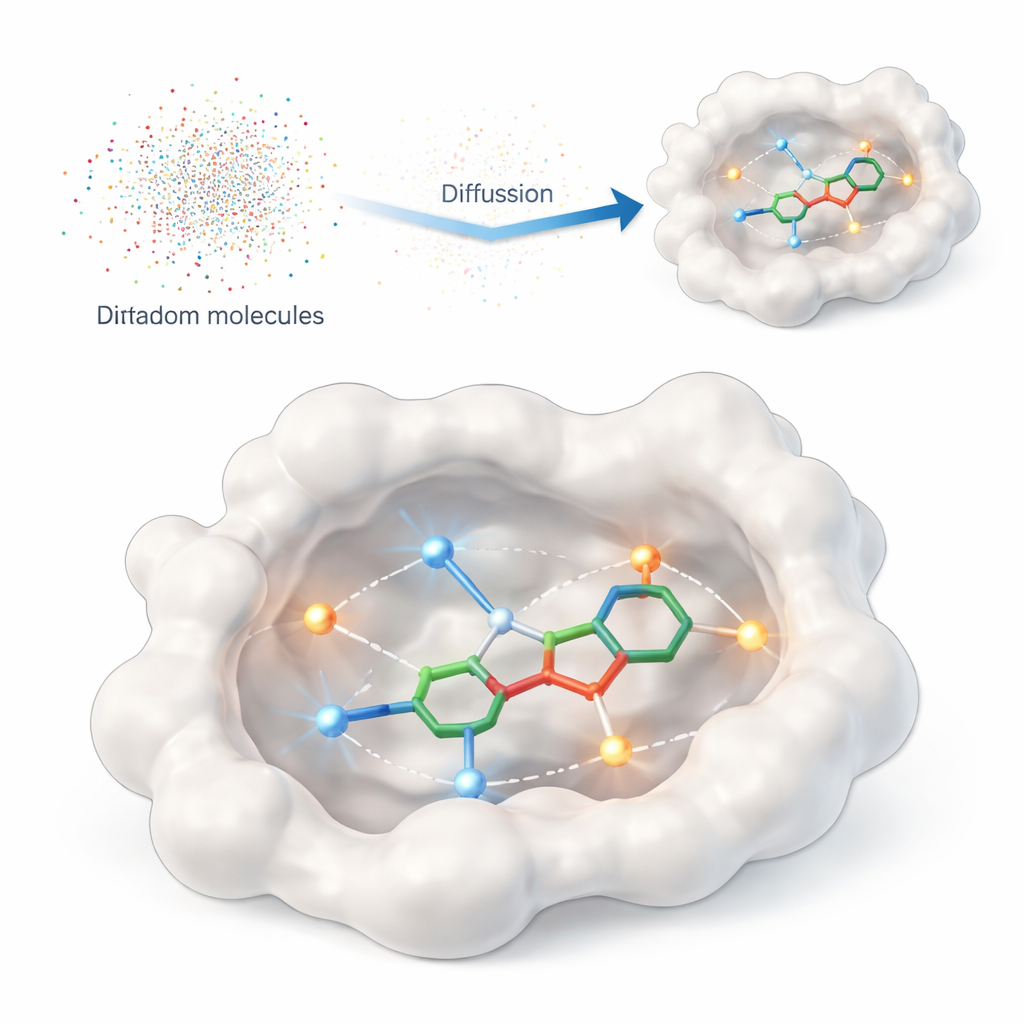
本研究はDiffPharmaを紹介します。これはタンパク質の結合部位の内部で直接三次元の薬物様分子を生成する計算フレームワークです。既存化合物の巨大なカタログを探索させる代わりに、DiffPharmaは原子ごとに新しい分子を作り出し、それらがタンパク質とどのように相互作用するかに従って生成を導きます。手法は拡散モデルと呼ばれる最新の生成モデルの一群に基づいており、ランダムなノイズから始めてそれを徐々に「脱ノイズ」して構造化された対象、ここではタンパク質ポケットに納まる3D分子を形成します。
タンパク質の握手を符号化する
モデルにタンパク質表面で何が重要かを伝えるために、著者らは主要な接触を参照分子とタンパク質の間の経路に沿って散りばめられた小さな「相互作用粒子」として表現します。強調される一般的な相互作用のタイプは二つあります:特定の原子間で方向性を持つ磁石のように働く水素結合、そして水から離れて油のような領域が集まる疎水性接触です。個別のニューラルネットワークが各相互作用タイプの幾何学と化学を学習し、さらに結合ポケットの全体形状を学ぶネットワークもあり、特別な融合アーキテクチャがこれらの視点を一つの一貫した像に統合して分子生成を導きます。
実際の結合パターンをどれだけ模倣できるか
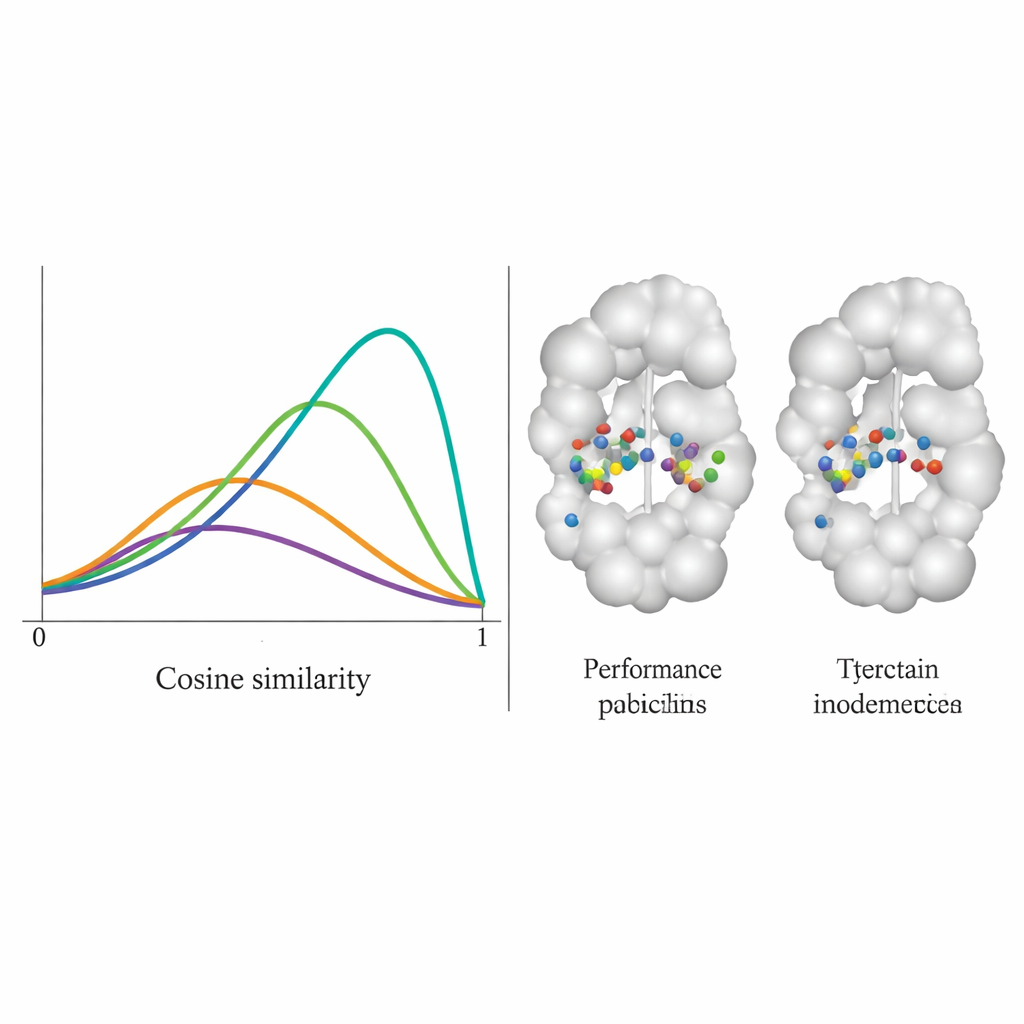
研究チームはDiffPharmaを100組の異なるタンパク質–分子ペアで評価し、新たに生成された分子がどれだけ元の接触パターンを残しているかを残基ごとに問いかけました。評価には0から1のコサイン類似度スコアを用い、1は完全一致を意味します。DiffPharmaの分布は約0.9付近にピークを示し、平均して同じタンパク質残基が参照構造と同じ種類の重要な相互作用を形成していることを示しました—6つの競合手法よりも大幅に優れています。重要なのは、モデルは分子形状の多様性を保ちつつ、生成化合物が実際の安定した分子に典型的な現実的な結合長や角度、全体の3D幾何を維持していた点です。
理論から実用的な薬剤候補へ
ベンチマークを超えて、著者らはDiffPharmaが実際のターゲット向けにもっともらしい薬剤候補を設計できるかを問いました。よく研究された二つの酵素—AKTキナーゼと抗生物質耐性に関連するβ‑ラクタマーゼ—に対して、手法は既知リガンドの本質的な相互作用パターンを保持しながらしばしば異なる化学スキャフォールドを使用する分子を生成しました。これは創薬化学における望ましい「スキャフォールドホッピング」の形です。より厳しい事例研究としてSARS‑CoV‑2のメインプロテアーゼでは、DiffPharmaを特定の相互作用選択で誘導し、分子動力学シミュレーションや結合エネルギー見積もりで検証しました。より厳しい相互作用制約下で生成された分子はより安定した複合体を形成し、時には既知の参照阻害剤よりも有利と予測される結合エネルギーを示しました。注目すべきは、訓練データに一度も現れていなかったにもかかわらず、システムがタンパク質構造と相互作用の指示だけからその参照化合物を再発見したことです。
将来の医薬品にとって何を意味するか
専門外の人にとって、DiffPharmaはタンパク質ポケットの形状と望ましい「握手」のパターンが与えられると、適切に収まり正しく相互作用する化学的に妥当な鍵を提案する賢い3D対応の設計ツールと考えられます。現在のところ溶解性や代謝など医薬品が必要とするすべての性質を最適化するわけではありませんが、この手法はタンパク質表面で重要な接触マップを確実に保持しつつ、現行のカタログを超えた化学空間の新領域を探索します。この相互作用指向のアプローチは、疾患関連タンパク質の構造データから実験的な薬剤開発のための多様で現実的な出発点へと研究者をより迅速に導くのに役立つ可能性があります。
引用: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
キーワード: 構造ベース薬物設計, 分子生成モデル, ファーマコフォアモデリング, タンパク質–リガンド相互作用, SARS-CoV-2メインプロテアーゼ