Clear Sky Science · ja
バーチャルスクリーニングと化合物有効性予測のためのAI誘導型競合ドッキング
新薬探索のための賢い探索
新薬の発見は、何百万もの分子から針を探すような作業です。本研究は、人工知能の最近の進歩が、どの分子が病気に関係するタンパク質に結合し、実際に薬として機能する可能性が高いかを予測することで、その探索をより速く、より安価にできることを示しています。研究者がラボで化学物質を一つずつ試す代わりに、著者らはAIモデルを使って分子同士を仮想的に競わせ、勝者を上位に上げる手法を採用します。
分子の鍵と錠前の適合をAIがどう学ぶか
多くの現代薬は、鍵が錠に合うのと同じように、タンパク質の小さなポケットにぴったり収まることで働きます。従来は、原子間の力を見積もる物理方程式でこの適合を予測してきました。しかしここ数年で、AlphaFold3やBoltzのような拡散ベースの共折りたたみモデルと呼ばれる新しいAIシステムは、大量の既知のタンパク質–分子構造から学習しました。これらのシステムは、実験構造が存在しない場合でも、タンパク質と候補薬が三次元でどのように折りたたまれるかを「想像」できるようになっています。著者らが取り組む中心的な問いは、これらのAIツールがもっともらしい絵を描くだけでなく、良い薬とそうでないものを見分けられるかどうかです。
本物の結合者と偽物
チームはまず、16種類のよく研究されたタンパク質に加え、DNAジャイレースというより複雑な細菌酵素をテストしました。各タンパク質について、AIモデルに既知の活性阻害剤と無関係の「オフトARGET」分子群の両方を同じ結合部位に配置させました。単一の予測を信用するのではなく、複数回の実行でAIが各分子をどれだけ一貫して配置するかを調べました。真の阻害剤は何度も同じ位置と向きに戻る傾向があり、数兆分の一メートル単位で集まってクラスタを形成しました。一方、非活性分子はより広く移動し、ポケットから離れていることが多かったのです。この単純な発想――配座の収束(pose convergence)――が、化合物が本当に標的タンパク質に適合する強い指標であることが示されました。
ドッキングを1対1の対戦に変える
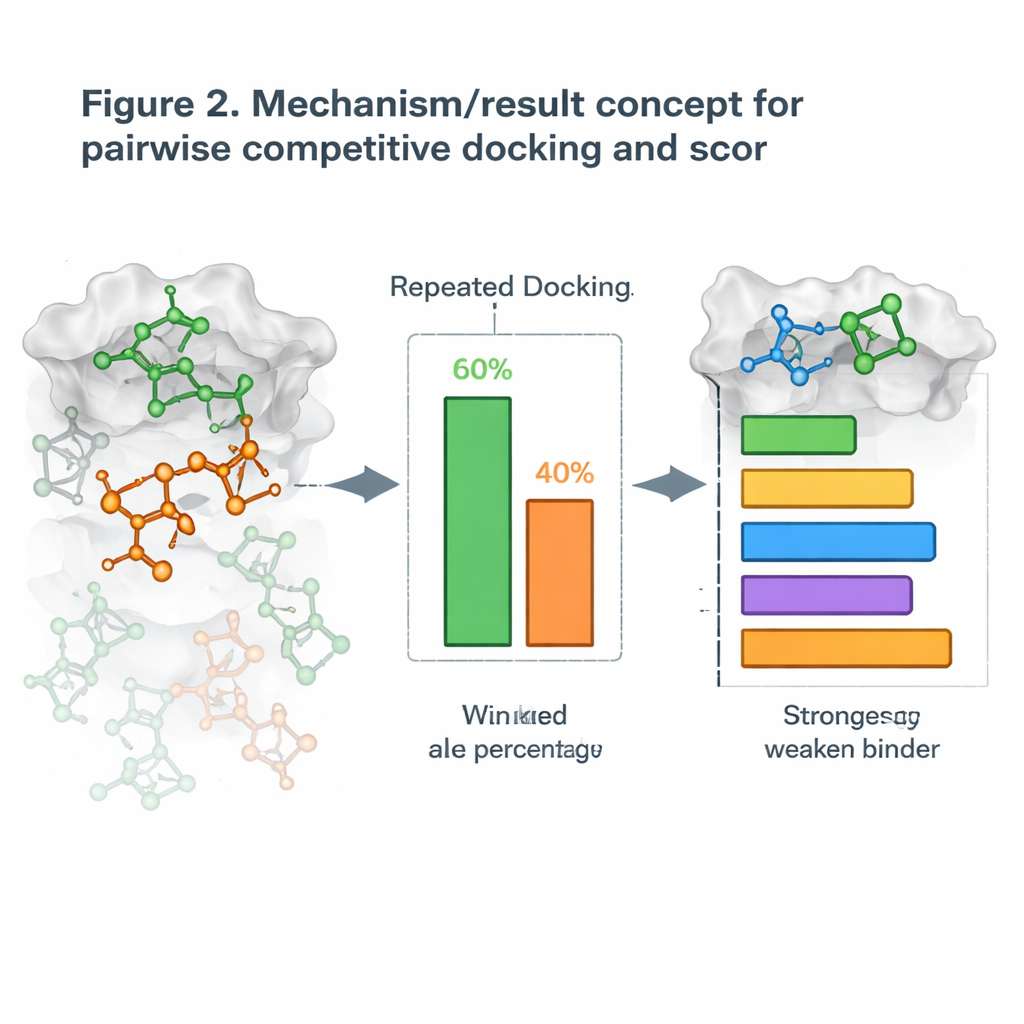
これを基に、著者らはペアワイズ競合ドッキングと呼ぶ新しい戦略を導入しました。分子を一つずつドッキングするのではなく、2つの候補を同時にタンパク質とともにドッキングさせ、同じポケットを「争わせ」ます。多数回の繰り返し実行の後、より頻繁にその部位を占める分子がその対戦の勝者と判定されます。全ての組み合わせを実行することで勝敗表を作り、各分子に対して競合ドッキングスコアを計算します。これは総当たりトーナメントでプレイヤーをランク付けするようなものです。これらのスコアを、実際に分子がどれだけ強く標的を阻害するかという実測値と比較すると、多くの場合で順位がよく一致し、あるタンパク質系ではほぼ完全に一致することもありました。
バーチャルスクリーニングからより良い抗生物質設計へ
細菌に必須の酵素であるDNAジャイレースは詳細なテストケースとして用いられました。このタンパク質には、フルオロキノロン類を含むさまざまなクラスの抗生物質が標的とする複数の薬剤ポケットがあります。AIモデルは通常、各薬剤クラスを正しいポケットに配置でき、競合ドッキングスコアは概ね測定された効力に従いました。著者らは次に、3000を超える承認薬のバーチャルスクリーニングに規模を拡大し、どの分子がフルオロキノロン部位で最も競り勝つかを問いました。彼らの二段階戦略――まず“同時競合”によって有力候補を選び、次にポケット内でどれだけ密集しているかでフィルタリングする――は、真のフルオロキノロンを大幅に濃縮し、弱い候補を除外しました。最後に、AI駆動の分子ジェネレーターを使って新しいフルオロキノロン類似構造を提案し、競合ドッキングを適用して、結合予測がより良く、薬物様性が許容範囲のものをいくつか見つけました。
約束、限界、そして患者への意味
本研究は、現代のAIモデルがもっともらしいタンパク質–薬物構造を描くだけでなく、競合という枠組みで実行すると、化合物をしばしば実験データと呼応する形でランク付けするのに役立つことを示しています。これはラボ作業に取って代わるものではありません――性能は特定のタンパク質に強く依存し、いくつかのポケットは誤予測され、非常に大きいまたは変わった分子ではAIが失敗することもあります。しかし、これらのモデルと訓練データが改善されるにつれて、ペアワイズ競合ドッキングのような手法は創薬初期をはるかに効率的にする可能性があります。患者にとっては、それが最終的に標的療法の開発を速め、耐性菌に対抗する新しい抗生物質の開発につながる可能性があります。
引用: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
キーワード: AIによる創薬, バーチャルスクリーニング, 分子ドッキング, タンパク質–リガンド結合, 抗生物質設計