Clear Sky Science · ja
がん免疫療法のためのマクロファージ工学:新たな知見と治療の可能性
体内の“清掃部隊”をがんと戦う戦士に変える
私たちの体にはマクロファージが多く存在します。これらは遊走する“清掃”細胞であり、病原体や死んだ組織を取り込んで処理します。本レビューは、研究者たちがどのようにこれらの細胞をがん攻撃へ向け直しているかを探ります。マクロファージは腫瘍内に豊富に存在し、現在の主要な免疫療法に抵抗する腫瘍にも多く見られるため、それらを理解し工学的に改変することは、治療が難しいがん患者に新たな選択肢を開く可能性があります。
一つの細胞種に現れる多様な姿
マクロファージは単一の固定された細胞種ではなく、形を変える能力を持ちます。血流からやって来るものもいれば組織に常在するものもあり、局所のシグナルに応じて応答します。腫瘍に存在する腫瘍関連マクロファージは、がん細胞の殺傷を助ける場合もあれば、逆に腫瘍の成長や転移を助長する場合もあります。以前は研究者たちはそれらを“M1”(攻撃モード)と“M2”(修復・支援モード)の二つに単純化して扱ってきました。だが、新しい遺伝学的および空間的マッピング手法は、より多様な状態のスペクトルを明らかにし、複数の亜群と振る舞いが腫瘍や部位ごとに異なることを示しています。かつて明確に“腫瘍促進”と考えられた細胞でさえ、状況によってはT細胞を呼び寄せ抗腫瘍免疫を支えることがあり得ます。
周囲を感知し、がん細胞を貪食する
マクロファージは化学的シグナルを受け取るだけでなく、周囲の物理的環境も感知します。腫瘍の密なタンパク質網を這い、細胞間を押し分け、流体力学的な力に耐えながら、Piezo1などの特殊な受容体を通じて硬さやひずみを感じ取ります。こうした機械的手がかりは、古典的な免疫シグナルとともに、マクロファージを炎症寄りか鎮静寄りかに傾けます。機能的には、マクロファージはがん細胞を取り込み、分解して断片(抗原)をT細胞に提示し、自然免疫と獲得免疫の橋渡しをします。がん細胞は抵抗として「食べないで」というシグナルを送り、代表的には表面分子CD47を介してマクロファージのブレーキに結合します。この相互作用を阻害する薬剤は多くの臨床試験で検討されており、がん細胞の排除を促進しますが、正常細胞への影響を避けるために慎重な調整が必要です。
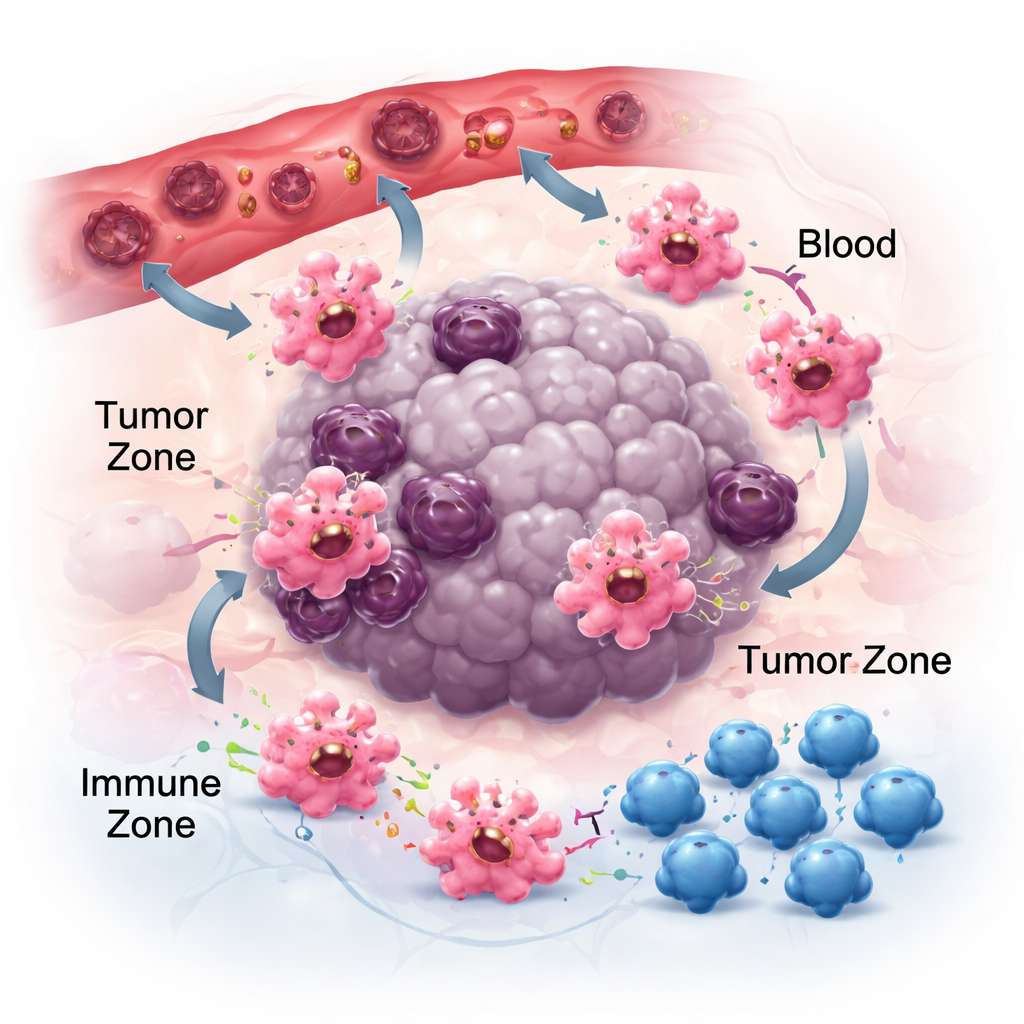
腫瘍の“近所”での移動、接着、情報伝達
がんで効果を発揮するためには、マクロファージはまず腫瘍に到達し、適切なニッチに位置する必要があります。彼らは化学的な足跡—ケモカインや増殖因子—に従って移動します。CCR2–CCL2のような対はマクロファージを腫瘍へ引き寄せるのに役立ち、これらの信号を遮断する薬剤はマクロファージの蓄積を減らしますが、それでも完全には阻止できず、CSF-1やVEGFなど他の誘因が関与していることを示唆します。定着後、局所マトリックスへの接着の仕方も彼らの振る舞いを左右します。インテグリンと呼ばれる接着受容体は単なる接着剤ではなく、炎症シグナルを増幅し、細胞をより腫瘍と戦う状態へと導くことがあります。同時に、マクロファージはRNAやタンパク質を運ぶ小さな小胞(細胞外小胞)を放出し、近隣の細胞と通信します。腫瘍の種類によって、これらの小胞は免疫を抑制し転移を助ける場合もあれば、抗腫瘍応答を強化する場合もあり、マクロファージのコミュニケーションが文脈依存であることを強調しています。
遺伝子と材料でマクロファージを再プログラムする
マクロファージは多くのT細胞よりも固形腫瘍へ自然に浸潤するため、研究者たちはそれらを“生きた医薬品”として再設計しつつあります。一つの遺伝的戦略はキメラ抗原受容体(CAR)T細胞療法からの発想を借り、合成受容体を加えてCARマクロファージ(CAR-M)を作ることです。これらの設計細胞は腫瘍マーカーを認識し、がん細胞をより効率的に貪食し、周囲のマトリックスを分解し、炎症性シグナルを放出し、腫瘍抗原を提示してT細胞を活性化します。HER2を標的としたCAR-Mの初期のヒト試験は安全性と生物学的活性で有望な結果を示していますが、強く持続的な効果を証明するにはさらなる取り組みが必要です。並行して、非遺伝的アプローチでは脂質や高分子で作られた粒子や“バックパック”が使われています。マクロファージは薬物を搭載したナノ粒子を取り込み、トロイの木馬のように腫瘍深部まで運ぶことができるほか、表面に付けたパッチが免疫増強シグナルをゆっくり放出して腫瘍と戦う性格を維持させる手法もあります。マクロファージ由来の小胞自体も、天然の細胞非依存型の送達手段として試験されています。
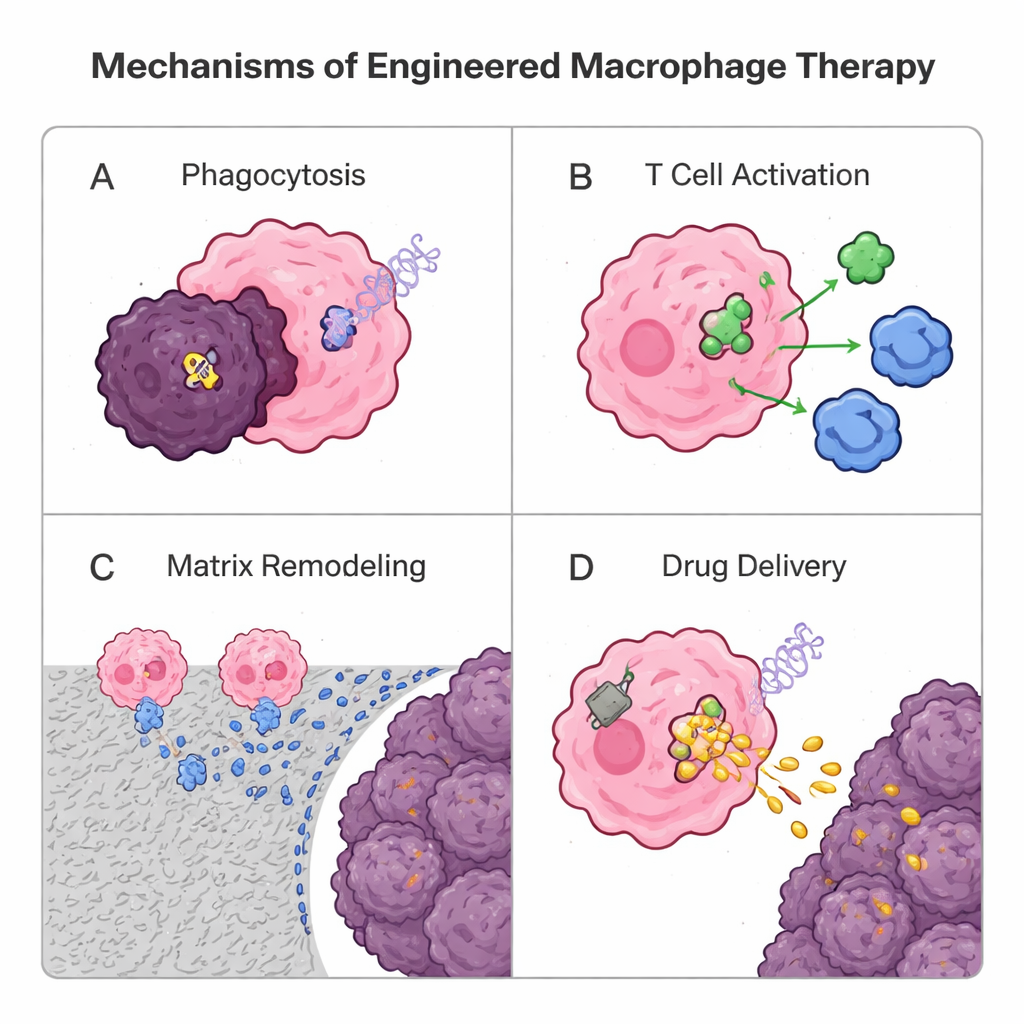
残る課題と希望の理由
有望である一方、マクロファージ治療には実際的なハードルが残ります。患者から十分で一貫した細胞を産生するには時間とコストがかかり、注入後のこれらの細胞は無限に生存・増殖するわけではありません。彼らの生得的な可塑性は生物学的には有益ですが、複雑で抑制的な腫瘍微小環境内で抗腫瘍モードに固定しておくことを難しくします。著者らは、実際の組織の力学を模倣する3D培養、オルガノイド、オルガンオンチップといった高度なバイオ工学モデルが、改変マクロファージの患者内での挙動を理解・予測するうえで重要になると論じています。それでも、固形腫瘍へ浸潤し、がん細胞を取り込み、T細胞を目覚めさせるという本来の能力と、初期の安全性実績を合わせると、マクロファージベースの治療は特に現在の免疫療法に抵抗する“コールド”腫瘍に対して重要な新しい武器となる可能性があると示唆されます。
引用: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
キーワード: マクロファージ免疫療法, 腫瘍微小環境, CARマクロファージ, 貪食作用, ナノ粒子薬物送達