Clear Sky Science · ja
26SプロテアソームにおけるATP駆動タンパク質伸展の非平衡化学機械変換
小さな機械が私たちのタンパク質を整える仕組み
細胞内には、26Sプロテアソームと呼ばれる微小なシュレッダーがあり、損傷したり不要になったタンパク質を常に分解して細胞の健全性を保っています。この機構の中心には、化学燃料(ATP)を消費してタンパク質をつかみ、伸展させ、中央の分解チャンバーへ引き込む環状のモーターがあります。本論文は高度なコンピュータシミュレーションを用いて、そのモーターが化学エネルギーをどのように機械的運動へ変換するかを明らかにし、老化、神経疾患、免疫、がんに関わる過程の詳細で定量的な像を提示します。
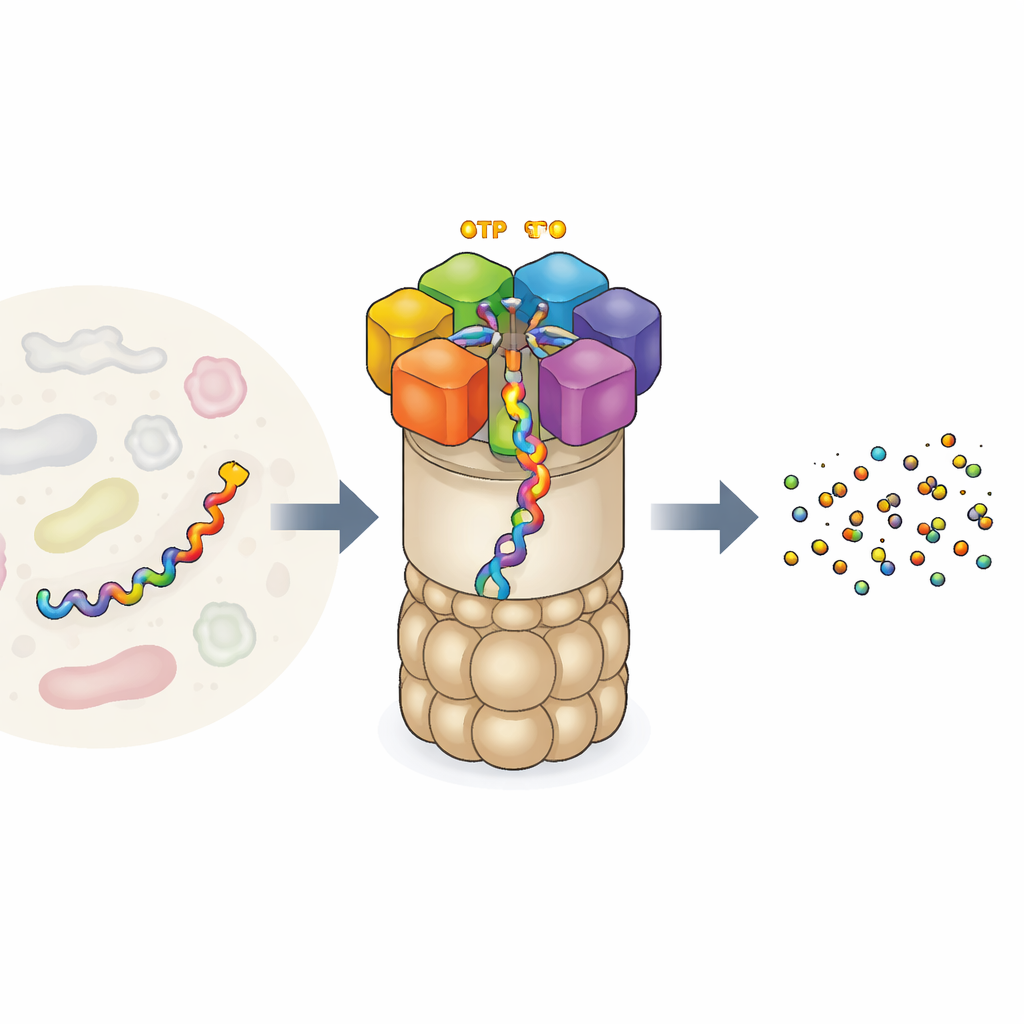
細胞のタンパク質リサイクル工場
26Sプロテアソームは細胞内で最大級かつ最も複雑なタンパク質機械の一つです。タンパク質を切断する樽状のコアと、どのタンパク質を破壊するかを認識する規制キャップから成ります。通路の入口には六つの異なるモーター単位が環状に並んでいます。各ユニットは細胞の普遍的なエネルギー通貨であるATPを結合でき、そのエネルギーを使ってタンパク質鎖をつかみ、コアへ引き込んで分解します。このモーターはランダムに動くわけではなく、以前の実験は六つのユニットが協調した「手渡し(hand-over-hand)」の様式で動作し、ロープ上の登山者のようにタンパク質を渡していくことを示唆していました。しかし実験ではその一連の動作の断片しか見えず、運動の完全な順序や燃料の消費がどのように機械的仕事に結びつくかに関しては不明点が残っていました。
分子綱引きをシミュレーションする
著者らは、モーターをATPやその生成物が結合・解離する間に多くの形状を行き来する系として扱う確率的コンピュータモデルを構築しました。彼らは、環の主要な30のコンフォメーションを定義し、そのうち1つ、2つ、3つのモーターサブユニットがタンパク質の保持を失う状態と、六つ全てがしっかり保持する特別な閉じた状態を含めました。標準的なランダム化学事象のシミュレーションアルゴリズムを用いて、ATP結合、ATP分解、モーター形状変化が起こる数十万のステップを追跡しました。これらの実行から、ATPやその消費形態であるADP、実験でよく用いられる分解されないATP類似体の量を変えた場合など、さまざまな条件下でタンパク質がどの速さで引き込まれるかを予測できました。
燃料が増えすぎるとモーターが遅くなるとき
シミュレーションは幾つかの不可解な実験結果を再現しました。ATP濃度が低い値から上がるにつれて、燃料結合が律速段階であるためモーターはより速くタンパク質を引っ張ります。しかし約1ミリモーラーを超えると速度は頂点に達し、その後低下します:環はATPで占有されているにもかかわらずタンパク質が移動しないジャムした非移行性コンフォメーションにより長く留まるためです。ADPや分解されないATPアナログを加えると、これらの分子がATPと結合部位を競合するが完全な駆動ストロークを完了できないため、モーターは着実に遅くなります。モデルはまた、タンパク質の非常に安定した折りたたみ領域に直面したときの振る舞いも予測します。それらは道路の障害物として作用し、モーターは抵抗に対してより長く苦闘し、全体の分解速度が低下します。これは人工的に安定化したタンパク質ドメインを用いた測定と一致します。
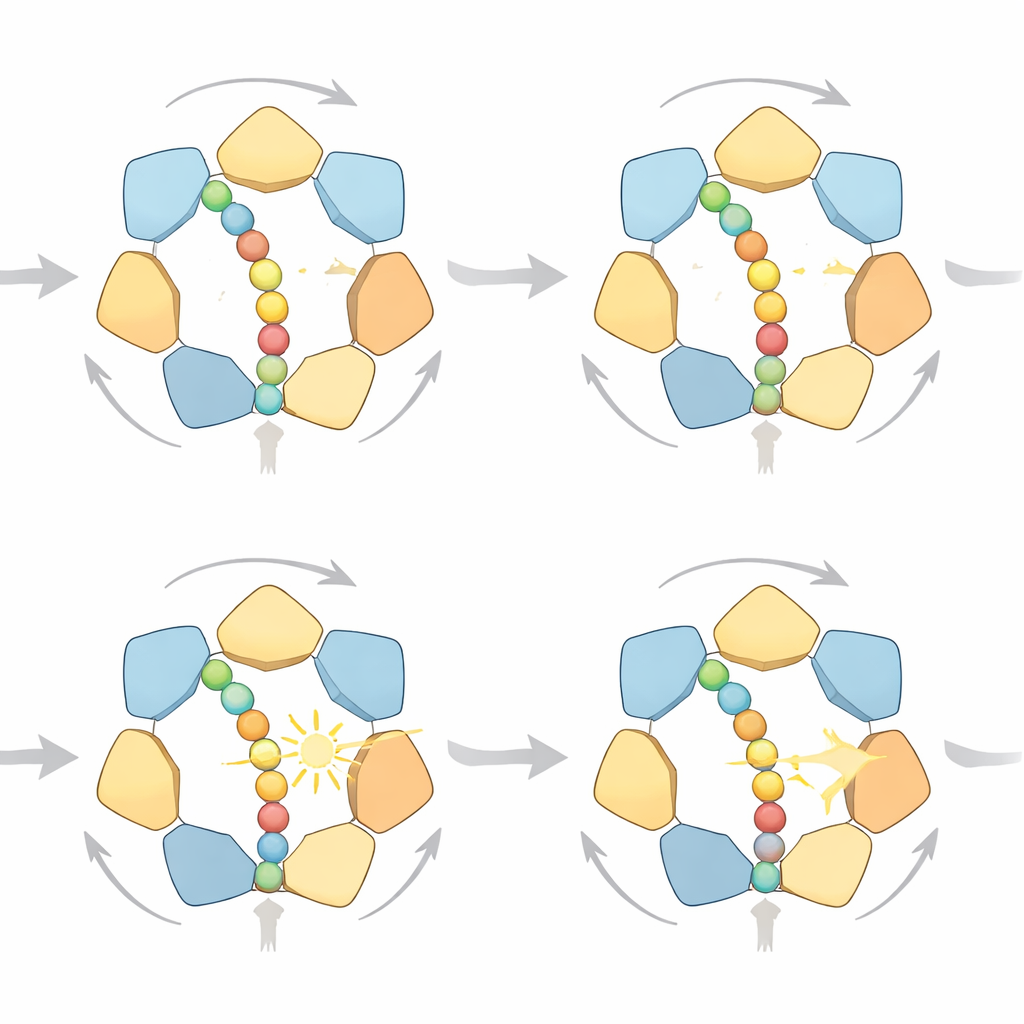
一歩を踏む多様な方法
シミュレーション軌跡を詳しく調べることで、研究者らは環が単一の剛直なサイクルに従っていないことを発見しました。代わりに、すべて同じ方向性の「手渡し」ルールを守りつつ複数の高確率経路が存在します:環の出口付近のサブユニットはATP分解後にタンパク質を放し、サブユニットの螺旋状の階段を上ってトップに移動し、鎖をより上方で再びつかみます。タンパク質の進みが一度に一小歩のときもあれば、同時に二つのサブユニットが離れることで二歩分進むこともあります。燃料が豊富な場合は抵抗に対して無駄な仕事が少ないため一歩動作が優勢になりますが、燃料が乏しいとモデルは二歩ジャンプがより頻繁になると予測します。シミュレーションはまた、機械的負荷とモーターの化学状態を結びつけます:抵抗が増してタンパク質が停滞すると、六つの結合ポケットのより多くにADPが蓄積する傾向があり—これは高分解能構造研究で観察されるものと一致します。
エネルギー使用と共有された設計原理
モデルにより、ATPが分解されるときにモーターのエネルギーがどのように上昇し、そのエネルギーが運動に変換されるときにどう低下するかを可視化できます。彼らは効率曲線を算出し、モーターが中程度の対抗力で最もよく働くことを示しました:抵抗が小さすぎるとATPを無駄に消費し、大きすぎると事実上停止に近づきます。チームが予測を細菌や酵母の関連するタンパク質分解機構のデータと比較すると、分解されないATP類似体がこれらのモーターを遅らせる傾向に非常に似た傾向が見られました。これは、環状酵素ファミリーの多くのメンバーがタンパク質を引っ張るための共通で保存されたメカニズムを共有している可能性を示唆します。
健康と疾患にとっての意義
散発的な構造スナップショットや生化学的測定を単一の検証可能な枠組みに統合することで、この研究は微小な分子モーターが化学燃料を力に変えて細胞のタンパク質をリサイクルする仕組みを定量的に示します。モデルは既存の幅広い実験を説明するだけでなく、燃料レベル、機械的負荷、あるいはモーター変異がタンパク質破壊をどのように変えるかについての予測も行います。類似の機械があらゆる生命形態で働き、神経変性からがんに至るまでの状態に中心的役割を果たすため、このレベルで内部の仕組みを理解することは、これらの微視的シュレッダーを調整、強化、あるいは選択的に阻害する薬剤設計の指針となる可能性があります。
引用: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
キーワード: プロテアソーム, AAA+ ATPアーゼモーター, タンパク質分解, 分子機械, 化学機械結合