Clear Sky Science · ja
生体内でのグルコース濃度を連続モニターするための微生物機能を利用したマイクロ流体バイオセンサー
糖尿病の人にとってこれが重要な理由
1型糖尿病とともに暮らす人々にとって、現在の「人工膵臓」システムは依然として継続的な注意を必要とします—食事の入力、アラーム対応、夜間の低血糖への不安などです。本研究は、単一の酵素やコンピュータの式に依存するのではなく、身体自身の糖制御機構の小さな生きた一部を借用するという、全く異なる種類のグルコースセンサーを検討します。具体的には膵臓の細胞クラスターである膵島というミニ臓器を用います。進化が最適化してきたこれら小さな臓器に自然な働きをさせることで、将来的により賢く、安全に、より独立してバックグラウンドで作動するグルコースモニターの構築を目指しています。
生きたセンサーとしての微小な臓器
現在の多くのバイオセンサーは、精製された分子や単一の細胞系を用いて化学物質を検出します。それらは特定の物質に反応し、生の信号をソフトウェアに渡して解釈させます。著者らは、このアプローチが強力な内在的「コンピュータ」を見落としていると主張します。膵島のようなマイクロ臓器は、多数の信号を同時に感知し、協調的な応答へと変換することを自然に行います。各膵島は複数のホルモン産生細胞を含み、これらは常に相互に情報をやりとりしています。膵島は血糖だけでなく、アミノ酸、腸やストレスホルモン、そして直近の高低の履歴にも反応し、総体として血糖を狭い安全な範囲に保ちます。著者らは、この内在的な複雑さが、単純なグルコースオキシダーゼセンサーよりも豊富で信頼できる情報を生み出すために活用できると示唆します。
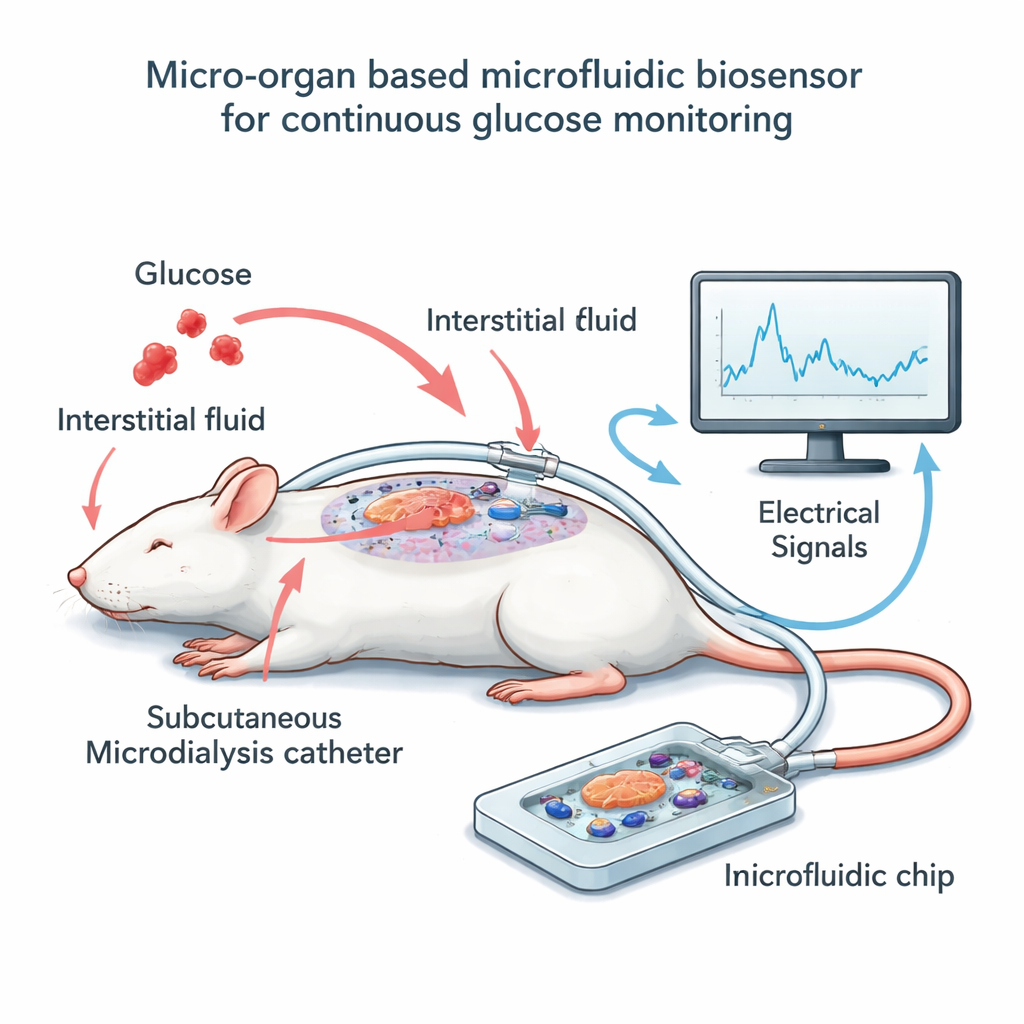
チップとカテーテルのシステム構築
この考えを検証するために、研究チームは体外に小さな装置を作り、数十個のマウス膵島を微小電極の格子の上に配置しました。これらの細胞を血液に直接さらす代わりに、マイクロダイアリシスと呼ばれる手法を用いました:細く柔軟なカテーテルを麻酔したラットの皮膚のすぐ下に置き、周囲の組織液を緩やかに採取します。この組織液は血糖にほぼ対応しますが短い遅延があります。低速で一定の流量がこの液を狭いチャネルを通してチップ上の膵島の上に運びます。ダイアリセート中のグルコース濃度が上昇・下降すると、膵島は電気活動を変化させ、電極はそれを遅い波状の信号として捉えます。同時に研究者らは定期的にラットの血液およびダイアリセート中のグルコースを測定し、電気的な読み出しを実際の糖濃度と時間軸で整合させました。
変化する糖に対する生きたセンサーの応答
まず、電極上の膵島が単純な実験室溶液ではなく実際の血液成分に反応できるかを試しました。異なるグルコース濃度のヒト血清およびラット血清に暴露したところ、電気波の頻度と大きさの両方に明確で段階的な変化が見られました。応答は糖濃度の小さな変化を、糖尿病に関連する範囲で識別できるほど十分に強いものでした。次にラット実験に移行し、血糖を上げるためにグルコース注射を行い、その後インスリンを注射して下げました。血液から組織液への移動や配管を通るのに要する時間を考慮した後、膵島の遅い電気信号の頻度は血糖とほぼ一致して上昇・下降することがわかりました。複数の動物にわたる統計解析は、信号頻度とグルコースレベルの間に驚くほど緊密で再現性のある関係を示しました。一方で信号の振幅も情報を含んでいましたが、やや変動が大きめでした。
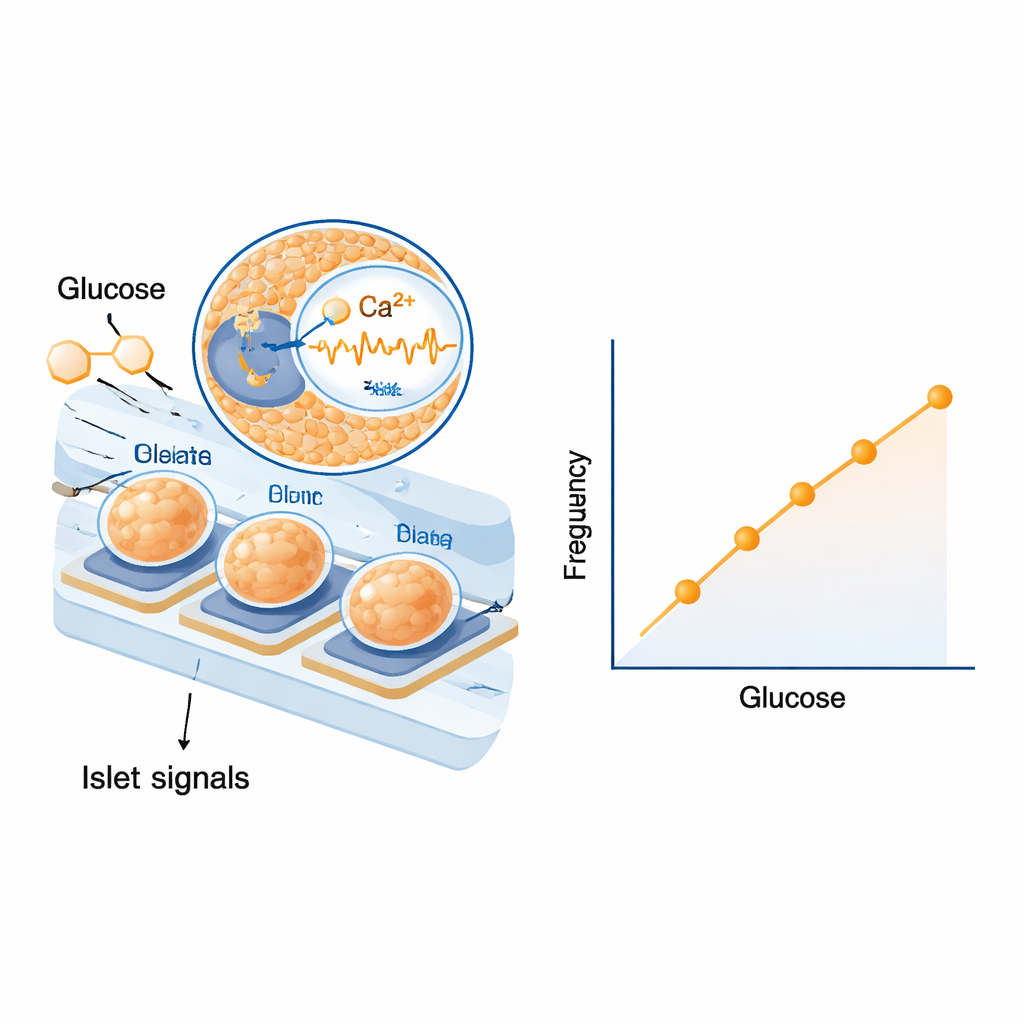
生物学から得られる組み込まれた安全機能
単一分子を使うのではなく全膵島を使う重要な利点は、その挙動に進化が形成した安全機構があらかじめ組み込まれている点です。以前の研究や本研究の示唆は、膵島がグルコースが上昇しているときよりも下降しているときに強く反応することを示しており—いわば「ヒステリシス」の一形態で—危険な低血糖から守るのに役立ちます。電気パターンはまた、インスリン放出を増幅または抑制する周辺の細胞型によって形作られます。チップはこれらの統合された信号を単に傾聴するだけで、色素や遺伝子改変を加えないため、細胞を傷つけずに数日間記録できます。著者らは技術的な課題も指摘しており、気泡の回避、長期マイクロダイアリシス性能の確保、そして最終的にどのようなヒトまたは幹細胞由来の膵島を使用するかの決定などが挙げられます。それでも、確立された糖尿病モデルを用いたコンピュータシミュレーションは、このような膵島ベースのセンサーが困難な条件下で現在のグルコースモニターに匹敵またはそれを上回る可能性があることを示唆しています。
将来の糖尿病ケアにとっての意義
この研究は、チップ上で生かされ、細いカテーテルで体につながれた少数の膵マイクロ臓器が、生体内で自然な電気的ざわめきによって血糖を連続的に追跡できることを示しています。専門外の人にとっての鍵は、単純な化学センサーにグルコースを測らせてからコンピュータにそれが体にとって何を意味するかを推測させるのではなく、通常インスリン量を決定している同じ種類の生きた組織の声に直接耳を傾けるという点です。もし改良され人体で実用化されれば、そのような生体センサーは真に自律的な人工膵臓システムの中核となり得ます—身体のニーズを先読みして静かに応え、日々の糖尿病管理の負担を軽減する装置です。
引用: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
キーワード: 持続血糖モニタリング, 人工膵臓, 膵島, マイクロ流体バイオセンサー, 1型糖尿病