Clear Sky Science · ja
ハイブリッドマウスモデルにおける加速かつ局在化したシヌクレイノパチー:陽電子放射断層撮影研究への示唆
この研究が重要な理由
パーキンソン病は振戦や運動障害でよく知られていますが、脳の奥では見えにくい小さな変化から始まります。医師はこれらの変化を早期に検出し、新薬を迅速に評価する方法を切望しています。本論文は、数週間という短期間でパーキンソン様の脳障害の主要な特徴を特定の脳領域に再現し、PET(陽電子放射断層撮影)といった高度な脳イメージングに適した改良マウスモデルを記述します。 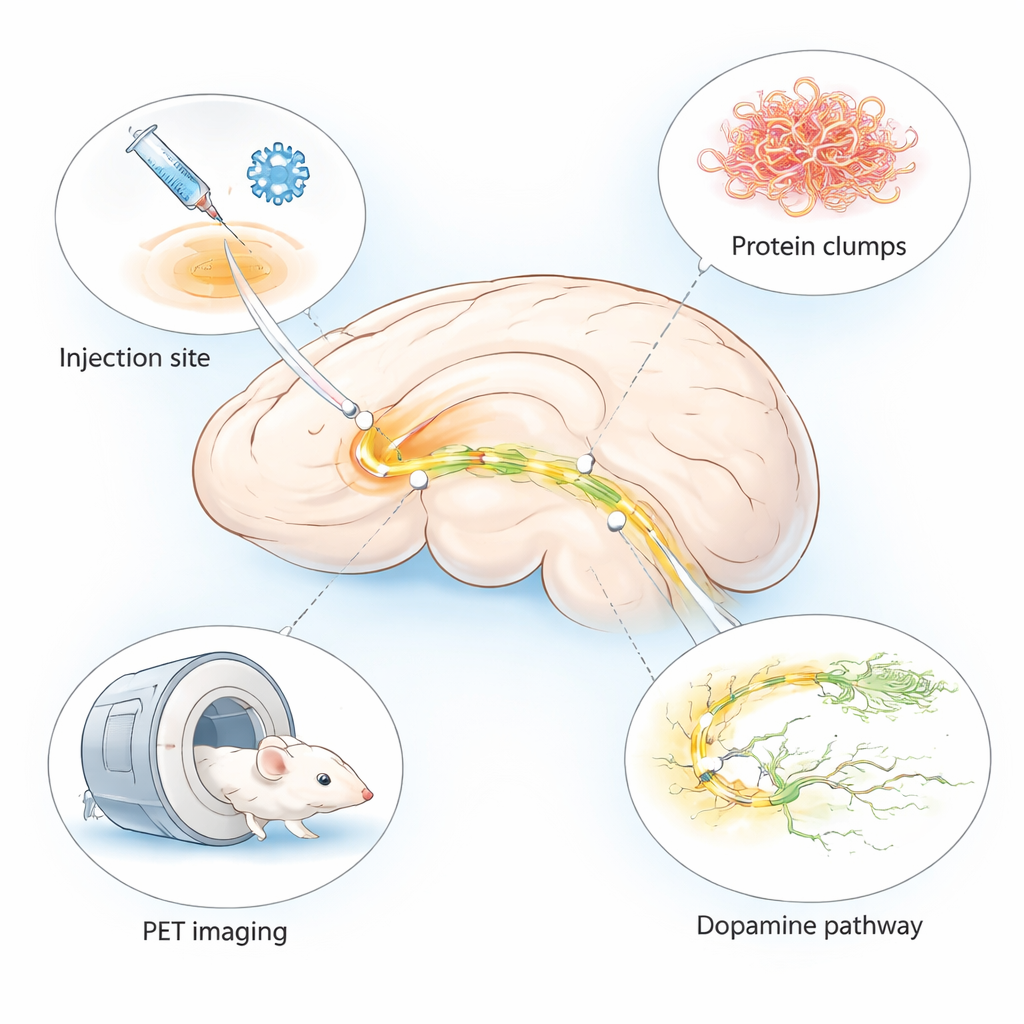
より速く、より局在化した疾患モデルの構築
既存の多くのパーキンソン病動物モデルは、症状の出現に数か月を要したり、患者で見られる脳変化の全貌を示さなかったりします。著者らは二つの確立された手法を組み合わせて“ハイブリッド”モデルを作成しました。無害なウイルスを注入して脳細胞にヒトのα-シヌクレインを産生させると同時に、すでに形成された線維(プリフォームドフィブリル)を注入して凝集を促す種として作用させました。いずれもマウス脳の一側の運動に関わる小さな領域である黒質に投与しました。この設計により、注入側に局所的かつ強度の高い病的変化が生じ、反対側は比較用に比較的健康なまま残ります。
タンパク質凝集と神経細胞死の追跡
注入からわずか2週間で、対象領域において高レベルのヒトα-シヌクレインとその異常なリン酸化型が検出されました。顕微鏡下では、パーキンソン病の特徴であるレビー小体やレビー神経突起に類似した構造が観察されました。以降数週間でこれらの異常沈着は増加しました。同時に、滑らかな運動に重要な神経伝達物質ドーパミンを産生する神経細胞が減少し始めました。これらの細胞のマーカーは5週目までに未処理側の約60%まで低下し、ドーパミン系の明確で進行性の喪失を確認しました。
炎症、シナプスの減少、疲弊したエネルギー工場
脳の免疫細胞であるミクログリアも損傷領域の周囲で強い活性化・炎症状態に移行しました。複数の炎症関連タンパク質の染色は、α-シヌクレイン沈着の近傍で反対側よりもはるかに強く出ました。過程の後期には、神経細胞の接点であるシナプスの喪失や、細胞のエネルギー工場であるミトコンドリアの機能不全の兆候も検出されました。これらの所見は、このモデルが単にタンパク質の凝集を作り出すだけでなく、炎症、接続の破綻、エネルギー問題という神経細胞死に寄与する連鎖反応も再現していることを示します。 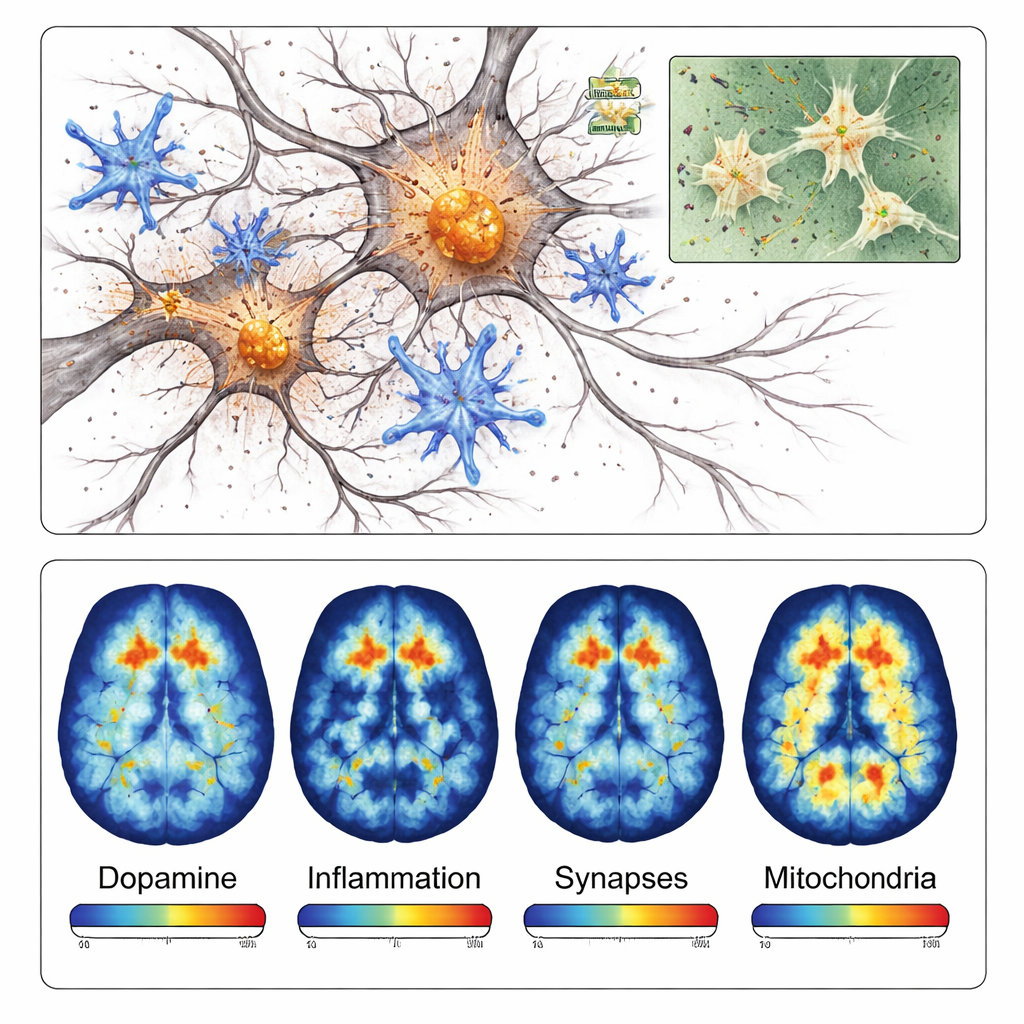
PETスキャナーの活用
このモデルは局在化しており発症が速いため、生体脳内の特定分子を測定できる陽電子放射断層撮影(PET)に特に適しています。研究者らは、ドーパミン神経終末、活性化したミクログリア、シナプスタンパク質、およびミトコンドリア酵素に結合する4種類のPETトレーサーを評価しました。いずれの場合も、PETスキャンは注入側で顕微鏡所見と一致するように信号が低下または上昇していることを示しました。たとえば、ドーパミン経路を標的とするトレーサーは損傷側で約40%信号が低下し、炎症トレーサーは影響を受けた領域で40%以上信号が上昇しました。
患者と将来の治療への意義
この新しいマウスモデルは、短期間でパーキンソン病患者の脳で何年にもわたって生じる主要な変化の多くを結集します。損傷が小さく明確に定義された領域に限局され、PETで追跡できるため、研究者は新しいイメージングトレーサーや治療候補をより効率的に評価できます。どのマウスも人間の状態を完全に再現することはできませんが、このアプローチは基礎研究と臨床研究の橋渡しをする強力かつ実用的なツールを提供し、診断の洗練とより良い治療法の探索を加速する助けとなります。
引用: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
キーワード: パーキンソン病, α-シヌクレイン, シヌクレイノパチー, PETイメージング, マウスモデル