Clear Sky Science · ja
STAR(stroma‑tumor AI risk)評価:AIにより算出された腫瘍‑間質比が上皮性卵巣がんの生存と関連し、KELIMを超えた付加的予後情報を提供する
腫瘍の「近隣環境」が重要な理由
がんを思い浮かべるとき、私たちはしばしば異常な細胞の集合体を想像します。しかし腫瘍は支持組織、血管、免疫細胞といった多様な構成要素がひしめく「近隣」に存在します。これらを総称して間質(ストローマ)と呼びます。本研究はシンプルだが強力な疑問を投げかけます。日常的な顕微鏡スライド上で人工知能(AI)が測定する腫瘍細胞と周辺組織の比率(腫瘍–間質比:TSP)を用いて、治療開始前にどの卵巣がん患者がより良い、あるいはより悪い転帰をたどるかを予測できるか、という問いです。
標準的な生検スライドを新しい視点で読む
上皮性卵巣がんの女性は通常、手術または生検で組織を採取します。これらのサンプルは染色され、すべての病院の顕微鏡で検査されます。研究者たちは腫瘍–間質比(TSP)という特徴に注目しました:画像のどれだけの部分ががん細胞に対して支持組織で占められているか、という指標です。従来の研究では病理医が目視でこの比率を推定し、間質が豊富な腫瘍はしばしばより攻撃的に振る舞い、標準的な白金系化学療法に抵抗することが示されていました。本研究では、チームは深層学習を用いたAIシステムでデジタル化されたスライド上のTSPを自動測定し、手作業で主観が入る作業を診断時点で迅速かつ再現性のある指標に変えようと試みました。
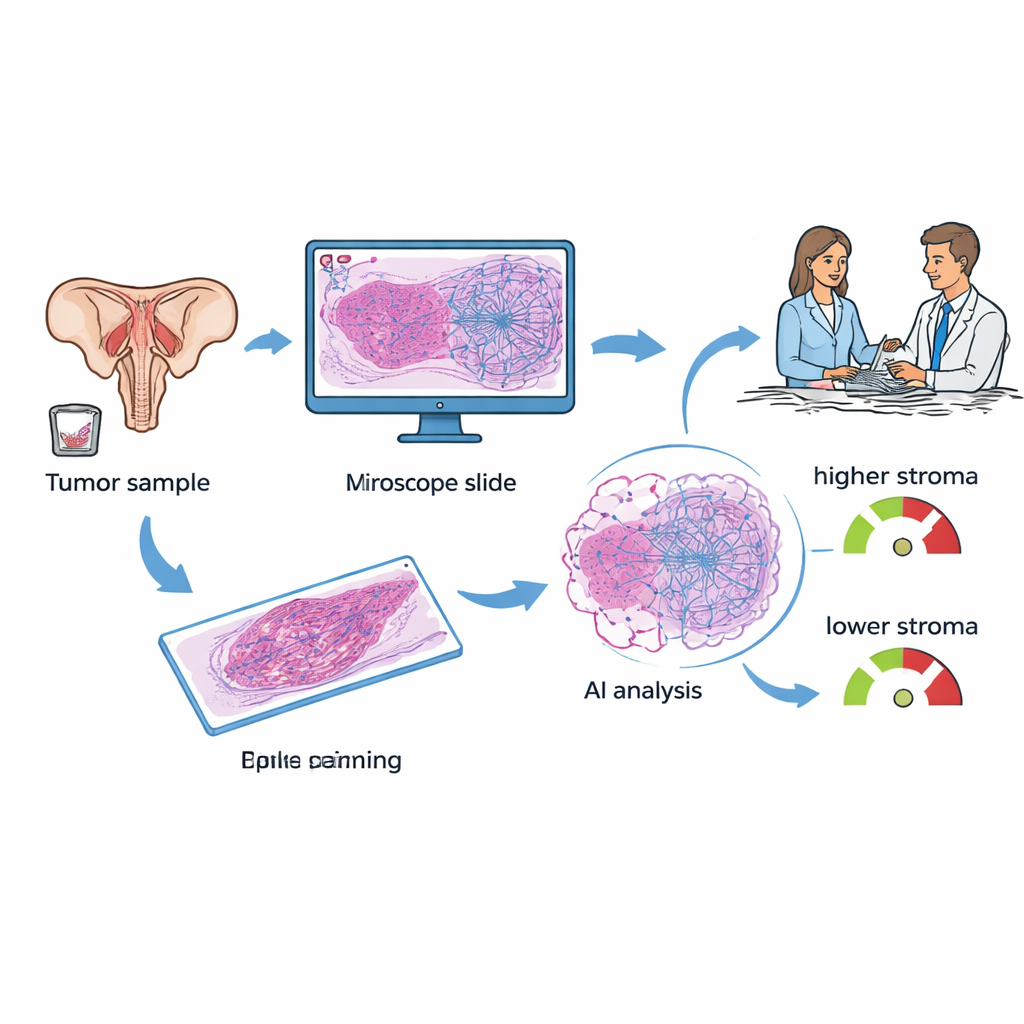
AIによる組織解析と血液ベースのスコアの比較
今日、卵巣がんで広く注目されているツールの一つがKELIMです。これは化学療法開始後最初の100日間に血中マーカーCA‑125がどれだけ速く低下するかに基づくスコアです。KELIMは費用対効果が高く有用ですが、算出には数週間の治療後の測定が必要で、すべての患者が十分な早期採血を受けているわけではありません。研究者たちは組織スライドと少なくとも3回のCA‑125測定を有する単一のがんセンターで治療を受けた89人の女性のデータを収集しました。各患者についてKELIMを算出し、病理医がスライド上の腫瘍領域にラベルを付けた後、AIモデルにTSPを推定させ、各症例を「ストローマ低(間質<50%)」または「ストローマ高(間質≥50%)」と分類しました。
AIは専門家に一致し、高リスク腫瘍を示す
AIの判定は経験豊富な病理医の評価と高度に一致しました:自動化されたTSP分類は94%の症例で手動分類と一致しており、卓越した一致度と見なされます。患者の転帰を解析すると、AIでストローマ高と判定された腫瘍を有する女性は、ストローマ低の患者に比べ全体生存が有意に短いことが分かりました。統計的には、高いTSPは追跡期間中の死亡リスクをほぼ2倍にし、この効果はKELIMスコアを考慮に入れても持続しました。対照的に、この実臨床コホートではKELIMは白金薬に対する耐性と関連していましたが、患者の生存期間と明確に結びつくとは言えませんでした。
治療判断にとっての意味
TSPは診断時に採取される日常的なスライドから測定できるため、AIベースのTSPは化学療法開始前、場合によってはKELIMより数か月早くリスクを評価する手段を提供します。高TSPの結果は腫瘍がより攻撃的で治療が困難である可能性を臨床医に示唆し、より厳重なモニタリング、追加治療の早期検討、あるいは異なる手術戦略の検討を促すかもしれません。この方法は比較的低コストでもあります:新たな検査ではなく既存の病理画像とソフトウェアモデルに依拠するからです。著者らは、自動化されたTSPが遺伝子検査やCA‑125の経時変化など他のマーカーと併用することで、患者や病理部門に大きな負担をかけることなく予後予測を洗練できると主張しています。
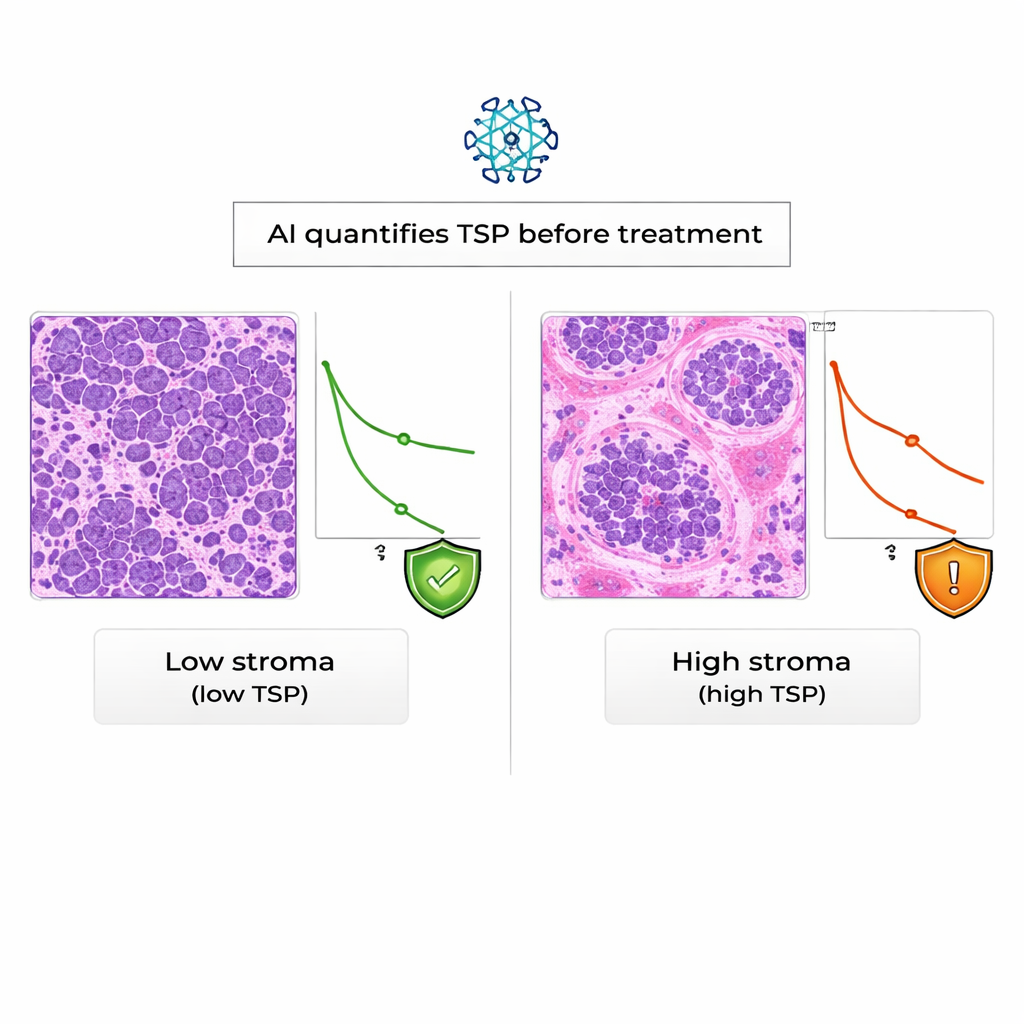
今後の展望:患者にとってより賢く早い指針へ
一般読者向けの主なメッセージは、すべての卵巣がんが同じではなく、腫瘍を取り巻く支持組織が疾患の振る舞いについて重要な手がかりを含んでいるという点です。本研究は、AIが標準的な生検スライド上でその手がかりを信頼性をもって読み取れること、そして間質が多い腫瘍は既存の血液ベースのスコアとは独立して生存率が低い傾向があることを示しています。日常診療に組み込むにはより大規模で多様な研究が必要ですが、AI由来のTSPは早期警告として有望であり、治療計画の個別化や患者への初期の期待値の明確化に役立つ可能性があります。
引用: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
キーワード: 卵巣がん, 人工知能, 腫瘍微小環境, 予後バイオマーカー, デジタル病理学