Clear Sky Science · ja
線維芽細胞増殖抑制とNupr1bを介したFbln2軸による心外膜活性の低下と筋線維芽細胞の減少がゼブラフィッシュの心臓再生を促進する
なぜある心臓は自らを癒せるのか
心筋梗塞が起こると、損傷した筋肉は通常、硬い瘢痕で覆われてしまい完全には元に戻りません。小さな縞模様の観賞魚であるゼブラフィッシュは驚くべきことを行います。心臓組織を再生し、最終的にはほとんどの瘢痕を取り除いてしまうのです。本研究は一見単純だが医学的に重大な疑問を投げかけます。癒えている心臓は、いつ瘢痕を作るべきか、いつそれを除去して新しい筋肉を育てるべきかをどのように判断しているのか。ゼブラフィッシュにおけるこのバランスを解読することは、将来負傷したヒトの心臓が破綻するのではなく自ら修復する手助けになる戦略を示唆します。
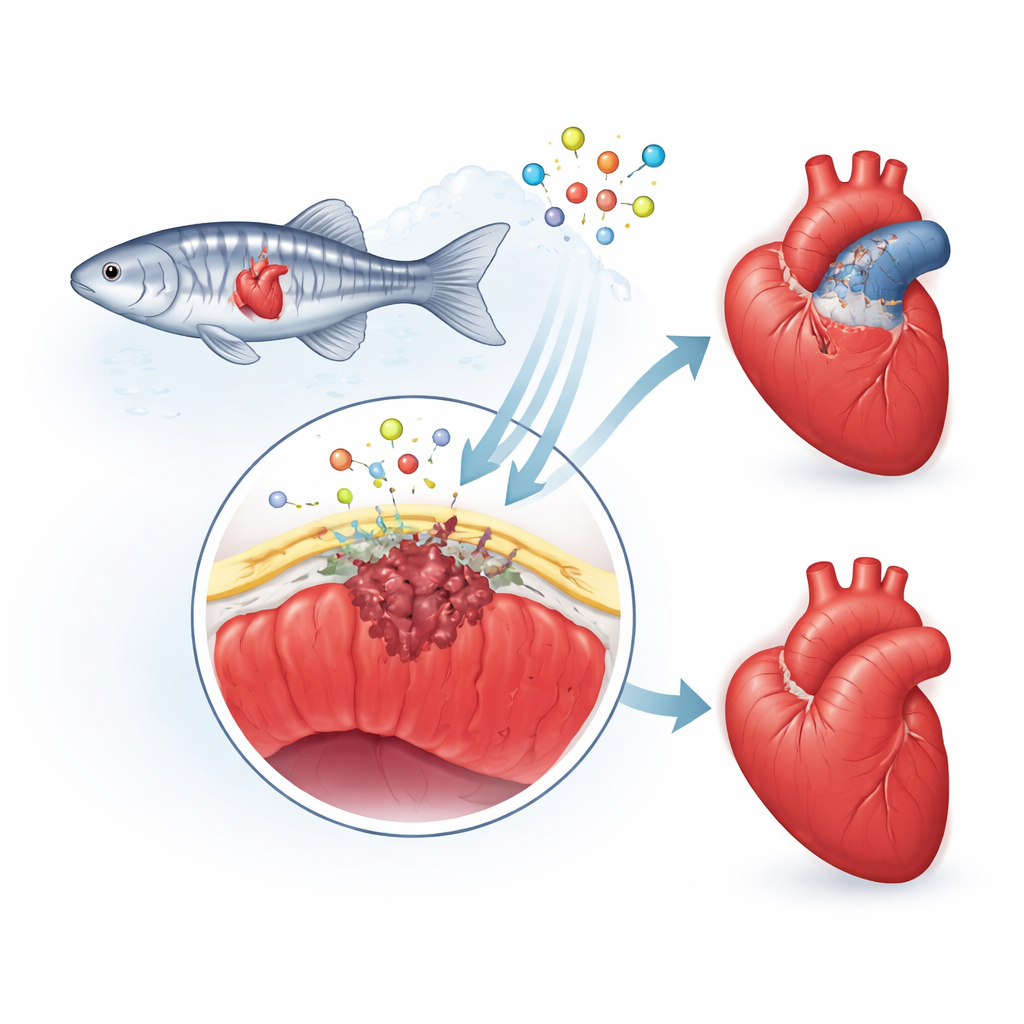
心臓を覆う保護の外皮
研究者たちは心臓を覆う薄い“皮膚”である心外膜(エピカルディウム)に着目しました。損傷後、この層は活性化し、その細胞はアイデンティティを変え、一部は損傷部位に侵入します。そこでこれらの細胞は支持細胞や瘢痕形成細胞になり、新しい血管や心筋の成長を導く化学シグナルを放出します。ヒトではこの修復応答が行き過ぎてしまい、厚く永続する瘢痕を残しがちです。対照的にゼブラフィッシュでは瘢痕は一時的で、健康な筋組織が戻るにつれて徐々に分解されます。チームは、心臓を取り巻く足場(マトリックス)に存在する線維タンパク質フィブリン‑2(Fbln2)が、この心外膜の応答の速度と強度を決めるのに寄与しているのではないかと考えました。
瘢痕化にかかる分子的ディマー(調節)スイッチ
ゼブラフィッシュで遺伝子編集を用い、Fbln2の量を変えた2種類の系統を作製しました:Fbln2が減少した系統と、タンパク質が完全に欠失した系統です。凍結プローブで魚の心臓に損傷を与え(心筋梗塞を模倣)、数週間から数か月にわたって治癒を追跡しました。Fbln2の量が下がると、初期の心筋や血管内皮の細胞分裂は減少しましたが、形成された線維性瘢痕は小さく、より容易に再編成されました。3か月後には、これらの心臓はよく再生し、主要な瘢痕材料であるコラーゲンはほとんど残りませんでした。一方、Fbln2を完全に欠く魚では、成長と瘢痕形成に関わる重要な経路(TGFβファミリーに関連するシグナル)の強い抑制が起こり、心外膜直下の瘢痕形成細胞がはるかに少なくなりました。初期の瘢痕は小さかったものの、その後これらの心臓はコラーゲンを除去できず、大きく永続する瘢痕と再生不全に終わりました。
心外膜の状態変化を拡大して見る
心外膜細胞が単一細胞レベルでどのように振る舞っているかを調べるため、チームは損傷直後に単一細胞RNAシーケンシングを用いました。静止した細胞、新たに活性化した細胞、低酸素に適応するストレス状態の細胞、活発に分裂している細胞など、いくつかの心外膜細胞の「状態」を同定しました。正常なFbln2を持つ魚では、心外膜細胞は静止→活性化→成熟の順に滑らかに進行しました。Fbln2が減少または欠失している魚では、この進行が停滞しました:細胞は早期段階に留まり、より成熟した活性化群は不足しており、特に完全欠失の個体で顕著でした。心外膜の活性化時やTGFβシグナル応答で通常オンになる複数の遺伝子の発現が抑えられており、Fbln2が瘢痕形成と再編成へのコミットの強さを決めるこの経路の調節因子であることを示しています。
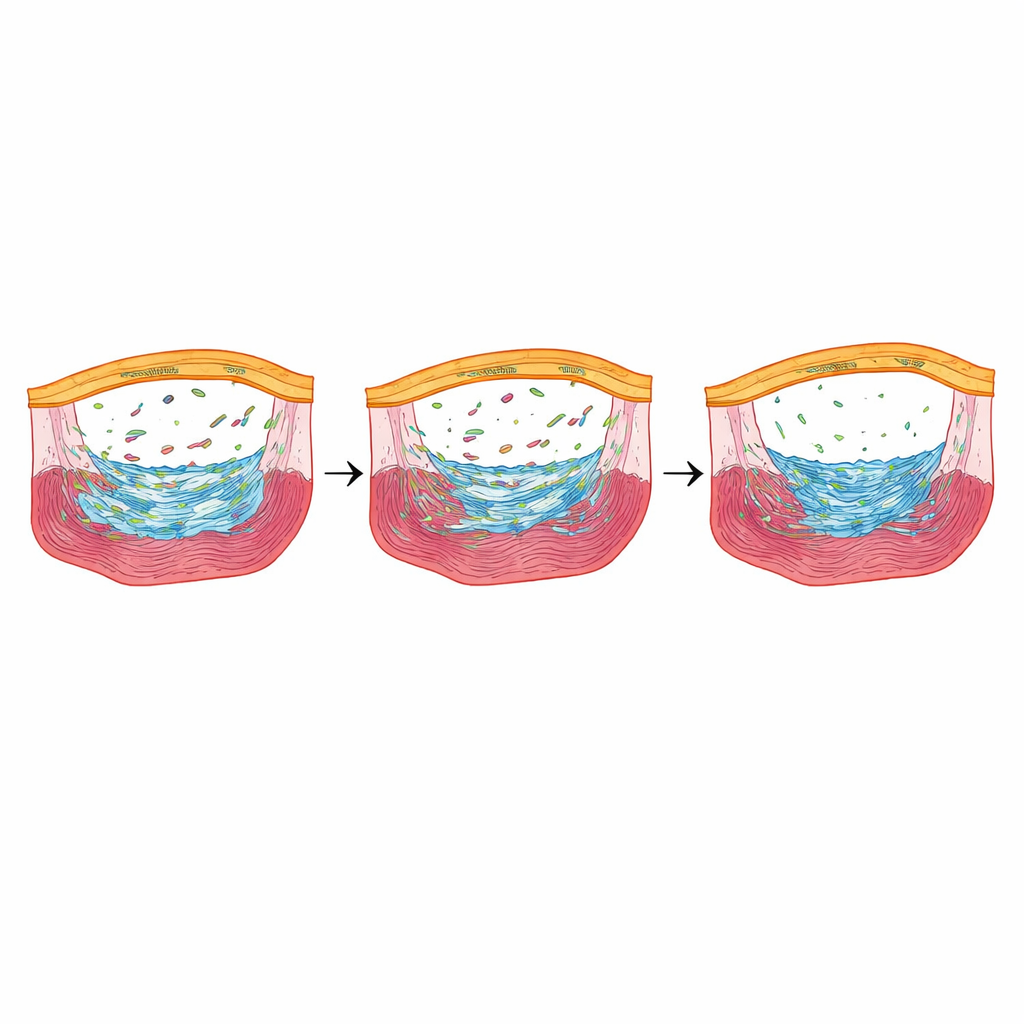
修復を微調整するストレス応答因子
Fbln2が低下したときに最も鋭く減少した遺伝子の一つが際立っていました:nupr1b。これは初期治癒期の心外膜細胞で活性化するストレス応答性の調節因子です。研究者たちがnupr1bを欠損させると、ゼブラフィッシュは心外膜由来の瘢痕形成細胞が減少し、心筋細胞の分裂も低下し、損傷後数か月経っても大量のコラーゲンが残存しました。これはFbln2を完全に欠く魚とよく似ていました。注目すべきは、Fbln2が減少した魚の心外膜細胞限定で短期間だけnupr1bを再活性化すると、瘢痕形成細胞の数と心筋細胞の増殖が回復し、後期の瘢痕化が増加したことです。TGFβ受容体を化学的に阻害するとnupr1bのレベルが低下し、nupr1bがFbln2–TGFβシグナル軸の下流に位置することが示されました。
ヒトの心臓治癒にとっての意味
これらの発見は、ゼブラフィッシュの心臓が過剰な線維化と不十分な線維化の間の綱渡りを行うのを助ける「心外膜Fbln2–Nupr1b軸」を明らかにします。この軸をわずかに下げると初期の瘢痕の爆発的発生が抑えられ、効率的な瘢痕除去が促されますが、完全に遮断すると再生が破綻して硬い瘢痕が残ります。ヒト医療への教訓は、瘢痕を全面的に阻止するのではなく、それを調節することが目標であるという点です。破裂を防ぐための十分な構造は保ちつつ、瘢痕組織が一時的で健康な筋に置き換わるようにすることが重要です。ゼブラフィッシュのこの制御システムを理解し最終的に利用できるようになれば、負傷したヒトの心臓を慢性線維化ではなく真の再生へと導く将来の治療法に示唆を与える可能性があります。
引用: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
キーワード: 心臓再生, 線維化, ゼブラフィッシュ, 心外膜, TGF-βシグナル伝達