Clear Sky Science · ja
潜在性TGF-β1活性化の選択的阻害は安全性を保ちながら組織線維化を抑制する
目に見えない瘢痕が重要な理由
多くの慢性疾患は、線維化と呼ばれる過程で硬い瘢痕組織を静かに蓄積し、臓器を徐々に損ないます。この瘢痕化は肝臓、腎臓、肺、そして腫瘍の周囲に至るまで正常な機能を阻害し、腫瘍周囲では最新のがん免疫療法の効果を鈍らせることもあります。タンパク質TGF-β1はこの瘢痕化の中心に位置しますが、体内のあらゆる場所でそれを遮断することは危険であることが示されてきました。本研究はSOF10と呼ばれる新しい抗体を記述しており、有害なTGF-β1の活性化だけを選択的に阻害してその必須機能を保つことを目的としており、肝疾患、腎不全、がんの動物モデルで有望な効果を示しています。
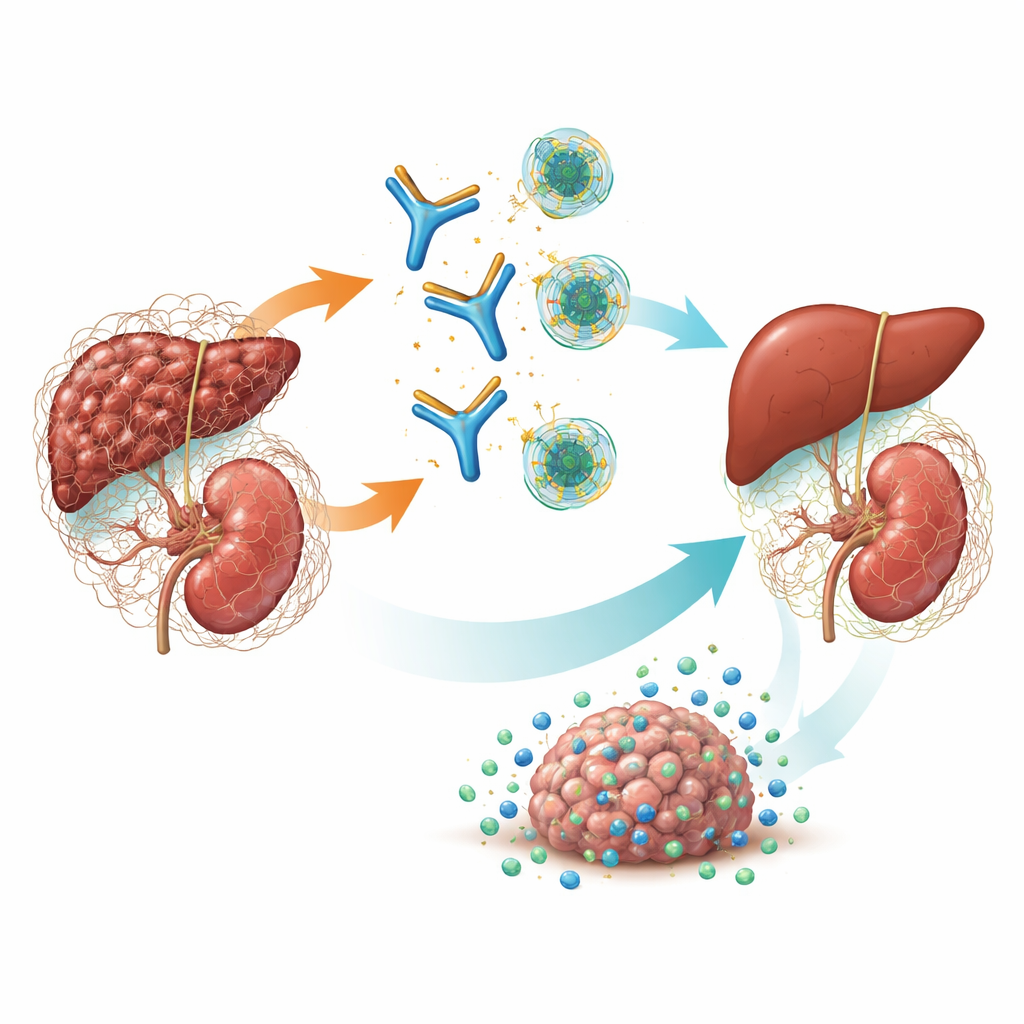
瘢痕化とがんのためのマスター・スイッチ
TGF-βは細胞の増殖、修復、免疫系との相互作用を制御する強力なシグナル分子です。慢性疾患では、その一つのアイソフォームであるTGF-β1が線維芽細胞を駆動して過剰な結合組織を構築させ、臓器の硬化と機能不全を引き起こします。また、腫瘍周囲に免疫抑制的で線維化した殻を作り、免疫細胞や薬剤ががん細胞に到達するのを妨げます。これまでの薬剤は3つのTGF-β形態すべてを同時に遮断しようとしましたが、この「パンブロッケード」は心臓弁障害、出血、皮膚腫瘍など深刻な副作用を引き起こしました。遺伝学的研究や既存モデルは、腎線維症や多くの固形腫瘍における主犯がTGF-β1であることを示唆しており、このアイソフォームだけを慎重に標的にすることで有効かつ安全性の高い治療が可能になるという可能性が示されました。
TGF-β1を不活性状態に固定する
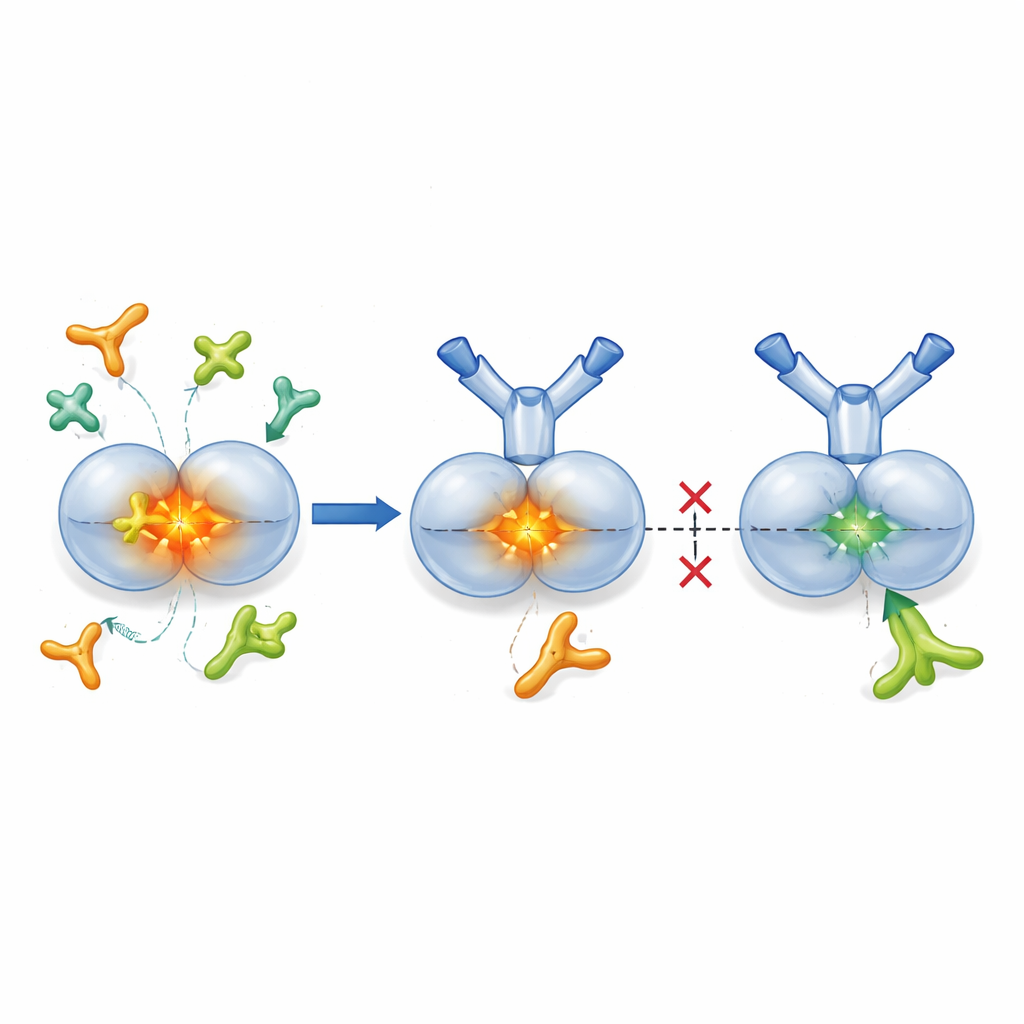
TGF-β1は通常「潜在」パッケージとして産生され、活性のコアはパートナータンパク質に包まれて必要になるまでオフの状態に保たれます。プロテアーゼと呼ばれる酵素や、インテグリンとして知られる細胞表面の接着タンパク質がこのパッケージを開き、活性TGF-β1を周辺組織に放出します。研究者らはSOF10を設計し、活性ホルモンや他のアイソフォームではなく、潜在性TGF-β1にのみ結合するヒト化抗体としました。X線結晶構造解析による構造研究は、SOF10が潜在複合体の二つの半分の間の界面に楔(くさび)のように入り込み、クランプのように安定化することを示しました。in vitroの試験では、これによりプロテアーゼと一つのインテグリン(αvβ8)による活性化が妨げられましたが、健常組織の免疫バランスを維持する上で重要な別のインテグリン(αvβ6)は概ね影響を受けませんでした。実質的に、SOF10は有害な活性化経路だけを選択的に沈黙させ、主要な恒常性経路を温存します。
肝臓と腎臓を徐々の損傷から保護する
このTGF-β1への選択的なクランプが実際に瘢痕化を抑えられるかを検証するため、研究チームは複数のマウスモデルでSOF10を試験しました。急速な食事誘発性脂肪肝モデル(肝線維化へ進行)では、SOF10治療によりTGF-β応答遺伝子やコラーゲン合成遺伝子の肝内発現が低下し、蓄積した瘢痕組織の化学マーカーであるヒドロキシプロリンも減少しました。二つの異なる腎モデル――間質線維化を駆動する外科的閉塞モデルと、糸球体の瘢痕化と腎不全を発症する遺伝性アルポート症モデル――においても、SOF10は線維化遺伝子活性を抑え、コラーゲン含量を減らし、顕微鏡下で瘢痕化領域を目に見えて縮小させました。慢性アルポートモデルでは血液検査で腎機能の改善が示され、これらの利益は他のTGF-βアイソフォームも阻害するより広域のTGF-β遮断抗体と同等でありながら、他のアイソフォームを遮断していませんでした。
腫瘍内の免疫系を解放する
腫瘍周囲の線維化組織は物理的な障壁であり免疫のブレーキとして働くため、研究者らはSOF10がチェックポイント阻害薬の反応を改善できるかを尋ねました。通常は抗PD-L1療法に弱いマウスの乳がんおよび結腸がんモデルで、SOF10を併用すると腫瘍増殖が有意に遅延しました。SOF10単独あるいは抗PD-L1単独ではほとんど効果が見られませんでした。併用治療を受けた動物の腫瘍にはより多くのキラーCD8陽性T細胞とそれらががん細胞を破壊するために用いる毒性酵素が増加していました。これらの腫瘍から採取した線維芽細胞は、コラーゲンやマトリックス構築経路の活性が低下する一方で、インターフェロンや抗原提示経路の活性が上昇しており、より免疫を支援する間質へとシフトしていました。これらの変化は広域TGF-β遮断で見られたものとよく一致しており、潜在性TGF-β1単独を標的にするだけで腫瘍環境を同様に再プログラムできることを示唆します。
動物での安全性シグナル
TGF-βを広く阻害しようとする以前の試みが安全性の問題に直面したため、チームはマウスとコニモンキーで13週の毒性試験を実施し、SOF10を反復高用量で投与しました。薬物は血中で典型的な抗体の挙動を示し、広範な用量範囲で主要臓器、血球数、心肺機能に損傷の兆候は見られませんでした。マウスでは2週間ごとに最大200 mg/kg、サルでは100 mg/kgまでの最高用量が有害影響未観察レベルに指定されました。この安全性プロファイルは、TGF-β2、TGF-β3、そしてαvβ6を介した活性化を温存することで、従来の選択性の低いアプローチで見られたリスクを低減できるという考えを支持します。
患者にもたらす可能性
総じて、TGF-βシグナルを全て消し去るのではなくTGF-β1を不活性な殻に固定することで、複数の臓器の瘢痕化を緩和し、腎機能を改善し、抵抗性の高い腫瘍を免疫療法に対して脆弱にできる可能性が示され、動物試験においては有望な安全性が示されました。これらの利益を確認し長期的な影響を監視するためにはヒト試験が必要ですが、SOF10や同様の戦略は慢性線維疾患や特定のがんを治療する新しい道を開き、治癒や免疫バランスに必要な役割を保ちながら有害な瘢痕化だけを抑える可能性があります。
引用: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
キーワード: 線維症, TGF-β1, モノクローナル抗体, 腎臓および肝疾患, がん免疫療法