Clear Sky Science · ja
血漿タンパク質の構造的署名がアルツハイマー病の状態を分類する
なぜ記憶障害の血液検査が重要か
アルツハイマー病は記憶障害が明らかになるずっと前から進行していることが多いが、早期発見のための現在の検査は侵襲的だったり高価だったり、利用が難しいことがある。本研究は別の発想を試している:血流中を巡るタンパク質の三次元的な形のごく小さな変化が、健康な加齢から軽度の記憶障害(MCI)、そしてアルツハイマー病へと至る過程のどこにいるかを示せるかどうかだ。うまくいけば、そのような血液検査はスクリーニングを簡便にし、より早期の治療を支え、新しい治療法の効果を追跡する研究にも役立つ可能性がある。
量ではなくタンパク質の形に着目する
ほとんどの血液検査は特定の分子がどれだけあるかを測る。ここで研究者たちはタンパク質の形に着目した。細胞内にはタンパク質を適切に折りたたむための品質管理システムがあり、このシステムが加齢とともに弱ると、誤って折りたたまれたタンパク質が蓄積して脳細胞にダメージを与えることがある。研究チームは、この「タンパク質の家事」機能の崩壊が血中タンパク質に構造的な指紋を残すかどうかを疑問に思った。認知的に健常、MCI、アルツハイマー病のいずれかに分類される520人のボランティアから採血し、共有結合を利用したタンパク質プロファイリングという化学手法でタンパク質の露出部位にタグを付けた。露出が大きい部位ほどタグが付けられやすく、これによりタンパク質の量にほとんど依存しない形状の数値化が可能になる。
血液中の構造的指紋を見つける
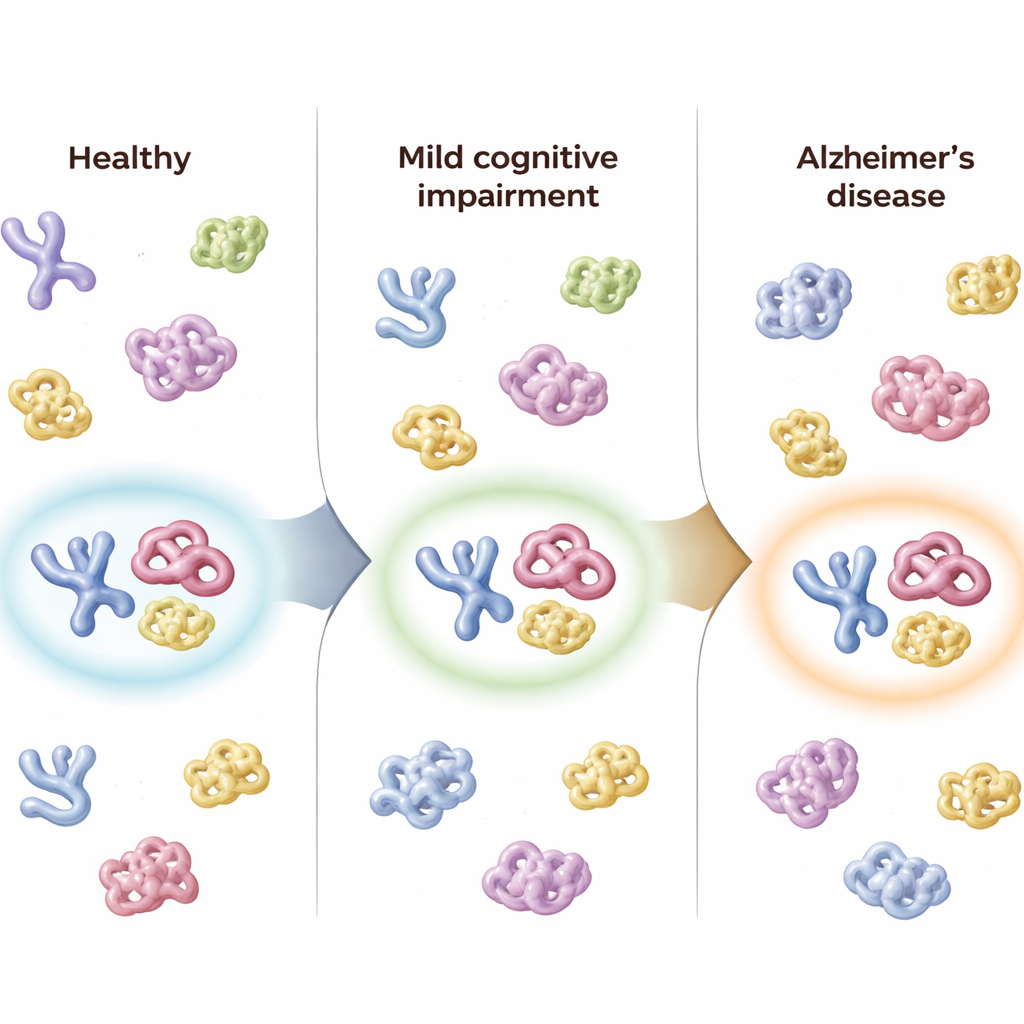
約900に近いタグ付きタンパク質断片にわたり、研究者たちは微妙だが一貫した傾向を観察した:健康からMCI、アルツハイマーへ移行するにつれて、特定のタンパク質表面がより露出が減り、個人間でのばらつきが増えていた。このパターンは、疾患進行に伴いタンパク質折りたたみの制御が悪化するという考えと一致する。チームはまた、アルツハイマー病の主要な遺伝的危険因子であるAPOE ε4変異がタンパク質の構造にどのように影響するかも調べた。ε4を2コピー持つ人々では、APOEタンパク質と相互作用するいくつかのタンパク質に特徴的な構造変化が見られ、このリスク遺伝子はどのタンパク質が存在するかだけでなく、それらがどのように折りたたまれ配置されるかにも影響することを示唆した。
血中タンパク質と気分・行動の関連
アルツハイマー病は記憶以外にも広範な影響を及ぼす。興奮、抑うつ、幻覚などの症状は一般的で、男女間で異なることも多い。研究者たちは12種類の神経精神症状の臨床評価をタンパク質形状の測定値と組み合わせた。男女ともに、症状が悪化するほどタンパク質がより構造的に「閉じた」状態になる傾向があった。クラスタリンやアミロイド蓄積に関連する複数のタンパク質は男女ともに症状の重症度と同様の軌跡を示したが、他のタンパク質は性別特有のパターンを示した。これらの発見は、血中タンパク質の構造が疾患の存在だけでなく、行動や気分としてどのように現れるかも反映している可能性を示唆する。
病期を分類する三つのタンパク質パネル
これらの複雑な測定値を臨床で役立つ形に変えるために、チームは構造データを18種類の機械学習手法に入力した。最良の性能を示したモデルはディープラーニングに基づき、C1QA、クラスタリン(CLUSとも呼ばれる)、アポリポタンパク質B(ApoB)から得られるわずか三つのタンパク質断片に依存していた。この三断片の構造的読み出しのみを用いて、モデルは独立したテストセットで個人を健常、MCI、アルツハイマーのグループに約83%の精度で正しく分類した。健康とMCI、あるいはMCIとアルツハイマーのような二択の問いにすると、パネルの性能はさらに高まり、構造ではなくタンパク質量に焦点を当てた現在の多くの血液ベース手法と同等かそれ以上の精度を示した。
経時的追跡
研究者たちはまた、約8か月までの追跡サンプルを50人の参加者から得ていた。診断が悪化した人々(例えば健常からMCIへ、MCIからアルツハイマーへ)では、三つのタンパク質パネルの合成スコアが同じ方向に変化し、疾患の進行を反映した。対照的に臨床状態が変わらなかった個人ではパネルスコアにほとんど変化が見られなかった。パネルの全体的な「アルツハイマー信頼度」スコアは、標準的な認知検査、日常機能の評価、MRIで見られる脳萎縮、アミロイドやタウの確立された髄液マーカーと密接に一致しており、血中の構造シグナルが基礎にある脳の変化を反映していることを示唆している。
患者にとっての意義
総じて、この研究は、ごく少数の豊富に存在する血中タンパク質の形状が小さく協調的に変化するだけで、個人が認知的に健常か軽度障害かアルツハイマー病かを信頼性をもって示せることを示している。検査が髄液や脳画像ではなく血液を用いるため、理論的には日常的なスクリーニングや臨床試験の参加者選別・モニタリングに拡張可能である。著者らは、より大規模で長期にわたる研究が必要であり、用いる化学手法はまだ専門的であると注意を促している。それでも、結果はタンパク質の量だけでなく構造が、アルツハイマー病のより早期かつ精確な検出と追跡のための有望な新しい情報源であることを示している。
引用: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
キーワード: アルツハイマー病 バイオマーカー, 認知症の血液検査, タンパク質の折りたたみ変化, 機械学習による診断, クラスタリンとC1QA