Clear Sky Science · ja
局所性認識モーダル整合を備えた条件付き拡散による多様なタンパク質立体配座アンサンブルの生成
なぜタンパク質の運動が重要か
細胞内のタンパク質は頑丈な彫刻のようなものではなく、常に形を変える小さな柔軟な機械のように振る舞います。これらの形の変化は酵素の触媒作用や受容体の薬物応答、細胞内のシグナル伝達を制御します。しかし一般に目にするタンパク質の図は一つの「スナップショット」構造しか示さず、実際に存在する豊かな構造アンサンブルを見落としがちです。本論文はMac-Diffという人工知能手法を紹介します。これは与えられたタンパク質について、多数の現実的な形状を高速に生成でき、タンパク質がどのように呼吸し動くかを一枚絵以上に示す助けになります。
単一スナップショットから動的アンサンブルへ
何十年にもわたり、研究者はタンパク質の運動を探るために手間のかかる実験や長時間の分子動力学シミュレーションに頼ってきましたが、これらは時間と費用がかかります。AlphaFold2のような画期的なツールはアミノ酸配列からタンパク質のもっともありそうな3次元構造を予測しますが、通常は一つか数個の優勢な形状を返します。とくにシグナル伝達やアロステリック調節に関わる多くのタンパク質は、複数のゆるやかな状態を自然にとります。著者らは、こうしたタンパク質の機能を理解し、より目立たない一過性の形に結合する薬を設計するには、単一の最良推定だけでなく、妥当な立体配座の全集合を生成する方法が必要だと主張します。
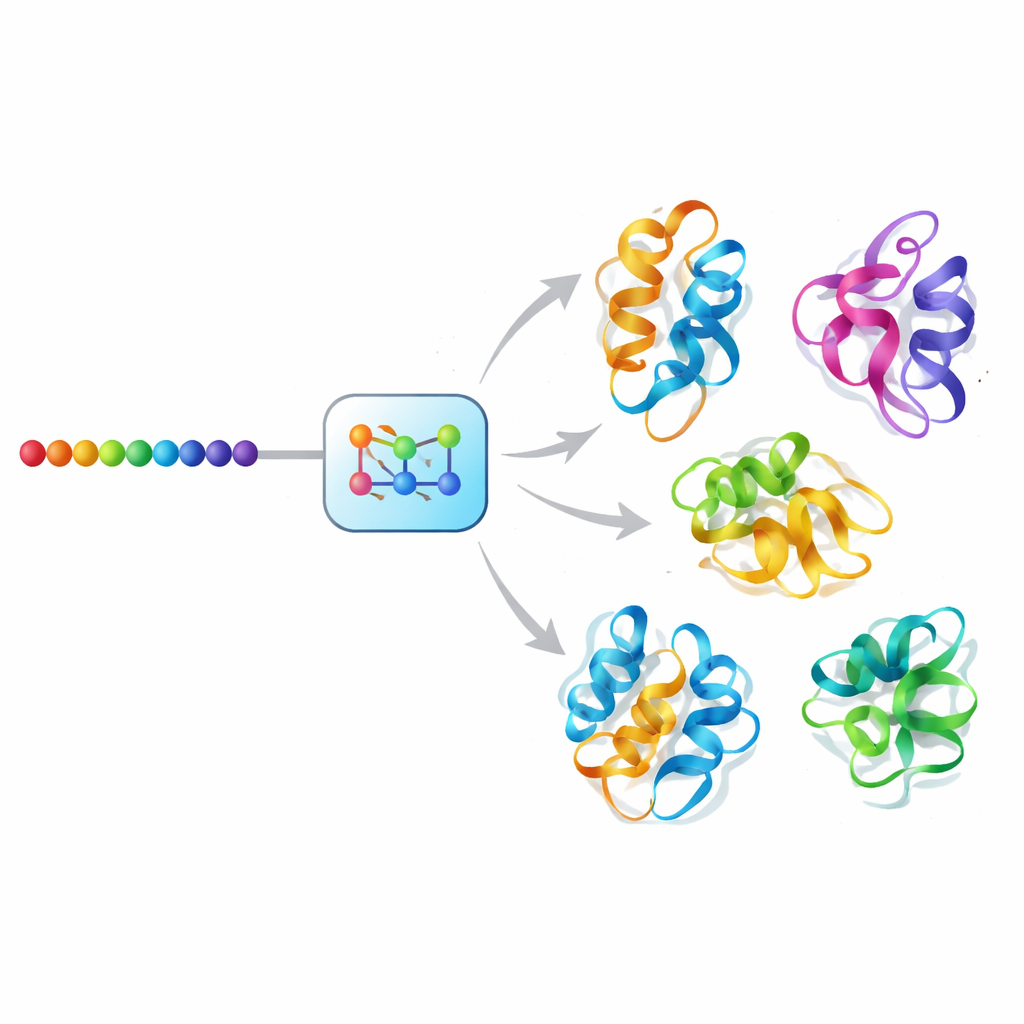
タンパク質運動へのAI「拡散」アプローチ
Mac-Diffは拡散型生成モデルというクラスのAIを用いてこの課題に取り組みます。この手法は画像合成の分野で最近の飛躍を支えてきました。Mac-Diffは写真のノイズ除去の代わりに、タンパク質バックボーンの抽象的な幾何学的記述のノイズ除去を行います。モデルはタンパク質を残基間の距離や角度といった、分子全体の回転や並進に不変な対関係のグリッドとして表現します。順方向ステップではこれらの幾何学パターンに段階的にノイズを加え、ランダムな静的ノイズのようにします。逆方向ではアミノ酸配列に導かれながら段階的にノイズを除去することを学び、整合する3次元幾何が再出現します。得られた幾何情報は標準的な構造構築ソフトウェアによって完全な原子モデルに変換できます。
配列と構造を局所的に結びつける
重要な革新は、線形の残基配列とその3次元近傍との結びつけ方にあります。テキストから画像へ変換するモデルのように、すべての残基がすべての他の残基に注意を向けるだけでは、重要な物理的制約がぼやけてしまいます。そこで著者らは各残基が小さな、ありそうな相互作用パートナーの近傍に注目する「局所性認識」注意機構を導入します。これらの近傍を推定するために、Mac-Diffは三つの要素を使います:各残基の生化学的文脈を符号化するタンパク質言語モデルESM-2、どの残基対が近接しやすいかを示すコンタクトマップのヒント、そして鎖に沿って近い残基を優先する単純な規則です。これらの信号を組み合わせることで、ノイズ除去中にモデルは物理的にもっともらしいパートナーからの情報を優先的に使い、現実的で柔軟な構造を再構築する能力を研ぎ澄まします。
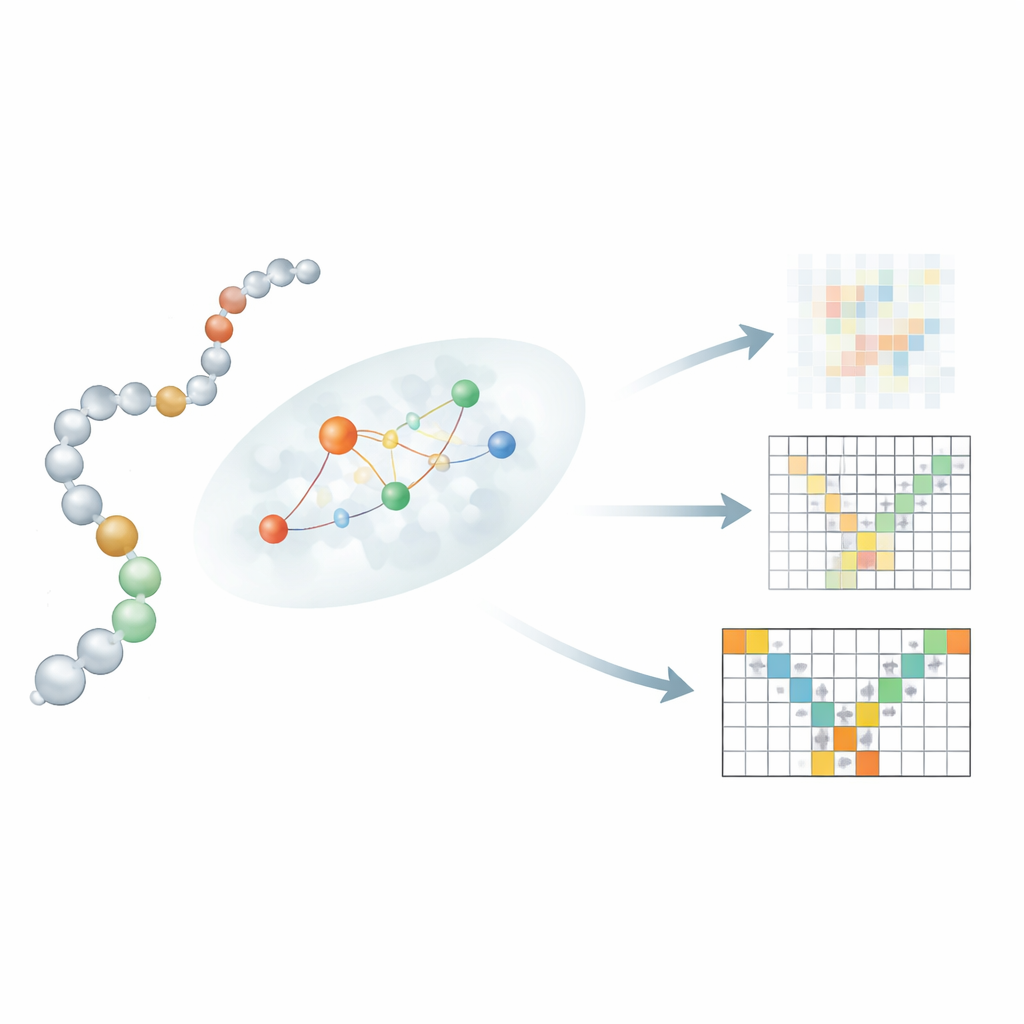
長時間シミュレーションと形状変化するタンパク質に対する検証
研究者らはMac-Diffを二つの厳しい側面で評価しました。まず高速折りたたみタンパク質や古典的ベンチマークであるBPTIの長時間にわたる精密な分子動力学シミュレーションで観察される広い形状分布を再現できるかを問いました。タンパク質内部の距離分布や全体のコンパクトさといった、生成したアンサンブルとシミュレーションデータの統計的性質を比較する複数の指標において、Mac-Diffは競合するAI手法と同等以上の成績を示し、かつより多様な配座を生成しました。シミュレーションで同定された主要な“準安定”状態の多くを捉え、残基レベルの柔軟性パターンも高い相関で再現しており、そのアンサンブルがグローバルな折り畳みと局所的な揺らぎの両方を現実的に反映していることを示しています。
隠れた機能状態の顕在化
次にチームは、仕事をする過程で非常に異なる形をとることが知られているタンパク質群に対してMac-Diffを試しました。例として、エネルギー代謝中に開閉を切り替えるアデニレートキナーゼや、それぞれ実験的に決定された二つの立体配座を持つ40個の厳選タンパク質セットが含まれます。Mac-Diffはタンパク質ごとにわずか100の候補構造を生成しました—通常のシミュレーション軌道に比べてはるかに少ない数ですが—それでも既知の状態の大部分を良好な幾何学的一致で回復しました。たとえばアデニレートキナーゼでは、開いた構造と閉じた構造の両方を結晶構造に高い類似性で生成しました。一方で複数の一般的な手法は一つの状態を優先する傾向がありました。さらにこのモデルは同等のハードウェアで従来のシミュレーションより約千倍高速に動作し、形状の多様性を系統的に探索することを現実的にしています。
生物学と医療にとっての意義
平たく言えば、Mac-Diffはタンパク質の配列から一枚の肖像画ではなく妥当な姿勢のギャラリーを生成し、どの部分が3次元で近づいたり握ったりしやすいかを考慮します。これらのアンサンブルを正確かつ効率的にサンプリングすることで、微妙な形の変化が機能の基盤となる様子を探る手段を提供し、まれだが重要な立体配座を見つけたり、一過性状態にのみ現れる薬物結合ポケットを探索したりできます。まだシミュレーションが提供する時間順の完全なムービーを再現するわけではありませんが、Mac-Diffは多くの系に対してタンパク質の動的ランドスケープを手の届くものにし、構造生物学、創薬、タンパク質設計に新たな洞察をもたらすことが期待されます。
引用: Wang, B., Wang, C., Chen, J. et al. Conditional diffusion with locality-aware modal alignment for generating diverse protein conformational ensembles. Nat Mach Intell 8, 415–434 (2026). https://doi.org/10.1038/s42256-026-01198-9
キーワード: タンパク質ダイナミクス, 拡散モデル, 立体配座アンサンブル, アロステリックタンパク質, 創薬