Clear Sky Science · ja
ラミンA/Cが制御するシステインの代謝フラックスはエピゲノム再プログラミングを通じて幹細胞運命を変える
細胞の骨格が代謝とどのように対話するか
なぜある細胞は若々しく多様な分化能を保つ一方で、他の細胞は老化したり誤った恒常性に固定されたりするのか?本研究は、DNAの形を作る核の“足場”と、硫黄を含む栄養素システインの間にある意外な対話を明らかにします。この対話が幹細胞を健康的な運命へ導くか、あるいは早期老化へ押しやるかを示すことで、細胞が「何を食べ」「どう代謝するか」を調整することで特定の遺伝病を防いだり、老化の側面を遅らせたりできる可能性を示唆しています。
核の殻の隠れた役割
細胞の奥深くで、DNAは核ラミナと呼ばれるタンパク質の網に押し付けられています。ラミンAおよびCと呼ばれるタンパク質がその一部を構成します。これらのラミンは核の形を保つだけでなく、どの遺伝子が不活性化されどれが利用可能であるかを決めるのに寄与します。著者らはマウス胚性幹細胞の最も柔軟な「ナイーブ」状態を調べ、ラミンA/Cが通常CBSとCTHという二つの代謝酵素を抑えており、これらはシステインの合成と分解を助けることを見出しました。ラミンA/Cが存在し活性であるとき、これらの酵素は抑制されシステインの処理は低く保たれ、安定した若々しい幹細胞状態が支持されます。 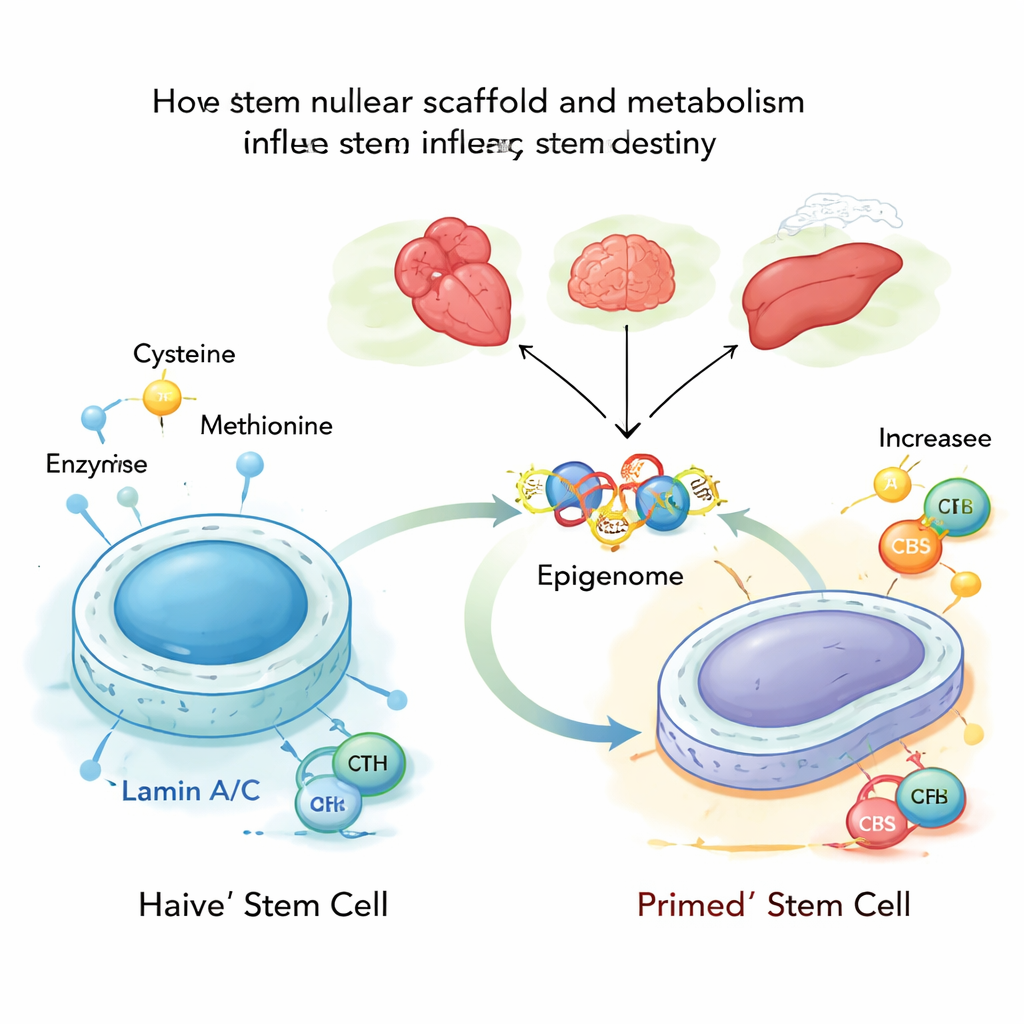
構造が崩れると代謝が加速する
次に、研究者たちはラミンA/Cを除去するか、ヒトの早老症であるハッチンソン=ギルフォード早老症を模倣する病的変異を導入しました。正常なラミンA/Cがないと、CBSとCTHの遺伝子はよりアクセス可能になり、転写因子SP1によって強く結合されて活性化されます。この変化はシステインをアセチルCoAへと終わる代謝経路へより多く流し、アセチル基を運ぶ小さな分子であるアセチルCoAが増えることでDNAの詰まりをゆるめるために用いられます。システインがより多くアセチルCoAへ送られると、アセチル基はヒストンタンパク質の特定部位、特にヒストンH3のK9とK27に優先的に付加され、近傍の遺伝子が発現しやすくなります。
化学的タグから細胞運命の決定へ
これらのヒストン「タグ」の変化は、細胞の制御パネル全体を再調整するように働きます。ナイーブな幹細胞では、CBSとCTHを増やすか単純にシステインを多く供給すると、細胞はより進んだ「プライムド」状態へと押し進められ、実際の組織を形成することに近づきます。心臓発生や他の系統に関与する遺伝子がより活性化され、DNAの三次元折りたたみもこれらのプログラムを支持する方向へ変わります。逆に、CBSやCTHの活性を下げたりシステインを制限したりすると、核ラミナが損なわれていてもよりナイーブで若々しい同一性を回復する助けになります。胚モデルでは、この代謝の誤配線により三胚葉―すべての器官の初期構成要素―の形成が偏り、CBSとCTHが是正されないと心筋細胞への偏りが生じました。 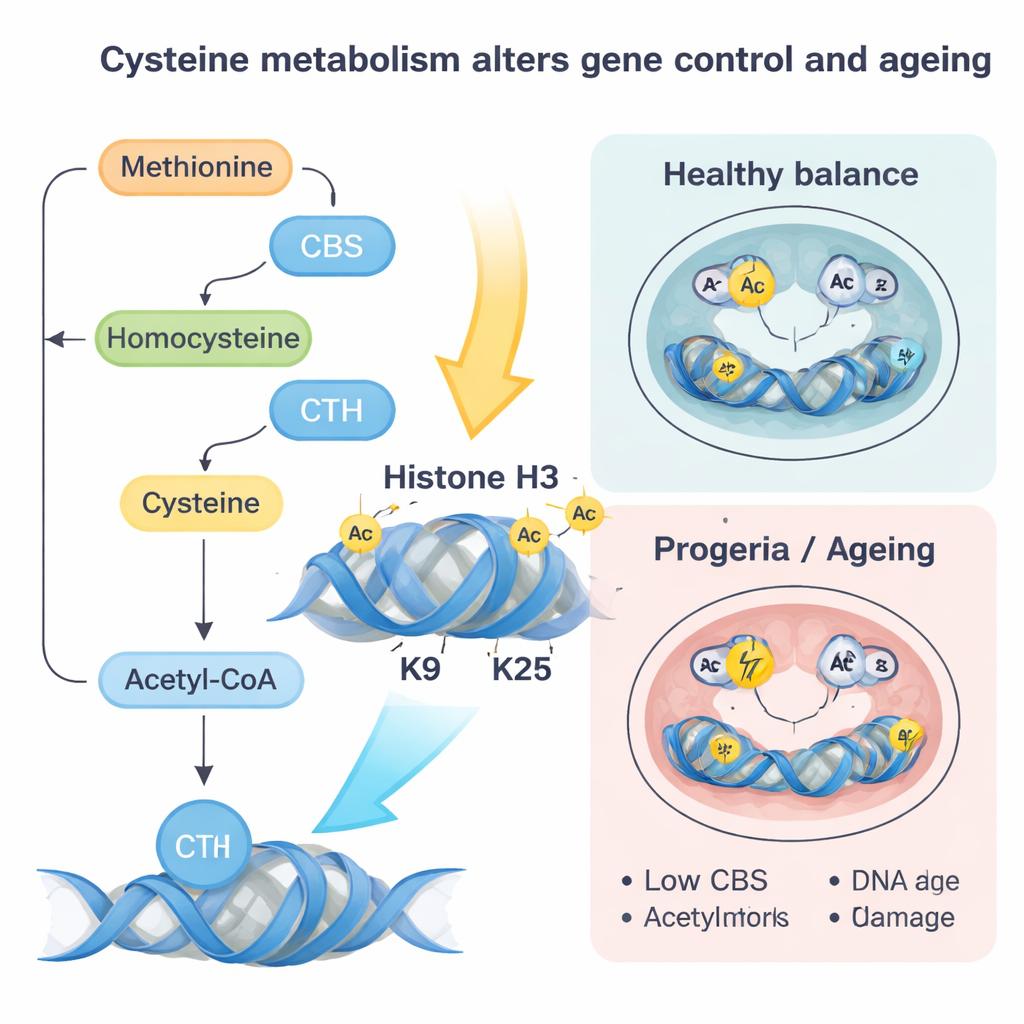
代謝、DNAの化学マークと早期老化
プロジェリア様のラミン変異は補完的な物語を語ります。この場合、CBSとCTHのレベルは低下し、システインフラックスとこの経路からのアセチルCoAが減少します。同時にホモシステインはメチオニン回路に戻され、SAM(メチル基の普遍的供与体)のレベルが上がります。これにより特にSUV39H1という酵素が付加するH3K9me3と呼ばれる余分なメチルマークが増え、クロマチンが凝縮してDNA修復の障害と結び付きます。著者らは、穏やかにCBSを回復させるかメチオニンを制限することでSAMを下げ、これらの抑制的メチルマークを減らし、DNA修復を改善し、酸化ストレスや老化マーカーを低下させ、心筋分化を部分的に救済できることを示しました。正常に老化したマウス心臓や高齢者やプロジェリア患者由来のヒト線維芽細胞でも類似のCBS低下と抑制的マークの上昇が観察され、この回路が自然な老化にも関与していることが示唆されます。
健康と老化にとっての意味
専門外の読者にとっての要点は、ラミンA/Cからなる核の構造的枠組みと代謝が密接に結びついているということです。ラミンでできた核の殻が乱れると、システインの使われ方が変わり、それがDNA包装タンパク質の化学的マークを書き換えます。これらのマークは幹細胞が体を作る際にどの遺伝子がオンになるかを決め、生涯にわたる細胞の損傷修復能にも影響します。CBSやCTHのような酵素を慎重に調整したり、メチオニンやシステインといった栄養素の供給を変えたりすることで、ラミンに基づく疾患での誤ったマーク付けを是正したり、早期あるいは正常な老化の側面を緩和したりする可能性がある、ということです。
引用: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
キーワード: 幹細胞, 核ラミナ, システイン代謝, エピジェネティクス, 老化