Clear Sky Science · ja
ABEL-FRETはA2Aアデノシン受容体の構造ダイナミクスを単一分子で測定する際の時間スケールのギャップを埋める
微小な細胞のスイッチをリアルタイムで観る
現在の多くの医薬品は、受容体と呼ばれる細胞表面の分子“スイッチ”を切り替えることで働きます。これらのスイッチは信号のオン・オフに伴って絶えず形を変えますが、ほとんどの計測手法は非常に速い動きか非常に遅い動きのどちらかしか捉えられません。本論文は、これまでよりずっと長時間、溶液中の単一の薬物標的受容体を観察する方法を示し、薬効に重要な特定の形に受容体が留まる様子を明らかにしています。
なぜこれらの形を変えるタンパク質が重要なのか
本研究はGタンパク質共役受容体(GPCR)という主要なクラスの細胞表面タンパク質に焦点を当てています。これらは視覚、気分、血圧、免疫応答など重要な生体プロセスを制御しており、承認済み医薬品の3分の1以上がGPCRを標的とします。よく研究された一例であるA2Aアデノシン受容体は、睡眠、疼痛、炎症、脳内シグナル伝達を調節し、パーキンソン病やがんなどの治療標的として有望です。GPCRは非常に柔軟で、異なる分子が結合すると受容体は特定のシグナル経路を好む異なる形に押し出されます。しかしこの柔軟性が、X線やクライオ電顕の静的スナップショットだけに基づく創薬を難しくしています。
受容体を固定せず単一分子を追跡する
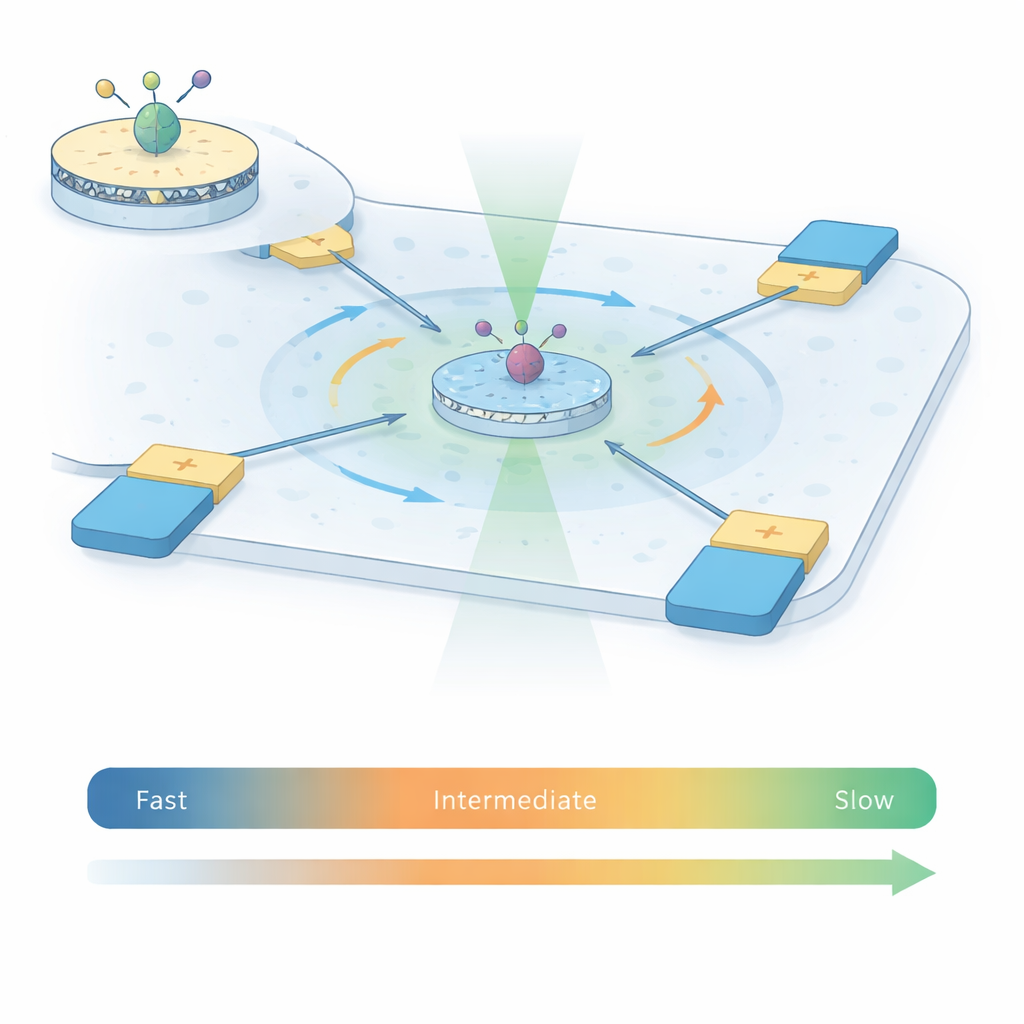
A2A受容体の動きをとらえるために、著者らは2つの強力な手法を組み合わせてABEL‑FRETと呼んでいます。まず単一受容体をナノディスクと呼ばれる人工膜の小さなパッチに再構成し、界面活性剤だけの場合よりも自然に近い環境を与えます。受容体の内側の2つの可動部位に蛍光色素を対で付け、受容体の形が変わるとこれら色素間の距離と相対配向が変化してエネルギー移動(フォスター共鳴エネルギー移動、FRET)が変わります。次に、受容体を表面に固定する代わりに、アンチブラウン電気泳動(Anti‑Brownian Electrokinetic、ABEL)トラップを用います。これは蛍光粒子の位置を検出し、電極で中心にやさしく戻すことでランダムなブラウン運動を打ち消すマイクロフルイディックチャンバーです。
欠けていた時間窓をつなぐ
従来の単一分子FRET実験では、自由拡散する受容体を数千分の一秒程度しか観察できないか、表面に固定した受容体を秒〜分単位で観察するかのいずれかでした。それぞれ異なる時間窓をカバーします。本研究ではABELトラップを用いることで、溶液中で自由にしておきながら個々のA2A受容体を1〜2秒にわたって観察し、拡散制限実験より約100倍長く保持できます。この延長された観察時間により、トラップ内での各バーストにおけるFRET信号のゆらぎや、リガンドなし、拮抗薬、2種類の作動薬という4つの条件にわたる多数の受容体の挙動を測定することが可能になります。分散、相関、再帰解析など信号解析から借用した統計ツールにより、ランダムな光子ノイズと実際の遅い構造変化を区別できます。
長時間持続する隠れた形が明らかに
FRETの読み出しは、受容体が複数の異なる立体配座を占め、通常の数百ミリ秒の観察時間内には完全には相互変換しないことを示しています。すべての条件でFRET値の分布はノイズだけから期待されるものより遥かに広く、構造的な不均一性、すなわち分子ごとに異なる長時間持続する形が存在することを明らかにしました。作動薬が結合すると平均FRETレベルは上昇し、受容体が内側のヘリックスが“活性様”の配列にある時間が増えることを示します。しかし相関解析は、高FRETあるいは中間FRETの状態に入った受容体は少なくとも数百ミリ秒はその状態に留まる可能性が高いことを示しています。これらの結果は、より高速な実験に基づく以前の推定を更新し、長時間持続する状態の特徴的“滞在時間”をミリ秒から0.1秒を大きく超える値へと延長します。
受容体のエネルギーランドスケープの新しい地図
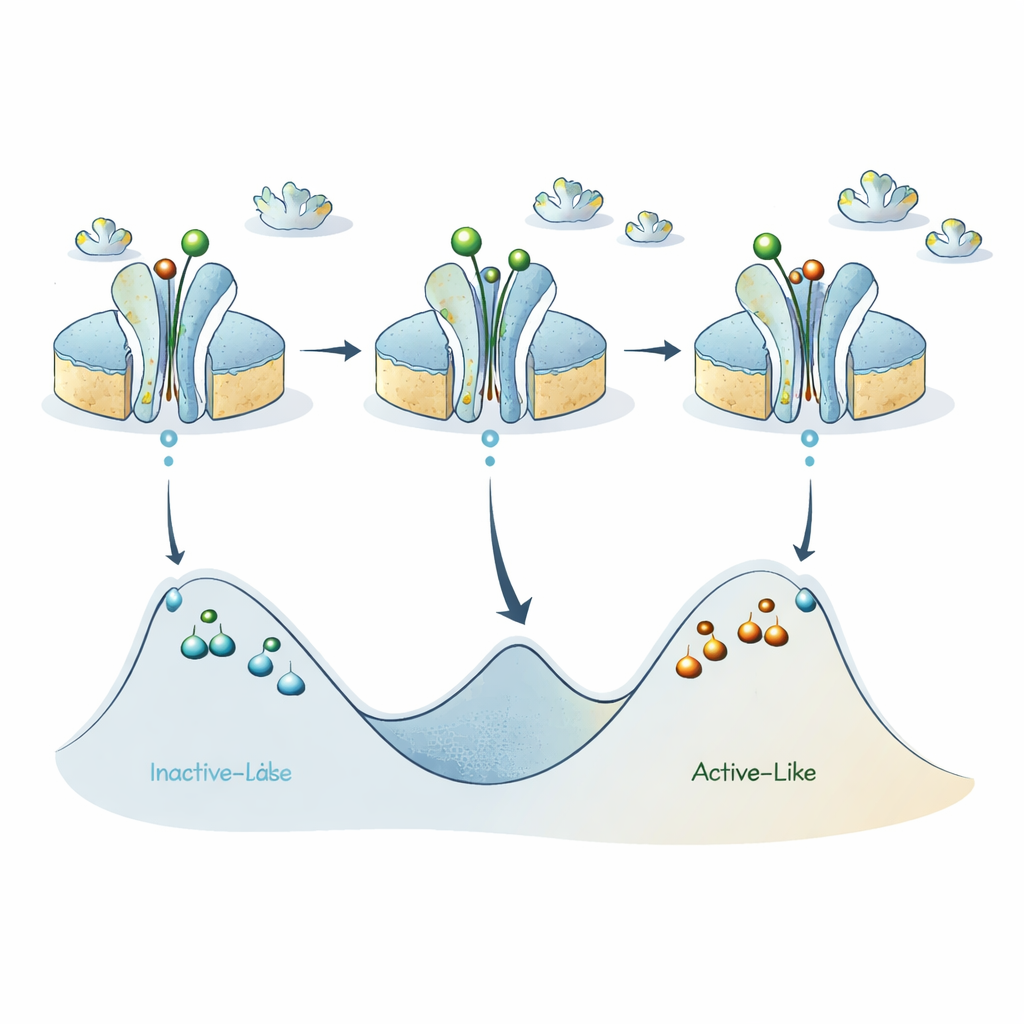
これらを総合すると、著者らはA2A受容体が主に不活性様状態と活性様状態の間を切り替えるという従来モデルを洗練させます。新しいデータは、これら2つの大きなカテゴリのそれぞれが実際には複数のサブ状態を含み、それぞれがかなりのエネルギー障壁で隔てられていることを示唆します。そのため個々の受容体は、活性様あるいは不活性様のあるバージョンに驚くほど長時間“はまり込む”ことがあります。作動型リガンドは主な不活性‑活性間の障壁を下げ、サブミリ秒スケールでの迅速な切り替えを促進しますが、各領域内部の内部障壁は高いままであり、ABEL‑FRETが検出する長時間持続するサブ状態を生じさせます。
将来の医薬品にとっての意味
専門外の方への要点は、A2A受容体のような薬物標的が単純に「オフ」と「オン」を切り替えるわけではないということです。代わりに、それは凸凹の多い形のランドスケープを探索し、そのいくつかは細胞内のシグナル伝達や薬の時間的作用に影響を与えるほど長く持続します。個々の受容体を自然で固定されていない状態のまま長く観察できるようにすることで、ABEL‑FRETは超高速測定と非常に遅い測定の間の重要なギャップを埋めます。この手法は多くの膜タンパク質に適用でき、薬物候補がどのように受容体の形を呼吸し、変化し、応答するかについて、より完全で時間分解能の高い図を提供します。
引用: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
キーワード: Gタンパク質共役受容体, 単一分子FRET, アデノシンA2A受容体, タンパク質の立体配座ダイナミクス, ABELトラップ