Clear Sky Science · ja
結合姿勢の深さが可視スイッチ型リガンドの5-HT2A受容体に対する有効性を調節する
スイッチ可能な脳用薬に光を当てる
光の一閃でオン・オフを切り替え、正確に脳の受容体を制御して副作用を避けられる薬を想像してみてください。本研究は、気分や知覚、幻覚薬に関連する重要なセロトニン受容体に対してまさにそのアイデアを探ります。研究者たちは、ほとんど同一の光応答分子がなぜここまで異なる挙動を示すのかを掘り下げました――ほぼ完璧なオン/オフスイッチのように振る舞うものと、完全にオフになろうとしないものです。彼らの答えは意外に単純な要因にありました:分子が受容体内にどれだけ深く入り込むか、です。
脳の光駆動薬
光で活性化される薬、すなわち光薬理学的ツールは、光が当たることで分子の一部が二つの形(曲がった形と直線に近い形など)を行き来するよう設計されています。これらの形は標的への結合の強さを変え得ます。本研究の標的はヒト5-HT2A受容体で、セロトニンに応答する脳細胞上のタンパク質であり、抗精神病作用や幻覚作用の中心にあります。対象となる分子はN,N-ジメチルトリプタミン(DMT)の誘導体で、光感受性のアゾベンゼン部位が導入されています。二つのバージョンは、環上の小さなメトキシ基が“パラ”位置か“メタ”位置かの違いしかないにもかかわらず、光下での生物学的挙動は劇的に異なります。
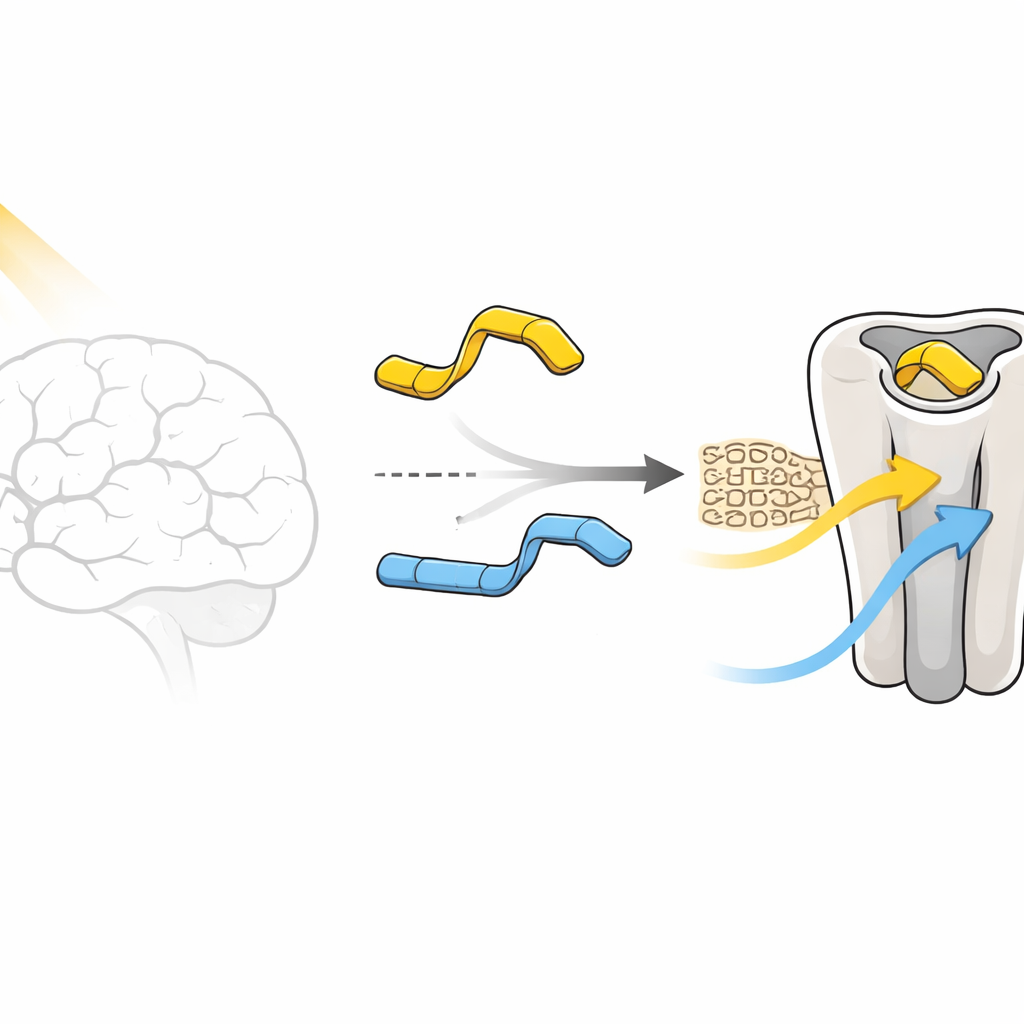
ほとんど双子の分子、まったく異なるスイッチ性
細胞実験では、パラ体(化合物1と呼ばれる)はほとんどデジタルスイッチのように振る舞います。暗所ではその“trans”形が受容体をほとんど活性化せず、むしろわずかに遮断して弱いアンタゴニストのように働きます。光で“cis”形に変わると、同じ分子が中程度のアゴニストとなり受容体を部分的にオンにします。一方、メタ体(化合物2)はこのようには協力しません:光・暗のどちらの形でも受容体をかなり活性化したままにし、真の“オフ”状態を示しません。本論文の中心的な謎は、環上の小さな置換基をわずかに移動させるだけの化学的変化が、なぜ受容体の応答をこれほど劇的に変えるのか、という点です。
原子レベルの“映画”で内部を覗く
これを解明するために、研究チームは広範囲の全原子分子動力学シミュレーションを用い、受容体、周囲の膜、水、および各リガンド中のすべての原子の詳細な“映画”を合計約80マイクロ秒にわたって再生しました。彼らは両分子のそれぞれの光制御形と、5-HT2A受容体の不活性型と活性型の両方をシミュレートしました。タンパク質内部の既知の構造的“マイクロスイッチ”(回転する重要なトリプトファン、切断される塩橋、コア深部のナトリウムや水の動きなど)を追跡することで、受容体がオフ寄りかオン寄りかを判定できました。また、新しい分子がよく研究された部分アゴニストであるLSDの結合姿勢をどれだけ模倣しているかを、環系の重なりを指標に比較しました。
形状だけでなく深さが重要
核心的な洞察は、分子の有効性は主に受容体の結合ポケットにどれだけ深く挿入されるかによって決まる、ということです。不活性受容体では、パラ体のtrans形が特別な水素結合を形成して異常に深く引き込まれ、典型的な活性化接触が起こる領域より下まで入り込みます。この“過剰挿入”により、受容体をオンに切り替える重要な極性残基に触れることができず、オフ状態を安定化させます。メタ体のtrans形は同じアンカリング接触を形成できず、むしろより高い位置にとどまり、LSDに似たポーズで活性化と両立するため残存的な活性を示すのです。光で両分子をcis形にすると、一般に浅めでよりアゴニスト様の位置に移動します。しかしここでも幾何学が重要です:活性型受容体では、cisの化合物2が二本のヘリックス間の疎水性トンネルに深く滑り込み、持続的な水素結合を形成して強いアゴニスト挙動を補強できる一方、cisの化合物1は立体障害によりそれができません。
内部の水とイオンの微妙な制御
シミュレーションはまた、結合深さが受容体活性化に影響することが知られている内部ナトリウムポケットと水の経路を微妙に調節することを示しています。パラ体のtrans形の深く硬い結合はナトリウムイオンをきつく閉じ込め、周辺領域を比較的乾いた状態に保ち、これはオフ状態に関連する特徴です。対照的に、メタ体やcis形のより移動しやすい結合はより多くの水の侵入を許し、ナトリウム環境を緩めて受容体を活性化しやすくします。重要な芳香族の“トグルスイッチ”残基は、リガンドが柔軟で過度に固定されていない場合に向きが変わりやすく、特にcisの化合物2では受容体をオン寄りにさらに押しやる効果があります。
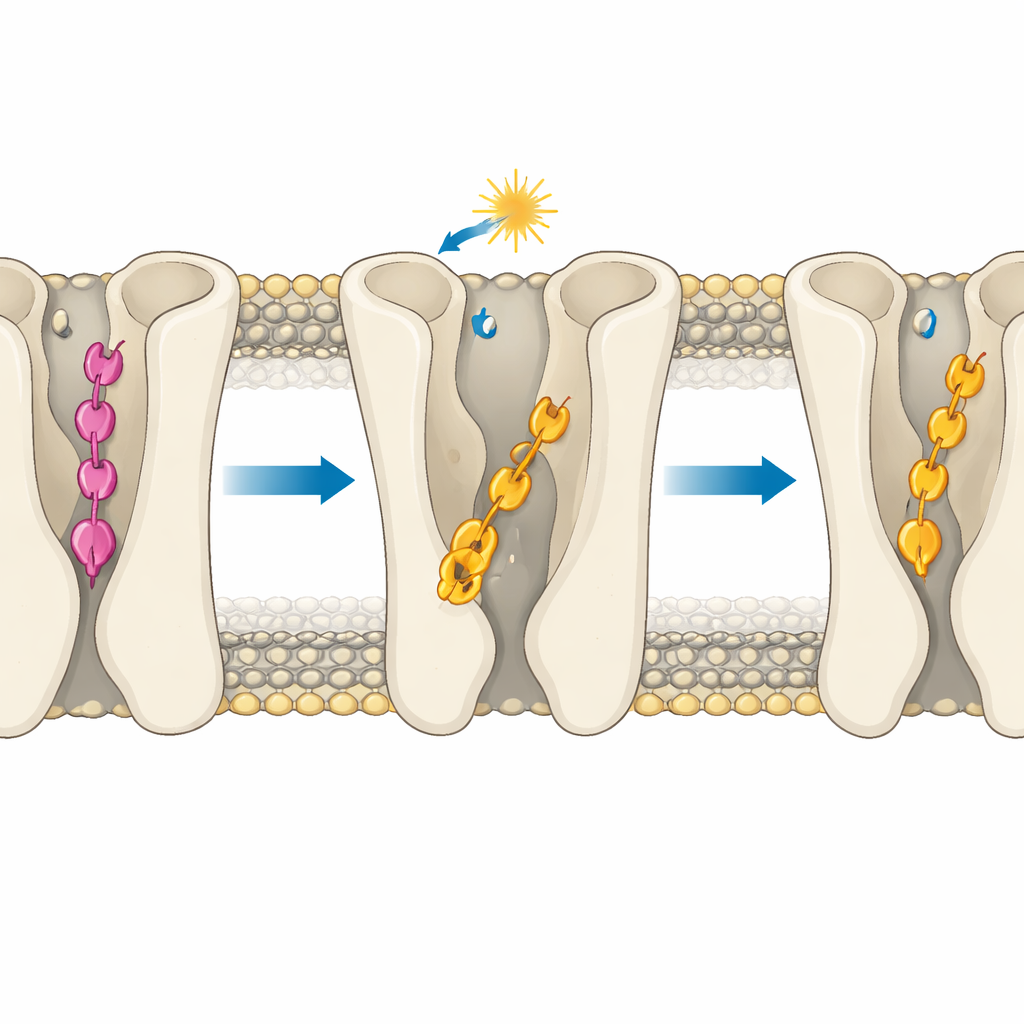
将来の光制御薬のための設計ルール
非専門家向けのメッセージは、薬が受容体のポケットにどの深さで位置するかが、化学的変化が紙上ではわずかに見えても、オフ、部分オン、強いオンの違いを生むことがある、という点です。一つの可視スイッチ型リガンドが過剰に挿入して受容体をロックオフしてしまう一方で、非常に近縁の別のリガンドが活性化に適した深さにとどまる様子を示すことで、本研究は明確な設計ルールを提供します:光誘起の形状変化を制御するのと同じ注意で挿入深度を制御せよ、ということです。これらの知見は、副作用を最小限に抑えつつシグナル伝達経路を制御可能かつ可逆的に上下できる次世代の光感受性化合物の創出に道を開くでしょう。
引用: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
キーワード: 光薬理学, セロトニン5-HT2A受容体, 可視化スイッチ型リガンド, GPCR活性化, 分子動力学シミュレーション