Clear Sky Science · ja
tau/TDP-43 液滴の研究から明らかになった多成分タンパク質凝縮体における足場-クライアントの振る舞いと構造的組織
小さな油滴のように振る舞うタンパク質
細胞内では、多くのタンパク質が水性の細胞質に均一に溶けているわけではありません。代わりに、それらは油滴のような小さな液滴として凝集します。本研究は、アルツハイマー病やその他の認知症と密接に関連する二つのタンパク質、tau と TDP-43 がどのように共同で液滴を形成するかを調べています。これらの液滴がどのように形成され、混ざり合い、組織化されるかを明らかにすることで、加齢した脳に有害なタンパク質凝集が生じる理由や、それを制御する方法の手がかりを提供します。
なぜこの二つの脳タンパク質が重要か
tau と TDP-43 はいずれも神経変性疾患で毒性のある凝集体を形成することで知られます。従来は個別に研究されることが多かったものの、ヒトの検案では両者が同じ損傷領域に共存する例が増えています。ここから重要な問いが生じます:細胞中に tau と TDP-43 が共存する場合、液滴内でどのように空間を共有し、その共有環境が疾患関連の凝集を促進するのか?著者らは簡略化しつつ現実的なモデルとして、tau と TDP-43 の低コンプレックス配列(LCD;液滴形成や最終的な固化に最も寄与する部分)を用いることを選びました。
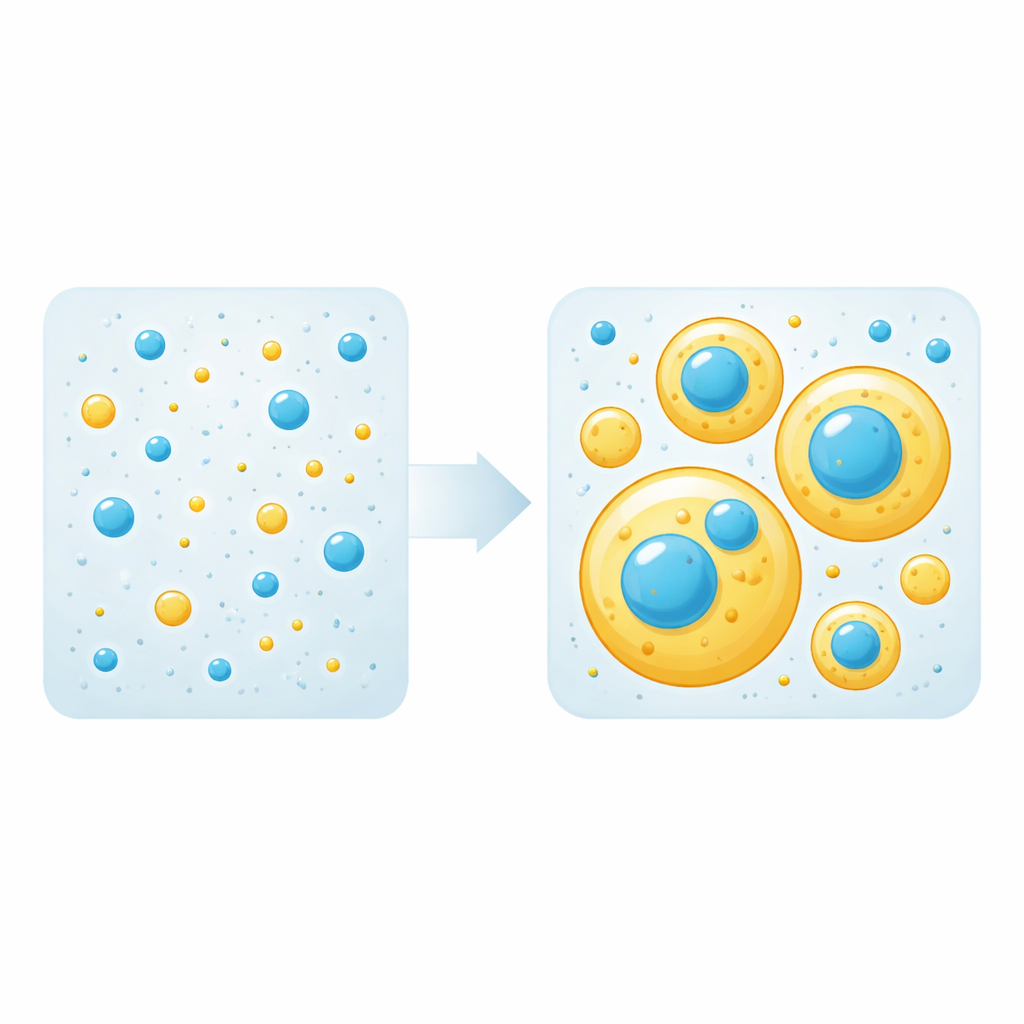
液滴、“スキャフォールド(足場)”と“クライアント(依存体)”
これらの液滴は、タンパク質間の引力がタンパク質と水との相互作用を上回るときに形成され、溶液が高密度相(液滴)と希薄相に分かれます。混合系では、液滴を構築するために必要なタンパク質だけがあり、これを「スキャフォールド」と呼びます。その他のタンパク質は単に「クライアント」として液滴に取り込まれます。研究チームはまず各タンパク質単独で液滴を形成し始める濃度閾値を測定しました。次に tau と TDP-43 LCD をさまざまな比率で混合し、蛍光顕微鏡で液滴の出現やタンパク質の配置を観察しました。注目すべきことに、どちらのタンパク質も濃度によってスキャフォールドにもクライアントにもなり得ることが分かりました:自身の閾値を超えれば液滴を構築し、閾値以下では相手が作る液滴に受動的に取り込まれます。
層状液滴と不思議なハロー(光輪)
両方のタンパク質が単独で液滴を形成できる十分な量がある場合、単一の均一な液滴に混ざり合うのではなく、大きな tau 濃厚の液滴が小さな TDP-43 濃厚の液滴を包み込むような層状の多相構造を作りました。ガラス上での接触挙動の測定から、TDP-43 液滴の表面張力は高く、したがってより濡れやすい tau 液滴の内部に収まるほうがエネルギー的に有利であることが示されました。界面では目を引く特徴が現れました:tau は TDP-43 液滴の表面に明るい「ハロー」として特に高濃度で蓄積し、tau 自身が液滴形成閾値以下であってもこのハローが見られました。時間経過と共に、TDP-43 濃厚領域はより固体に近い硬化を示す傾向があり、tau 濃厚領域は液体の性質を保ち続けることから、長く存続する凝集体への移行性に違いがあることが示唆されます。
相互作用の調整と微視的メカニズムの探査
次に著者らは、どの分子間力がどのタンパク質をスキャフォールドやクライアントにするかを制御するかを検証しました。TDP-43 LCD の凝縮を駆動する疎水性(疎水的)相互作用を 1,6-ヘキサンジオールで選択的に弱め、別に tau の凝縮を駆動する静電的(電荷に基づく)相互作用を塩濃度上昇で弱めました。いずれの場合も、あるタンパク質の主要な相互作用を無効化するとそのタンパク質は液滴を形成できず、相手の液滴内のクライアントへと変わり、濃度を下げた場合と同様の振る舞いを示しました。ハローのより深い理解のため、塩濃度を変えてどれだけ tau が TDP-43 液滴に取り込まれるかを調べ、各アミノ酸を単純化したビーズとして扱う計算シミュレーションを行いました。これらのシミュレーションはハローを再現し、tau の負に帯電した N末端領域の最初の約40残基が液滴表面にアンカーのように付着し、分子の残りが周囲の液体側に伸びて“両親媒性”(一部は液滴を好み、一部は水を好む)シェルを作ることを示しました。N末端のこの伸びを欠く短縮版 tau フラグメントを用いた実験は、これがないとハローが消えることを確認しました。

脳疾患への示唆
これらの結果は、多成分タンパク質液滴がどのように組み立てられ、組織化されるかについての一般的なルール群を明らかにします。この tau/TDP-43 系では、疾患細胞で見られる状況を反映して、濃度と相互作用の強さがどのタンパク質が液滴を構築し、どれが単にその中に存在するかを共同で決定します。表面張力と両親媒性の配列は層状液滴やハローを形作り、複数の疾患関連タンパク質を同じ狭い空間に濃縮して長期的な硬化を促す可能性があります。一般向けの要点は、tau と TDP-43 が単に無秩序に塊を作るのではなく、単純な物理原理に支配された構造化された液滴へ自己組織化するということです。これらの原理を理解し最終的に操作することは、神経変性疾患における有害なタンパク質蓄積を遅らせたり防いだりする新たな道を開く可能性があります。
引用: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
キーワード: タンパク質凝縮体, 液-液相分離, タウ(tau), TDP-43, 神経変性