Clear Sky Science · ja
光制御可能なアゾベンゼン架橋可イオン化両親媒性ヤヌス糖化合物:単一成分・臓器可変のpDNA送達
より賢い遺伝子送達に光を当てる
遺伝子治療は、細胞に直接遺伝情報を届けることで病気を根本から治療する可能性を秘めています。しかし、この壊れやすい貨物を血流に乗せて安全に運び、正しい臓器へ、さらに標的細胞の内部へ届けることは依然として大きな課題です。本研究は、体内へ入れる前に光で挙動を切り替えられる新しい糖ベースの小さな粒子群を提示します。これにより、治療用遺伝子の到達先や発現の強さを誘導でき、かつ細胞へのダメージは比較的抑えられます。 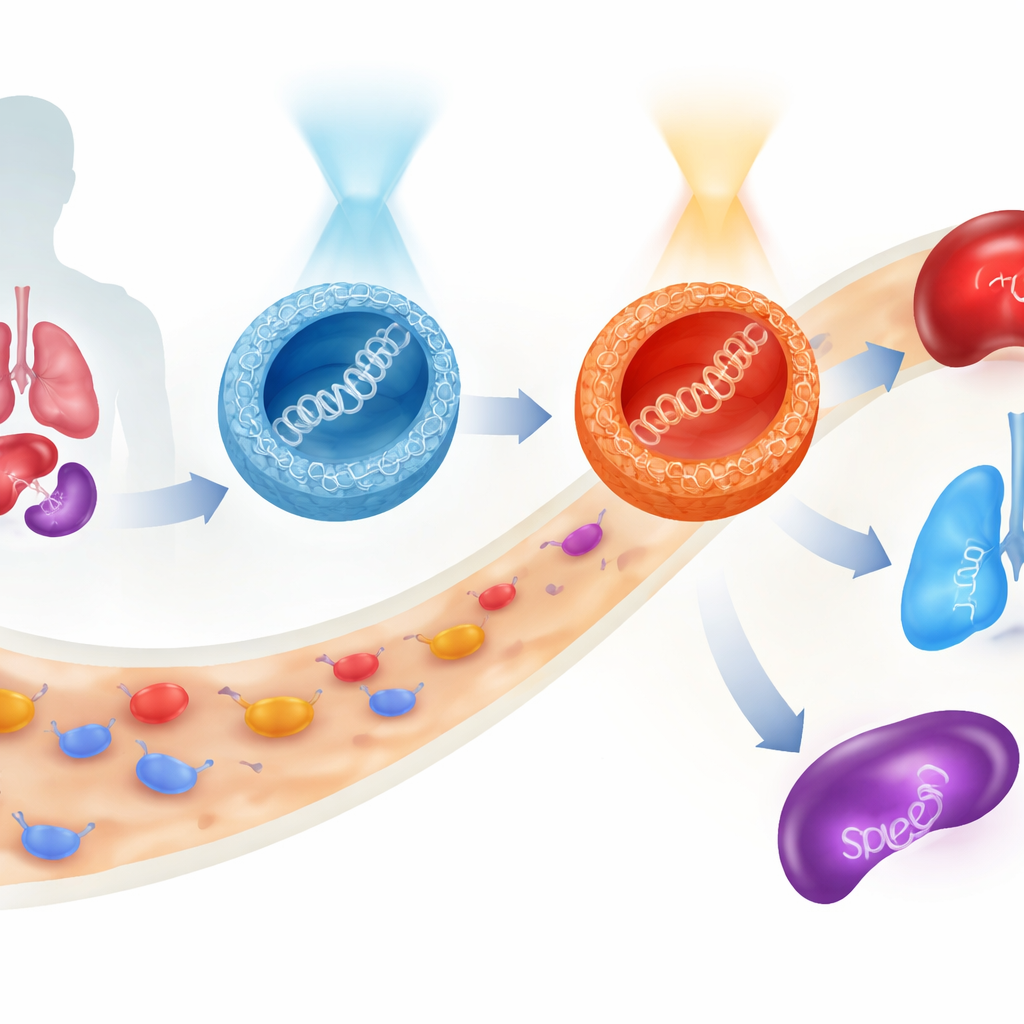
精密な遺伝子運搬体の必要性
現在最も成功している遺伝子送達体は脂質ナノ粒子であり、これがmRNA COVID-19ワクチンを可能にしました。これらの多成分エマルションは核酸を包み保護しますが、主に肝臓に集まりやすく、細胞内で貨物を放出する割合は低い傾向があります。組成を調整すれば標的臓器を変えられますが、混合物は複雑で正確な制御が難しい。本研究チームは代わりに、単一で定義の明確な分子が自発的に集合して予測可能な形と挙動を持つナノ粒子を形成し、外部からの単純な光トリガーで能動的に調整できるよう設計することを目指しました。
光で制御される分子のシーソー
この新しい系の核心は、一対の「ヤヌス」糖化物です。これらは二つのグルコース単位から構成され、親水性の帯電したヘッドと疎水性の尾部を備え、中央のアゾベンゼン“ヒンジ”で結ばれています。アゾベンゼンは異なる色の光にさらされると、E型とZ型という鏡像に似た二つの形状の間を反転できます。DNAが存在する水溶液中では、多数のこれらの分子が自発的に集まり、プラスミドDNAを包む柔らかな層状粒子を形成します。研究者らは糖とヒンジの間を酸素架橋にした版と硫黄架橋にした版の二種類を用意し、安定性や生物学的挙動を微調整しました。溶液を事前に照射することでE型またはZ型のどちらかを富化させ、それぞれの状態が生成される遺伝子送達粒子にどのように影響するかを調べました。
形を変える粒子の挙動
粒子サイズ、表面電荷、内部構造の測定から、E型とZ型の光誘起スイッチが明確な物理的影響をもたらすことが示されました。一般にZ型では、より小さく均一な形状で、内部がより秩序だった層状構造を持つナノ粒子が生成され、E型よりも規則的でした。電子顕微鏡観察では、これらの内部配列が脂質様の層とDNAが交互に並ぶ様子に似ていることが明らかになりました。重要な点として、両方のイソマー状態ともにDNAを酵素分解から保護しました。腎臓、肝臓、免疫組織由来の培養細胞では、同一のDNAにもかかわらずイソマー状態の違いが遺伝子発現量に劇的な差をもたらしました。粒子が細胞内に入った後に繰り返し光パルスを与えると発現が数倍に増強され、これはスイッチによる機械的な衝撃で粒子が緩み貨物を放出しやすくなること、及び細胞内小器官からの脱出を助ける可能性を示唆します。 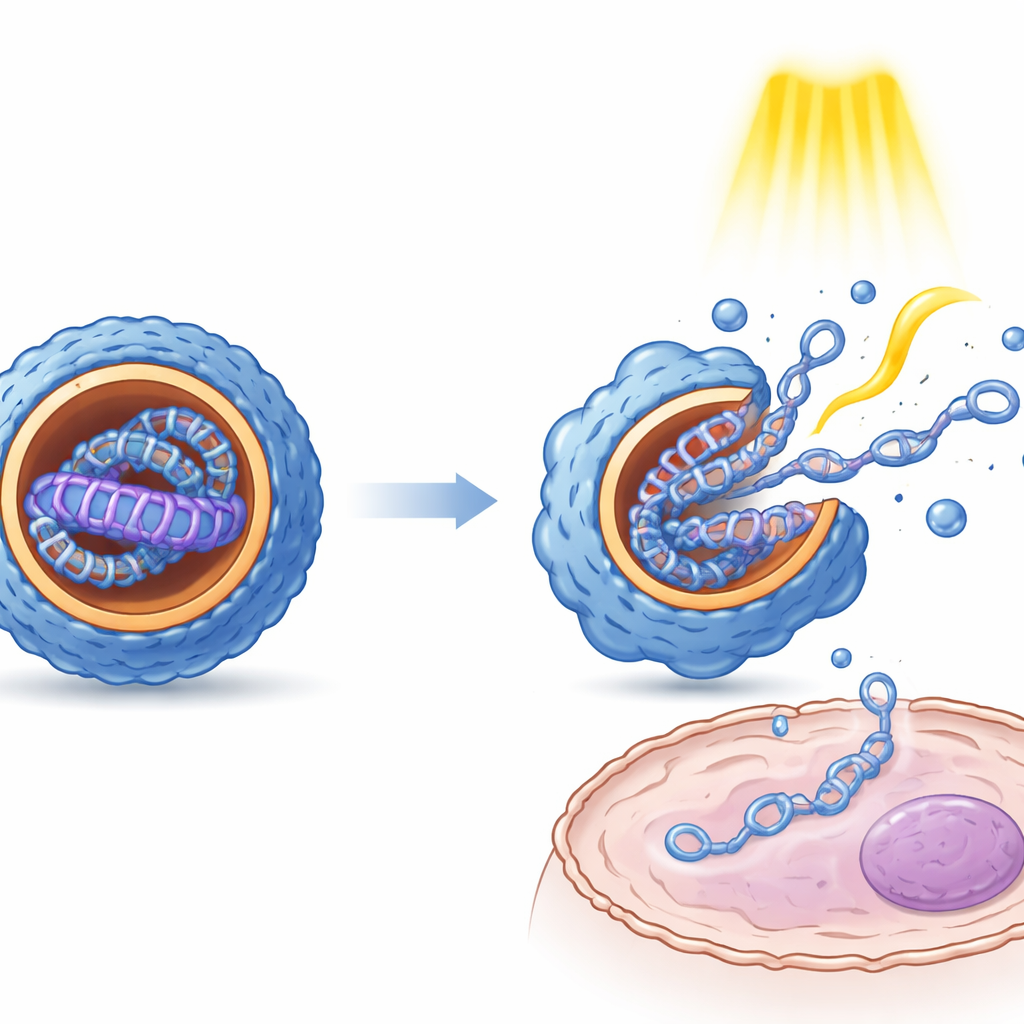
遺伝子を特定の臓器へ導く
最も驚くべき挙動はマウスで観察されました。酸素架橋粒子をE型豊富な状態で投与すると、マーカー遺伝子の発現は主に肝臓に、わずかに肺でも見られました。注入前にZ型へ前スイッチすると総発現量が増加するだけでなく、肺への比率が高まることが分かりました。一方、硫黄架橋粒子は別の特徴を示しました:そのZ型は主要な免疫臓器である脾臓への偏りを示しました。つまり、同じ基本的分子骨格と同一のDNA貨物を用いながら、架橋の種類(酸素か硫黄か)と光で活性化された形(EかZか)を選ぶだけで、肝臓、肺、または脾臓のいずれかへ主に遺伝子活性を導くことができました。これらの試験を通じて細胞生存率は高く保たれており、系は比較的穏やかであることが示唆されます。
将来の遺伝子医薬への光で調節できる道
平たく言えば、研究チームはDNA用の小さな光で切り替え可能なシャトルを構築しました。注入前に短時間の光処理でシャトルを二つの形のいずれかに「プログラム」します。各形は特有のサイズや表面性をもつナノ粒子へと集合し、それがどの細胞種にどれだけ強く付着し体内のどこへ到達するかを決定します。同じ化学的足場は多くの小さな修飾が可能であり、スイッチングは可逆的でDNA自体を変化させないため、このプラットフォームは遺伝子療法の作用場所や方法を精密に調整する柔軟な手段を提供します。臨床応用に至るにはまだ多くの研究が必要ですが、本研究は光で制御される慎重に設計された単一分子キャリアが、より安全で精密な遺伝子医薬の強力な道具になり得ることを示しています。
引用: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
キーワード: 遺伝子送達, 光応答性ナノ粒子, アゾベンゼンスイッチ, 標的DNA療法, ナノメディシン