Clear Sky Science · ja
医薬化学者に向けた知見を伴う抗がん薬効力(IC50)予測の深層学習モデルのベンチマーク
将来のがん治療薬にとって本研究が重要な理由
新しいがん薬の設計は遅く高価です。というのも、有望な分子ごとに生細胞でその増殖抑制の強さを試験する必要があるためです。本研究は実践的な問いを投げかけます:最新の人工知能ツールは、これらの試験結果を事前に信頼できる形で予測し、実験の時間とコストを節約できるか?著者らは複数の代表的な深層学習システムを体系的に比較し、成功・失敗の条件を検討し、さらに実際の医薬化学者にとって有用性をより現実的に評価する方法を提案します。
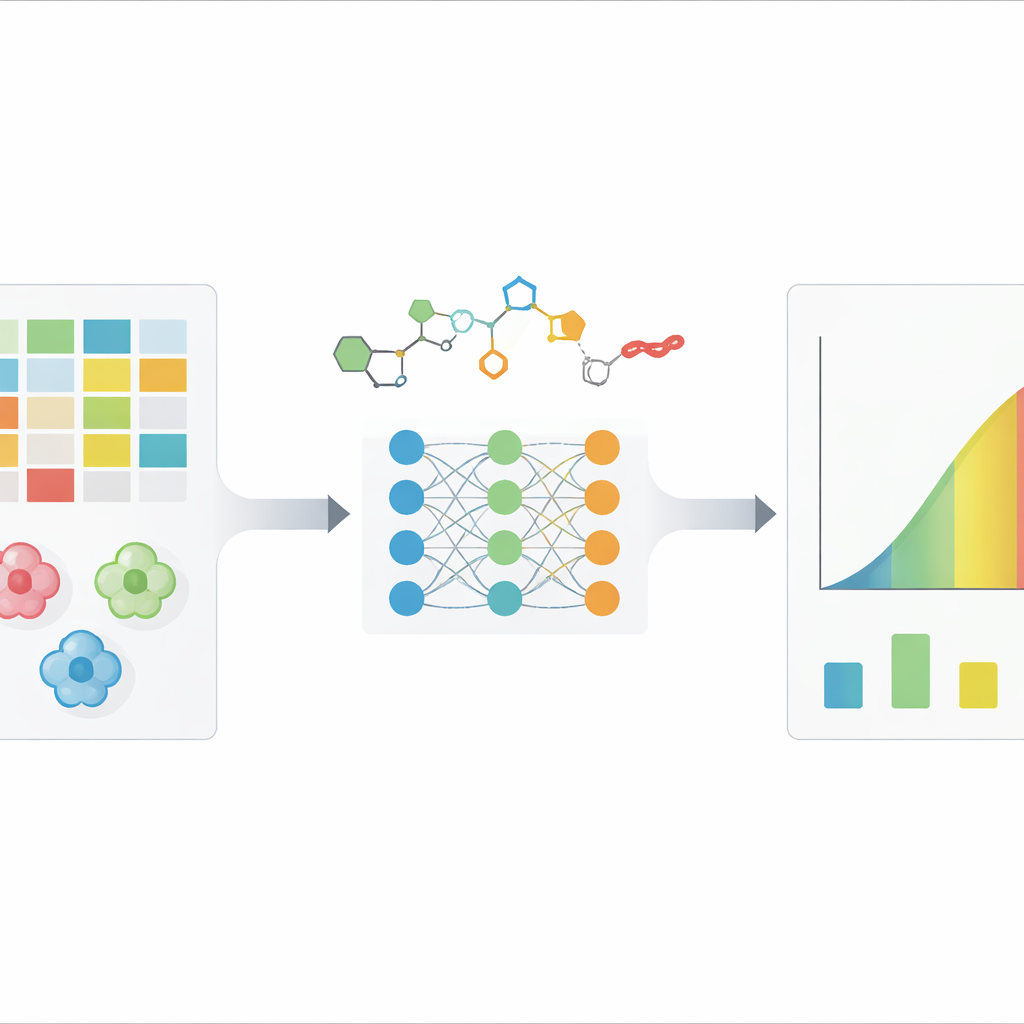
薬ががん細胞と戦う強さの測定
潜在的な抗がん化合物を試験する際、研究者はしばしばIC50と呼ばれる数値を報告します:細胞増殖を半分に抑える濃度です。IC50が低いほど薬効が高いことを意味します。しかし同じ化合物でも、異なるがん細胞株ではIC50が大きく異なることがあり、同じ薬と細胞の組み合わせでもアッセイや条件により数倍の差が生じることがあります。従来のコンピュータ支援設計法は分子が単一のタンパク質標的にどのように適合するかを捉えますが、生細胞の複雑さ全体には苦戦します。近年の深層学習手法は、化学構造とがん細胞に関する詳細な遺伝情報をIC50の大規模データセットから直接学習しようとします。
5つの深層学習ツールを検証
著者らは、薬とがん細胞の表現にそれぞれ異なる戦略を用いる主要な深層学習モデル5種を検討しました。分子を原子と結合のグラフとして扱うもの、細胞の遺伝情報を生物学的プロセスの構造化ネットワークに変換するもの、最も情報量の多い遺伝子に注目するものなどがあります。すべてのモデルは、数万件のIC50測定値を含む主要な資源GDSCから整備された同一データで学習・評価されました。加えて、著者らは意図的に単純な比較手法を用意しました:生物学や化学を無視し、訓練データからの平均IC50値だけを予測する「ベースライン」です。これにより、どの深層モデルが最良かだけでなく、どれほど素朴な近道を本当に上回れているかも問えます。
予測を評価するより現実的な方法
相関や二乗平均平方根誤差のような一般的な機械学習指標は印象的に見える一方、実験室の研究者には解釈が難しいことがあります。この乖離を埋めるため、著者らは予測精度をパーセンテージ誤差やIC50の倍数差に対応する対数スケールでの誤差など、より直感的な指標で表し直しました。重要なのは、実際のIC50測定のノイズ量を大規模なバイオアクティビティデータベースから定量化した点です。一般的なアッセイ条件下では、同一の薬–細胞対について90%の再測定値が約7倍の範囲内に収まることを示しました。これを用いて、著者らは新しい指標、実験変動認識予測精度(EVAPA: Experimental Variability-Aware Prediction Accuracy)を定義しました:モデル予測がその実験的に現実的な範囲内に入る割合です。
モデルが得意な領域と苦手な領域
データをランダムに分割し、多くの薬と細胞株が訓練・検証セットの両方に現れるようにした場合、すべての深層学習モデルは良好な性能を示しました。測定IC50値との強い相関と高いEVAPAスコアを示し、単純なベースラインを明確に上回りました。既知の薬を見せつつ全く新しい細胞株へ一般化させるよう求めた場合でも性能は比較的良好に保たれました;この場合ベースラインも驚くほど健闘し、複数細胞種における薬の平均的振る舞いが既に有用な情報を含むことを示唆します。本当の問題は新たな化学構造に直面したときでした:精度は急落し、相関はほぼゼロあるいは負に近づき、いくつかの試験では単純なベースラインが深層モデルに匹敵するか上回ることもありました。著者らは予測誤差が分子の大きさ、極性、柔軟性などの基本的な薬物特性や細胞株の組織起源に依存するかも調べましたが、弱い相関しか見られませんでした。これはモデルが多様な化学性やがん種全体で概ね同等に機能することを示唆しますが、それでも真に新規の化合物には弱いことを意味します。
最近の研究からの真に新しい分子を試す
公開データベースを超えて検証するため、著者らは医薬化学文献から150を超える最近報告された抗がん化合物を収集し、いくつかの深層学習モデルでこれら未知の分子をテストしました。結果はGDSCデータにおける「新薬」シナリオを反映しました:予測はノイジーで、パーセンテージ誤差が大きく、現実的な実験的許容範囲内に収まる予測の割合は中程度に留まりました。それでも、異なるアッセイ型にわたるモデルの挙動は、薬が細胞に与える影響に関するアッセイ非依存のパターンをいくつか捉えていることを示唆しました。これらのモデルから構築された簡単なウェブサーバーにより、化学者は構造を入力して数百のがん細胞株に対するIC50予測を得られますが、信頼性は新しい分子が訓練セット中の分子に似ている場合に最も高い、という注意書きがあります。
薬物探索にとっての意味
本研究は、現在の深層学習ツールが既知の化学領域内でアイデアの順位付けや探索に既に有用である一方、真に新しい分子設計に対する水晶玉にはほど遠いことを示します。粗雑な平均ベースのモデルが複雑なニューラルネットワークに匹敵する場合があることを強調し、実験変動に基づく精度指標を導入することで、IC50予測ソフトウェアから何を期待すべきかを医薬化学者により明確に示します。結論はバランスが取れています:これらのモデルは、慎重にベンチマークすれば薬物探索の有望な支援手段ですが、分布外の分子に対して信頼して探索を導けるようにするには、アーキテクチャや学習の大幅な改良が依然として必要です。
引用: Garai, U., Pal, A.S., Ghosh, K. et al. Benchmarking deep learning models for predicting anticancer drug potency (IC50) with insights for medicinal chemists. Commun Chem 9, 106 (2026). https://doi.org/10.1038/s42004-026-01916-9
キーワード: 抗がん薬の効力, IC50予測, 深層学習モデル, がん細胞株, 計算薬物探索