Clear Sky Science · ja
RiPP 生合成における前駆ペプチドの均一切断を触媒する S9 プロテアーゼ WprP2
なぜ細胞内の小さな切断機構が重要か
細菌内部では、特化した分子のハサミが長いアミノ酸鎖を小さく活性のある断片に切断し、それらはしばしば抗生物質やその他の有用な天然物になります。本研究は、従来知られていなかった切断ツール—WprP2 と呼ばれるプロテアーゼ—を明らかにし、標的ペプチドをきわめて正確に切り分けることを示しました。この酵素の働きを理解することで、研究者は新たな生理活性ペプチドや次世代抗生物質の設計に役立てる可能性があります。
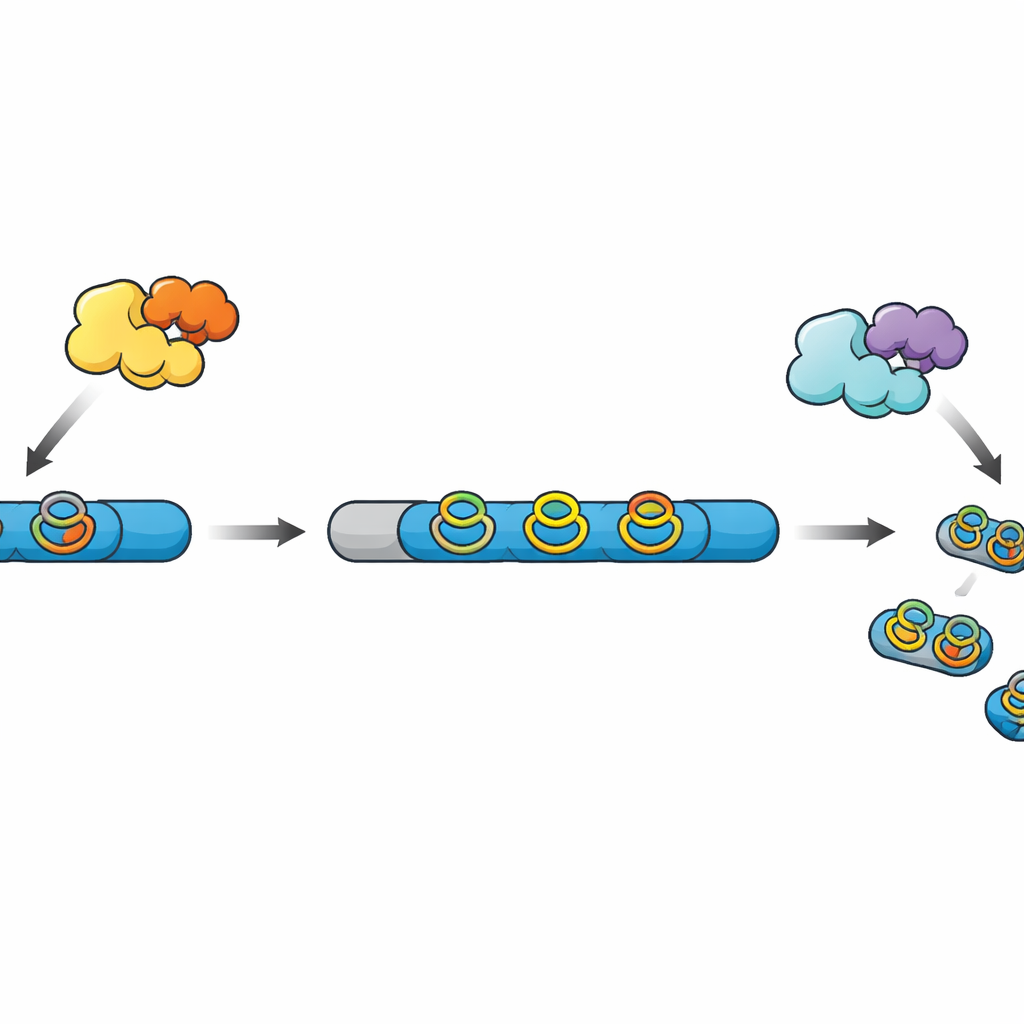
未加工の鎖から完成したミニ医薬品へ
RiPP と総称される多くの近代的なペプチド系天然物は、リボソームで作られる単純な鎖として始まります。これらの鎖は、扱いやすいリーダー領域と、化学的改変ののちに最終生成物になるコア領域を含みます。ほかの酵素が架橋や環を導入してペプチドを安定化・活性化し、最後にプロテアーゼがリーダーを切り離して成熟分子を放出します。最近発見された一群の RiPP では、ラジカル SAM 酵素が芳香族アミノ酸を巻き込む緻密な “シクロファン” 環を構築しますが、既知の多くの遺伝子クラスターでは対応するプロテアーゼが欠如しており、最終処理の過程は謎に包まれていました。
欠けている相方酵素を追跡する
著者らは以前、前駆ペプチド中の繰り返し WPR セグメントのそれぞれに同一の架橋を導入するラジカル SAM 酵素 WprB1 を研究していました。新たな研究では、この酵素の類縁体を細菌ゲノム中で探索し、近傍にプロテアーゼをコードしうる遺伝子があるかを調べました。Streptomyces venezuelae において、有望なクラスターが見つかりました。そこには類似の架橋酵素、その補助タンパク質、3 つの WPR 繰り返しを持つ前駆ペプチド、そして S9 ファミリーに属する候補セリンプロテアーゼ WprP2 が含まれていました。これにより、ペプチドが最終的にどのように切断されて活性断片が放出されるかを解明するための理想的な実験系が整いました。
ペプチドが切り刻まれる様子を観察する
WprP2 を調べるために、研究チームは前駆ペプチドを細菌で発現させ、架橋酵素の有無の両条件で精製し、制御されたインビトロ反応でプロテアーゼと混合しました。質量分析により、WprP2 はまず各 WPR セグメントの直後を切断し、その後配列上の特定のプロリン残基の手前の一定距離で二回目の切断を行うことが示されました。この二段階の切断により、均一な小さな断片の一連が生成されます。注目すべきは、WprP2 がシクロファン環が既に導入されているかどうかにかかわらずこの切断パターンを実行したことで、環は認識に必須ではないことが示されました。市販のトリプシンと比較すると、トリプシンは特定の架橋部位を切れない場合がありましたが、WprP2 は引き続き機能し、その異常な耐性が強調されました。
酵素が何を認識しているかを解読する
研究者らは次に、WprP2 がペプチドのどの特徴を読み取っているのかを問いただしました。切断部位周辺のアミノ酸を体系的に変えることで、多くの近傍残基の置換はほとんど影響を与えない一方、WPR セグメント内の重要なアルギニンや、二回目の切断部位にあるグルタミンやプロリンを変更するとその特定の段階が阻害されることが分かりました。異なる側鎖を持つ関連前駆ペプチドを用いた実験では、プロテアーゼは依然として WPR の直後を切断したが、グルタミン—プロリンの組が存在する場合にのみ二回目の切断を行いました。AlphaFold3 を用いたコンピュータ生成の構造モデルはこの見解を支持しました:予測された複合体では、WPR 基盤部位とグルタミン—プロリン部位がそれぞれ順に酵素の触媒中心に整列しており、逐次的な二段階機構と整合します。
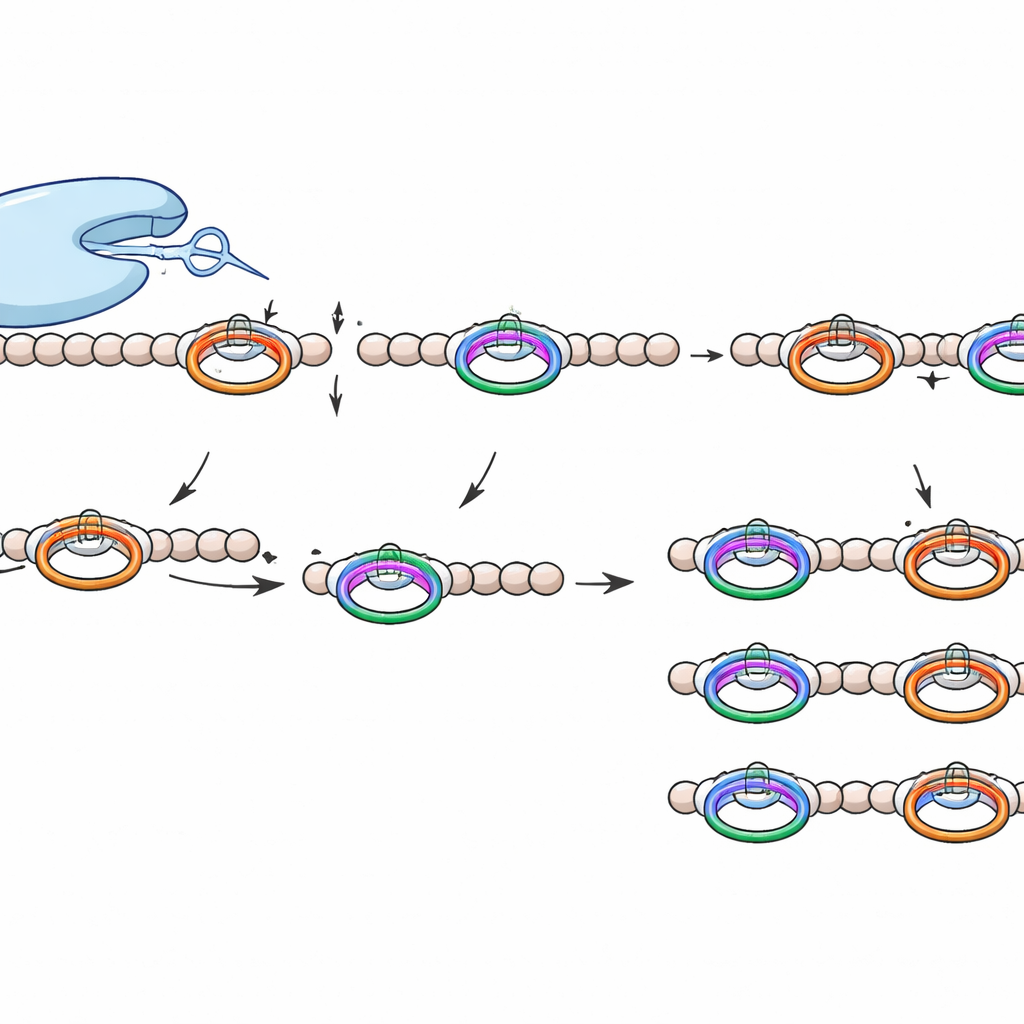
この切断ツールの何が特別なのか
WprP2 は医療的に関連する酵素も含むより広い S9 ファミリーに属しますが、いくつかの点で際立っています。プロリン残基の後ではなく前側(N末側)を切断すること、繰り返しモチーフに作用して前駆鎖全体にわたって均一な断片を生成すること、そして二つの認識部位の間にあるアミノ酸に対して広い許容性を示すことです。この精密さと柔軟性の組み合わせは、RiPP 関連プロテアーゼではこれまでに見られませんでした。
この発見の応用可能性
単純な配列シグナルを認識し、均一で繰り返しの切断を行うプロテアーゼを明らかにしたことで、本研究はペプチド工学の拡充するツールキットに強力な新しい道具を加えます。実用的には、WprP2 は設計ペプチドを放出または再形状化するために利用でき、トリプシンなどの標準酵素に対して耐性を示す複雑な架橋を含むペプチドにも適用できる可能性があります。専門外の読者にとっての要点は、研究者らが長いペプチド鎖を正確で均一な大きさに切り分ける新種の分子ハサミを発見し、潜在的な抗生物質やその他の生理活性分子のより制御された生産への道を開いたことです。
引用: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
キーワード: RiPP ペプチド, セリンプロテアーゼ, WprP2, シクロファン天然物, ペプチド工学