Clear Sky Science · ja
生細胞でタンパク質コンフォメーションを監視するための立体制約誘導発光プローブ
形を変えるタンパク質をリアルタイムで観察する
すべての生細胞内で、タンパク質は信号を伝え、周囲を感知し、重要な機能を果たす過程で常に形を変えています。これらの形の変化が乱れることが多くの疾患の原因になりますが、生細胞内でその動きを直接観察することは、特に非常に速い時間スケールから遅い時間スケールにわたって、これまで非常に困難でした。本論文はBIOSCEと呼ばれる新しい発光プローブを紹介します。BIOSCEはごく小さなタンパク質の動きを可視化する「光の点滅」に変換し、研究者が生細胞内で個々のタンパク質が曲がったりねじれたり相互作用したりする様子をリアルタイムで追跡できるようにします。 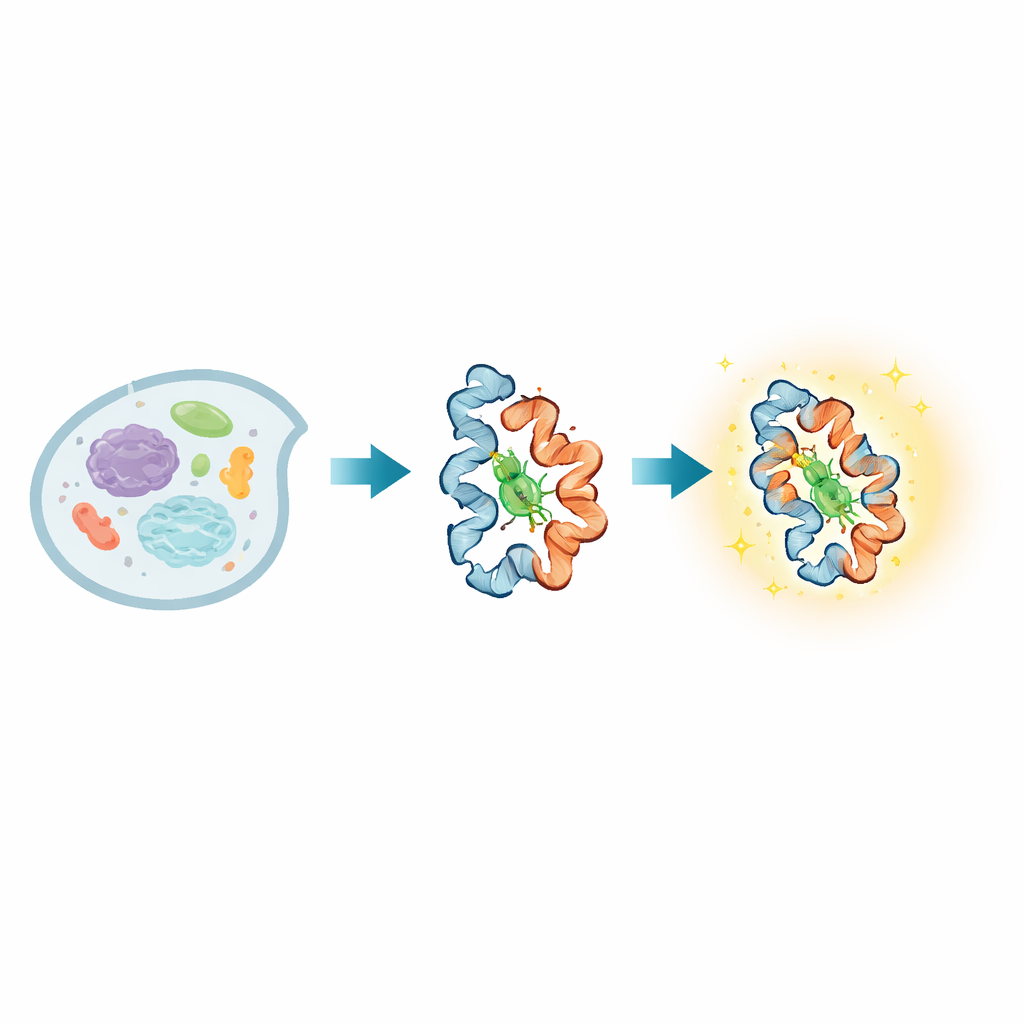
動くタンパク質のための新しい光スイッチ
BIOSCEの核心は、押し込まれると明るくなる小さな色素分子MTPABP-Clです。研究者たちはこの色素を広く使われているタンパク質タグであるHaloTagに結合させます。HaloTagはほとんど任意の関心タンパク質に遺伝学的に融合できます。タグ付きタンパク質が形を変えたり隣接する分子とより密に詰まったりすると、色素が動ける「余地」が変わります。緩い環境では色素の内部部分は自由に回転でき、吸収した光は運動として失われますが、より狭いポケットではその運動が阻止され、代わりにそのエネルギーがより多く光として放出されます。この「立体制約誘導発光」は、単一タンパク質周辺の局所的な混雑の微細な変化をオン/オフの単純な信号ではなく、明るさの滑らかな変化に変換するため、微小なコンフォメーション変化に対して高い感度を示します。
圧迫感度色素の設計と評価
チームはまず、溶液中では暗く、HaloTagやよりコンパクトな融合タンパク質に保持されると明るくなるようにMTPABP-Clを設計・合成しました。注意深い測定により、この色素は青色光を吸収し遠赤色光を発することが確認され、これは細胞深部でのイメージングや長時間観察に有利です。HaloTagにのみ結合したときでも光出力は上昇し、HaloTagが色素を包み込むように折り畳まれるパートナータンパク質と融合するとさらに明るくなりました。計算機シミュレーションは、よりコンパクトなタンパク質配列では色素がより強い混雑、露出面積の縮小、安定化する接触を受け、それらが運動を制限して発光を増強することを確認しました。色素はまたHaloTagに迅速かつ特異的に結合し、タグを欠く細胞ではバックグラウンドが非常に低く、使用濃度で非毒性を保つため、生細胞実験への適用を支持します。 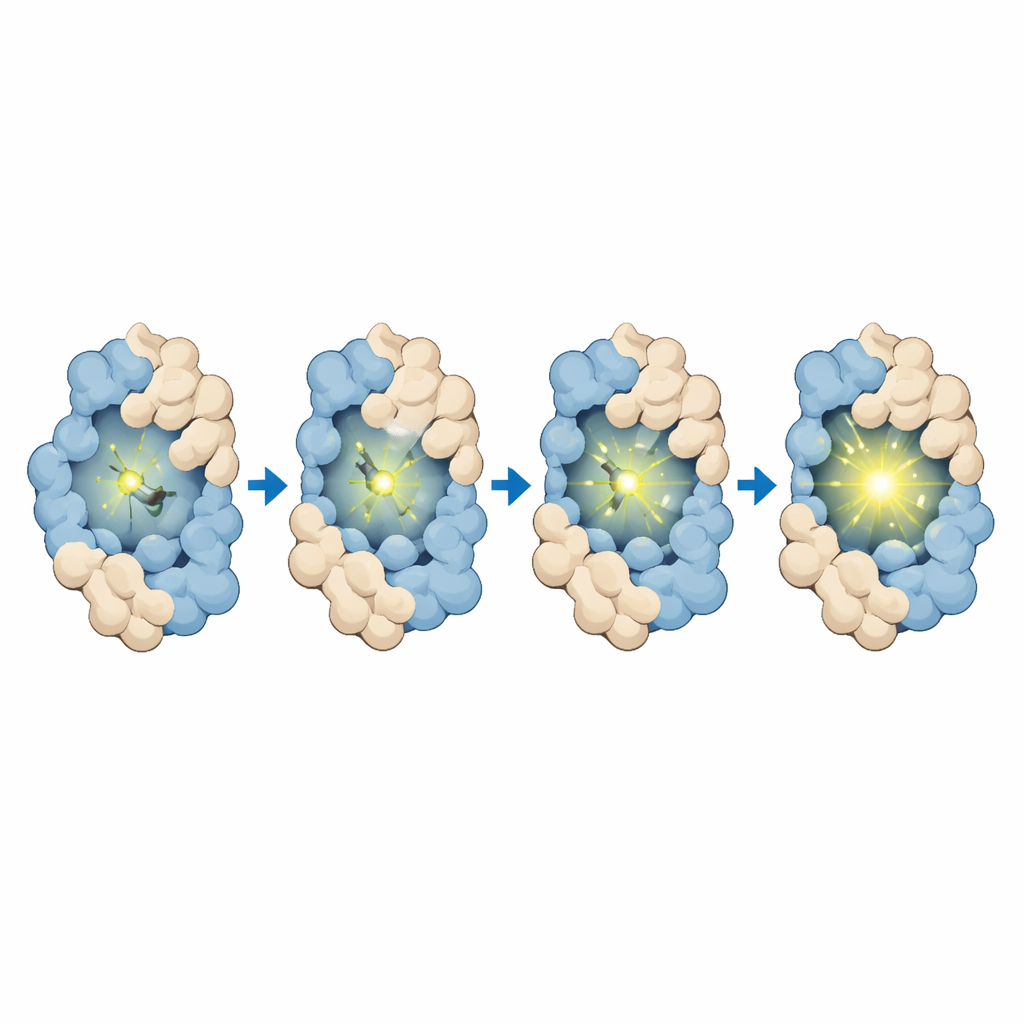
高速信号とタンパク質遭遇の追跡
BIOSCEの能力を示すために、著者らはそれをいくつかのよく知られた細胞過程に適用しました。まず、カルシウムイオン結合時に形を変えるカルモジュリンに基づくカルシウムセンサーを応用しました。カルシウムは神経での発火や多くの細胞イベントで中心的なメッセンジャーです。カルモジュリンをHaloTagに融合しMTPABP-Clで標識することで、SCECaMPと呼ばれる化学遺伝学的指標を作成しました。ヒト細胞やニューロン様細胞では、この指標はカリウム刺激で引き起こされたカルシウムスパイクに合わせて明暗を繰り返し、応答速度は広く使われているGCaMP蛍光タンパク質と同等でした。BIOSCE信号は色素周辺の局所的な混雑に直接依存するため、カルモジュリンの構造変化を忠実に反映し、長時間のイメージングに適した安定した持続的な蛍光を提供できます。
薬剤誘導の相互作用と毒素による損傷の可視化
次に研究者たちは、BIOSCEが薬剤によって二つのタンパク質が引き寄せられるときの追跡に使えるかを検討しました。彼らはラパマイシンが成長制御経路で重要な二つのパートナー、FKBPとFRBを結びつける古典的な系を用いました。FKBPまたはFRBのいずれかにHaloTagを付けMTPABP-Clで標識すると、ラパマイシンがこれらのタンパク質を近づけ再配列させるときに、ミリ秒スケールの迅速な蛍光上昇が観察されました。明るさの増加は、パートナーが近接することで色素の周囲により緊密なマイクロ環境が生じたことを反映しています。より複雑な検証では、神経終末で神経伝達物質放出に不可欠でありボツリヌス神経毒Aの主標的であるSNAP25を調べました。毒素の切断部位の両側にHaloTagを配置し色素で標識することで、切断後のN末端断片とC末端断片の動きを個別に追跡できました。単一粒子追跡により、一方の断片は細胞膜近傍に固定されたままで、他方は細胞質内をより自由に拡散し、その正確な挙動は標識が毒素曝露の前か後かによって異なることが明らかになりました。プローブはこの過程での亜鉛誘導による迅速な構造の微調整さえも報告しました。
生物学・医学への意義
これらの結果は総じて、BIOSCEが個々のタンパク質が生細胞内でどのように移動し、折りたたまれ、相互作用するかを幅広い時間スケールで可視化する多用途な新手法であることを示しています。この手法は一般的なHaloTag融合と単一の小分子色素に依拠するため、原理的には毎回センサー全体を作り直さなくても多くの異なるタンパク質に適用できます。連続的で制約依存の明るさ変化により、研究者は大きな二値的イベントだけでなく微細な構造変化を検出できます。今後、著者らはプローブ導入法とイメージング深度を改良し、BIOSCEが組織や全動物で使用できるようにすることを計画しています。これが実現すれば、タンパク質の位置、運動、機能を健康と疾患の文脈で結びつける強力なツールとなり、最終的には細胞挙動の詳細な計算モデルへとつながる可能性があります。
引用: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
キーワード: タンパク質の立体構造ダイナミクス, 生細胞イメージング, 蛍光バイオセンサー, HaloTagプローブ, ボツリヌス神経毒