Clear Sky Science · ja
標的化された神経膠腫治療のための四重結合カーボンドットナノモデルの開発
手強い脳腫瘍に新たな希望
膠芽腫のような高悪性度の脳腫瘍は、治療が非常に難しいがんの一つです。多くの薬剤は体の他の部位では有効でも、脳の防御機構である血液脳関門を通過できなかったり、移行過程で正常組織を損なったりします。本研究は、より正確に脳腫瘍に入り込み、強力な薬剤の組み合わせを運び、腫瘍細胞の核内で直接放出してがんを効果的に攻撃しつつ正常細胞への影響を抑えることを目指した、実験室で作られた「スマート」なナノ粒子を紹介します。
炭素で作られた小さな配送トラック
新しいアプローチの中心はカーボンドットです。カーボンから作られるナノメートルサイズの粒子で、製造コストが低く水とよく混和し、特定の光で蛍光を示します。表面に豊富な化学的結合点があるため、複数の生体分子を同時に装飾できます。本研究では、研究者らは「四重結合」ナノモデルを作製しました:各カーボンドットは一回のワンポット反応で、二種類の標的ペプチドと二種類の抗がんペイロードに化学的に結合されています。このモジュラー設計により、各ドットは腫瘍細胞を認識し、細胞の障壁を通過し、薬剤を適切な細胞内の住所に届ける小さな配送トラックになります。
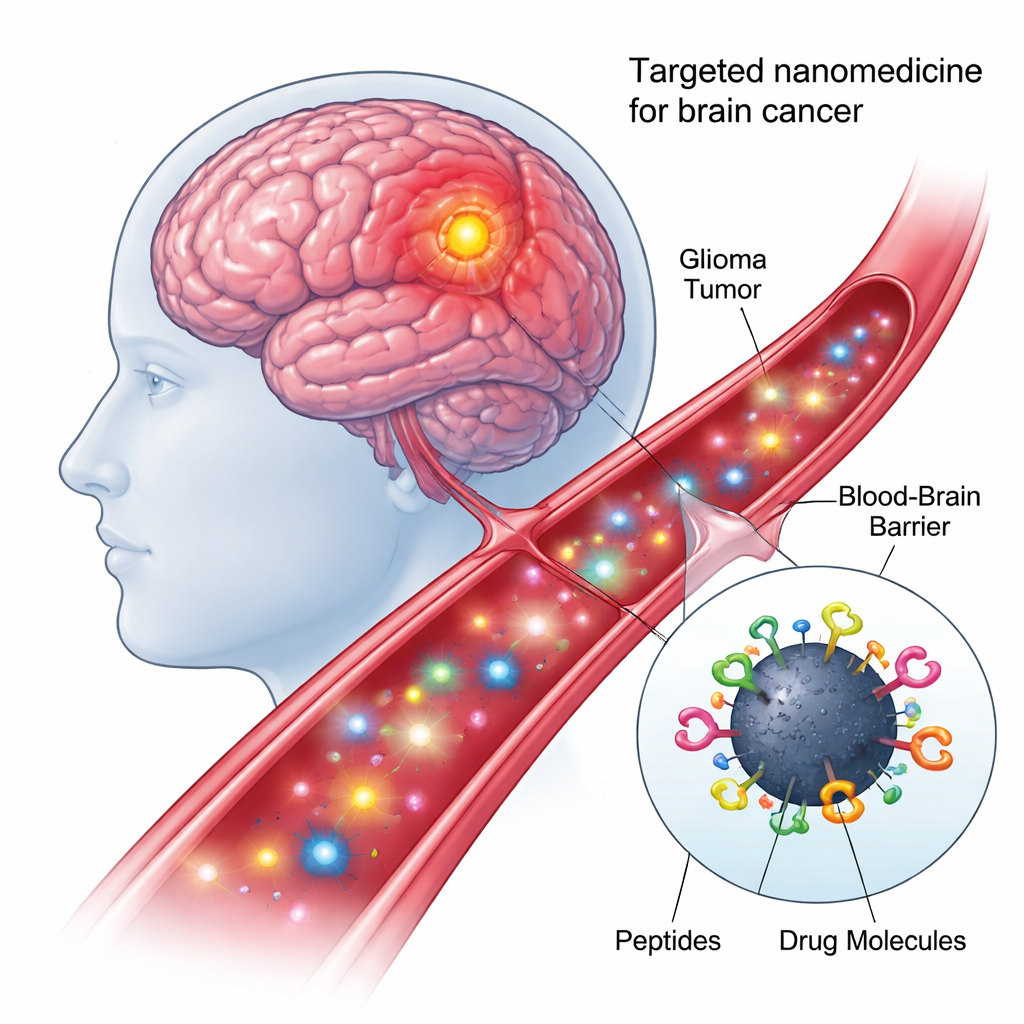
正しい脳細胞を見つけて侵入する
ナノ粒子上の最初のペプチドであるshPep-1は、IL13Rα2と呼ばれる受容体を認識するように設計されています。この受容体は成人および小児の膠芽腫やびまん性橋髄膠腫(diffuse intrinsic pontine glioma)を含む多くの攻撃的な脳腫瘍で高発現していますが、正常な脳細胞では弱くしか存在しません。shPep-1がIL13Rα2に結合することで、カーボンドットは腫瘍細胞に選択的に集まり、受容体媒介性取り込みを通じて細胞内に入ります。二つ目のより長いペプチドlnPep-1は核局在化シグナルを含みます:これは積荷が核膜を通過してDNAが格納される細胞の制御中枢に到達するのを助ける短い配列です。この二つのペプチドが組み合わさることで、ナノ粒子は腫瘍選択性と、細胞内に入った後に核に到達する能力を同時に獲得します。
協調した薬剤攻撃を届ける
治療用ペイロードは二つの小分子で構成されます。第一はエピルビシンで、DNAに挿入されて二本鎖切断の修復に必要な酵素を阻害することでがん細胞を死滅させる既知の化学療法薬です。第二は5-アミノイミダゾール-4-カルボンアミド(AIC)と呼ばれる代謝物で、生理学的pHで脳腫瘍薬テモゾロミドから生成されます。先行研究で同じグループは、カーボンドット上にエピルビシンとAICを組み合わせると、いずれか単独よりもがん細胞の死滅が強化されることを示していました。新しい設計では、両者が二重ペプチドナノ粒子上で共同送達され、腫瘍細胞核内での相乗効果を狙っています。
腫瘍細胞には強力、正常細胞には穏やか
ナノモデルの有効性を検証するため、研究チームは成人膠芽腫、小児膠芽腫、およびびまん性橋髄膠腫モデルを含む複数の高悪性度グリオーマ細胞株に四重結合カーボンドットを曝露しました。非常に低濃度(50ナノモーラー程度)でも、腫瘍細胞の生存率は未処理対照の約半分まで低下し、より高濃度では試験したすべての結合体がほとんどの腫瘍細胞を死滅させました。重要なのは、四重ナノモデルはエピルビシン全体の搭載量が少ないにもかかわらず、より単純な「単一ペプチド」バージョンより優れた性能を示した点です。非がん性の血管平滑筋細胞で試験したところ、同等の生存率低下を得るには約25〜40倍多くのナノ粒子を必要とし、腫瘍標的化による有用な安全域が示唆されました。
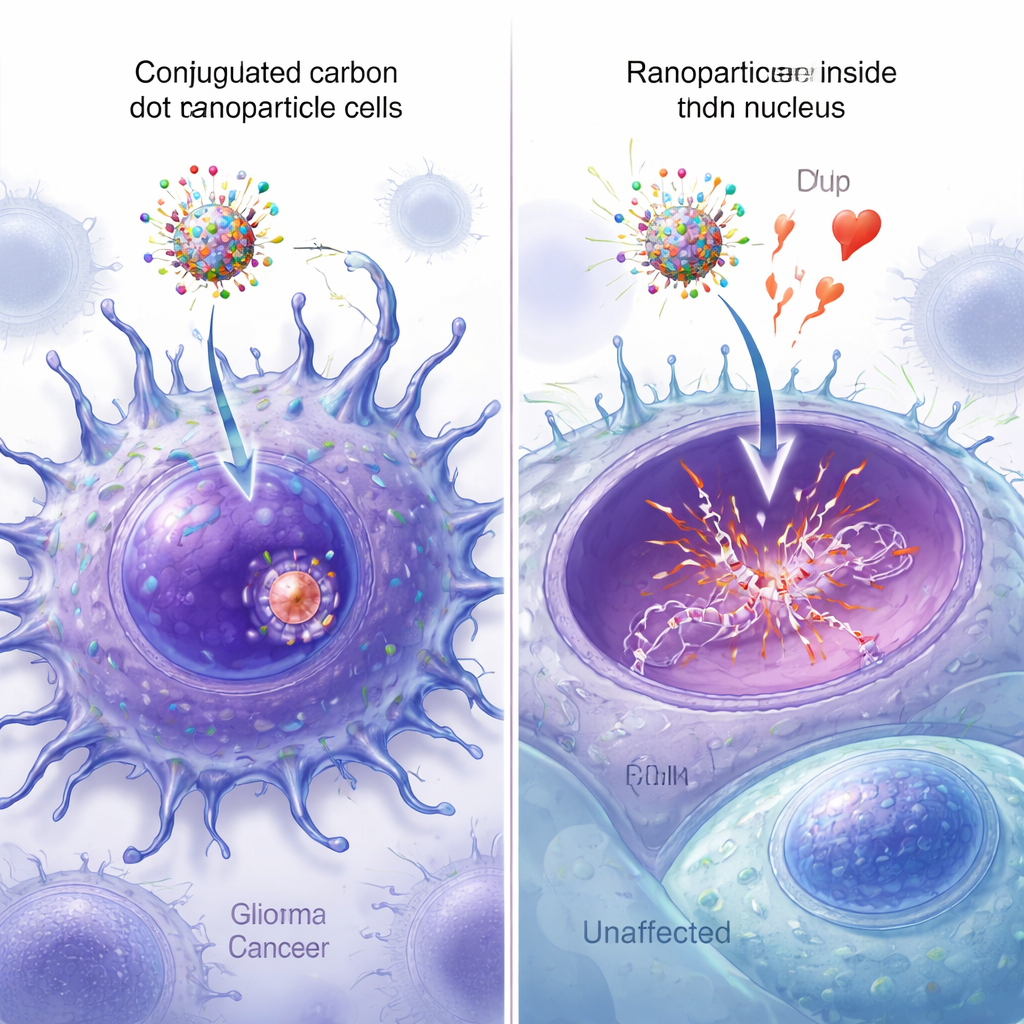
ナノ粒子が核に到達する様子を可視化
蛍光標識されたナノ粒子により、各設計がどれだけ細胞に入り核に到達するかを観察できました。顕微鏡下では、両方のペプチドを備えたカーボンドットが細胞全体にわたって最も明るいシグナルを示し、緑色のナノ粒子蛍光と青色の核染色との強い重なりが観察されました。定量的画像解析は、二重ペプチド粒子が核での共局在化が最も高く、単一ペプチドまたはペプチド非装着粒子を有意に上回ることを確認しました。さらに分光法、質量分析、および原子間力顕微鏡による測定は、四つの成分がすべてカーボンドットに成功裏に結合され、サイズが適度に増加したことを検証し、エピルビシンの重要なDNA結合機能を損なっていないことも示しました。
将来の脳腫瘍治療にとっての意義
患者にとって、これらの知見は現時点では治療として準備が整ったものではなく、初期段階の細胞培養での実証に過ぎません。しかし、小さく安定で比較的作りやすい炭素ベースのナノ粒子が、標的ペプチドや薬剤の組み合わせで迅速に個別化できるという有望な概念を示しています。IL13Rα2を過剰発現する腫瘍細胞に薬剤を的確に誘導し、核内に濃縮することで、将来的には用量の低減、副作用の軽減、膠芽腫やびまん性橋髄膠腫のような致死率の高い脳腫瘍に対するより個別化された治療戦略が可能になるかもしれません。
引用: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
キーワード: 膠芽腫, ナノ医療, カーボンドット, 標的薬物送達, 脳腫瘍