Clear Sky Science · ja
限られたcryo-EM観測でAlphaFoldをファインチューニングする
タンパク質の形が見えにくい理由
タンパク質はエネルギー産生から神経伝達まで、体内のほとんどすべてのプロセスを担う微小な分子機械です。それらがどのように機能するか、あるいは薬剤がどう制御できるかを理解するには、正確な三次元形状を知る必要があります。この課題に対して強力な二つの手段が現れました。凍結タンパク質の大量のぼんやりしたスナップショットを撮るcryo–電子顕微鏡(cryo‑EM)と、配列からタンパク質構造を予測する人工知能システムAlphaFoldです。しかし多くの実験ではcryo‑EMのデータが不完全であり、AlphaFoldの予測が実際と一致しないこともあります。本論文はCoCoFoldを提案します。これはAlphaFoldに対して難しいcryo‑EMデータを直接“聞かせ”、予測を改善する方法です。
カメラが少なすぎるとき
Cryo‑EMはタンパク質を急速冷凍し、多数の個々の粒子をさまざまな角度から撮影して、それらを統合して3次元マップを作成します。しかし実際には、十分な良質画像が得られないことがしばしばあります。タンパク質が短時間しかとらえられない高エネルギー状態にいる場合、捕捉される粒子はごくわずかですし、氷面上で特定の向きを好むと多くの視角が欠けます。これらはいずれもぼやけた不完全なマップを生み出し、信頼できる原子モデルへ翻訳するのが難しくなります。既存のソフトウェアはAlphaFoldの予測構造をそのようなマップに当てはめることができますが、成功は最初に鋭く高分解能のデータがあるかどうかに大きく依存します。
生の画像から学ぶようAlphaFoldを教える
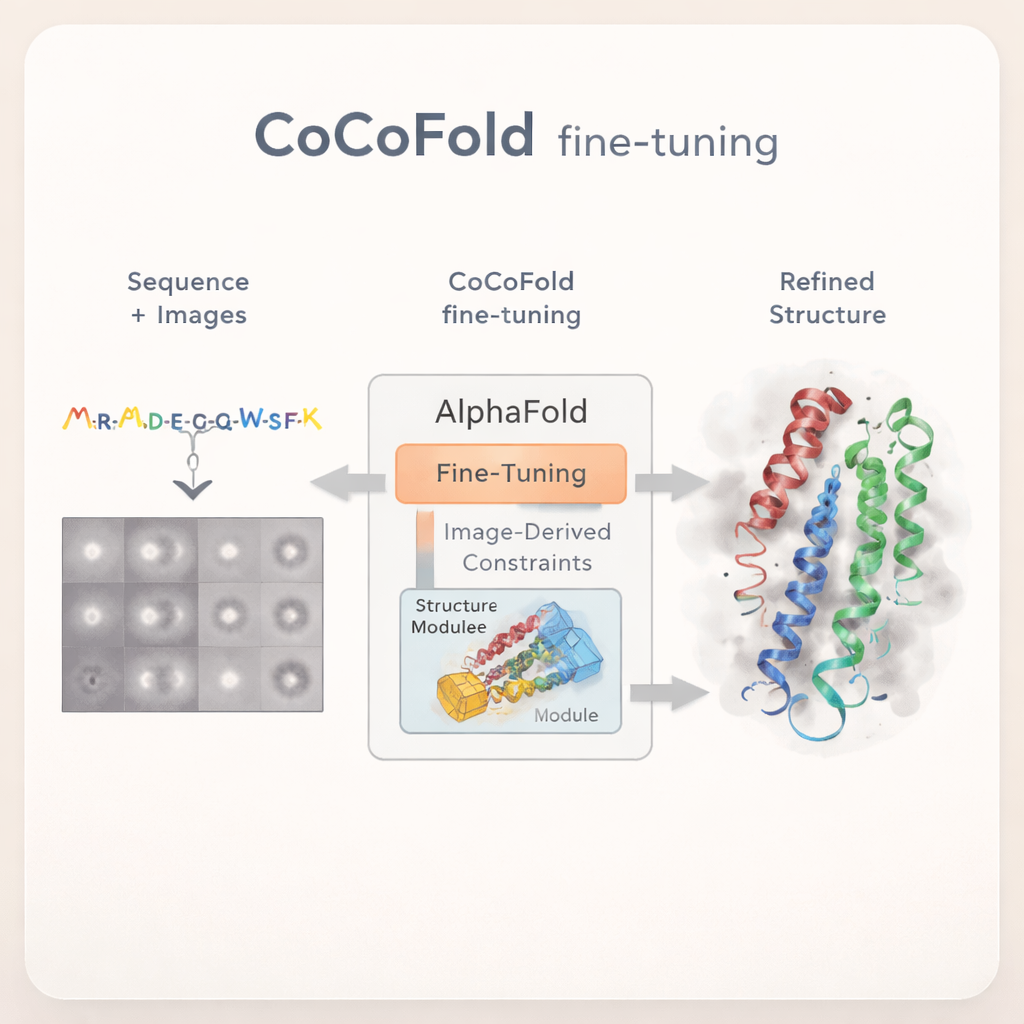
CoCoFoldは別のアプローチを取ります。完全に再構成された3D cryo‑EMマップに頼る代わりに、生の2D粒子画像を直接用いてAlphaFoldをファインチューニングします。手法はAlphaFold‑Multimerの予測から始め、ネットワークの大部分を固定したままにして、タンパク質折りたたみについての広範な知識を保持します。変化を許されるのは最終的な構造生成部分のみです。軽量の“アダプタ”を追加して、cryo‑EM画像から得られた情報をこの構造モジュールに供給し、実験データと整合する形状へと穏やかにモデルを導きつつ、既知のタンパク質物理から大きく逸脱しないようにします。
画像を構造的フィードバックに変える
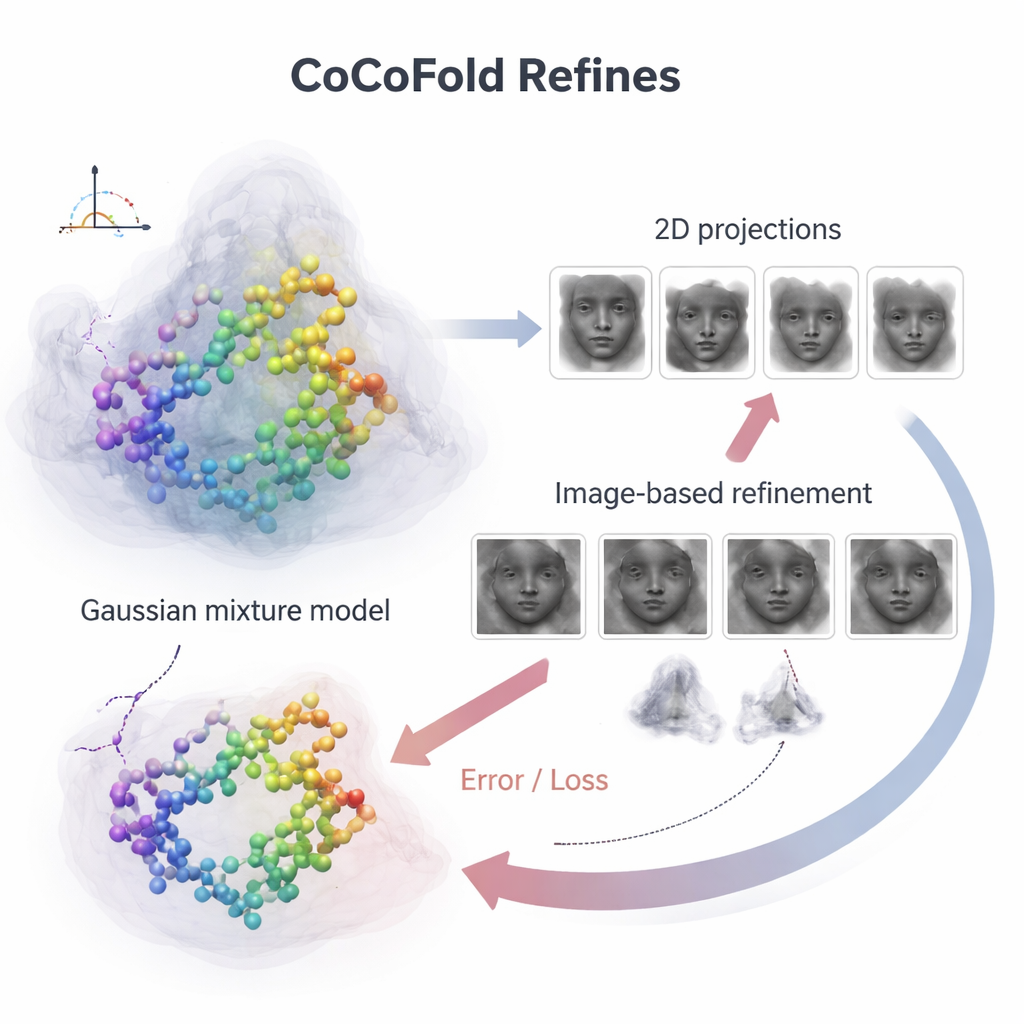
個々の原子をノイズの多い顕微鏡画像に結びつけるため、CoCoFoldは予測構造を重なり合う三次元ブロブ(ガウス混合)で滑らかかつ柔軟に表現します。この表現から、実際の実験と同じ視点や撮像条件で顕微鏡がタンパク質をどのように見えるかをシミュレートします。これらのシミュレートしたスナップショットは、実際のcryo‑EM粒子と周波数領域でリングごとに比較され、どれだけ一致するかが評価されます。不一致はフィードバック信号となりネットワークへ還流し、モデルと密度表現の両方をわずかに調整します。訓練後、原子モデルは局所的な幾何学的衝突を除去するために物理ベースの精緻化ステップでさらに洗練されます。
データが乏しいか偏っているときにも正確さを保つ
著者らは、粒子数が少ない場合と視角に大きな欠損がある場合というcryo‑EMの主要な二つの問題を模した実験およびシミュレーションデータセットでCoCoFoldを検証しました。こうした厳しい条件下で、再構成マップに依存する既存の標準ツールや他の深層学習法は、タンパク質の領域を見落としたり、ヘリックスを誤置したり、マップがぼやけるにつれて微細な詳細を失う傾向がありました。これに対してCoCoFoldは、既知の参照構造により近く、かつより完全なモデルを一貫して生成しました。粒子数が大幅に減少した場合や大きな視角コーンが欠けている場合でも誤差は小さく、これは生の画像から直接学習することで、マップベースの手法が捨ててしまう重要な情報が保持されることを示唆しています。
今後の構造生物学にとっての意味
専門外の読者に向けた要点は、CoCoFoldが強力なAI予測と不完全な実験データの間の翻訳者として働くことです。AlphaFoldかcryo‑EMのどちらか一方を盲目的に信頼するのではなく、特に実験が部分的な視点しか与えない難しい状況で、双方が互いに情報を補完し合えるようにします。豊富で高品質なデータがある単純なケースでは、既存のマップ駆動型ツールが依然として非常に有効です。しかし、粒子が稀であったり向きが欠けたりする――頻繁に起こる一過性や壊れやすいタンパク質状態の追跡では――CoCoFoldは本来捨てられてしまう情報から信頼できる原子モデルを回復する手段を提供します。
引用: Liao, J., Zheng, D., Zhang, H. et al. Fine-tuning AlphaFold with limited cryo-EM observations. Commun Chem 9, 95 (2026). https://doi.org/10.1038/s42004-026-01899-7
キーワード: cryo-EM, AlphaFold, タンパク質構造, 深層学習, 構造生物学