Clear Sky Science · ja
ヒト血清トランスフェリンとバナジウム化合物の反応で生じた付加体の初の結晶構造
なぜ血中タンパク質と金属薬が重要なのか
多くの実験的治療薬は金属原子を含み、糖尿病からがんに至る疾病の治療に寄与する可能性があります。しかし、これら金属を含む薬が血流に入ると、体の天然の輸送タンパク質に乗って運ばれる必要があります。本研究は、血中の主要な鉄輸送体であるヒト血清トランスフェリンが、有望なバナジウム化合物とどのように相互作用するかを調べ、金属薬が体内でどのように運ばれるか、またより安全で効果的な治療へと最適化できる可能性について光を当てます。
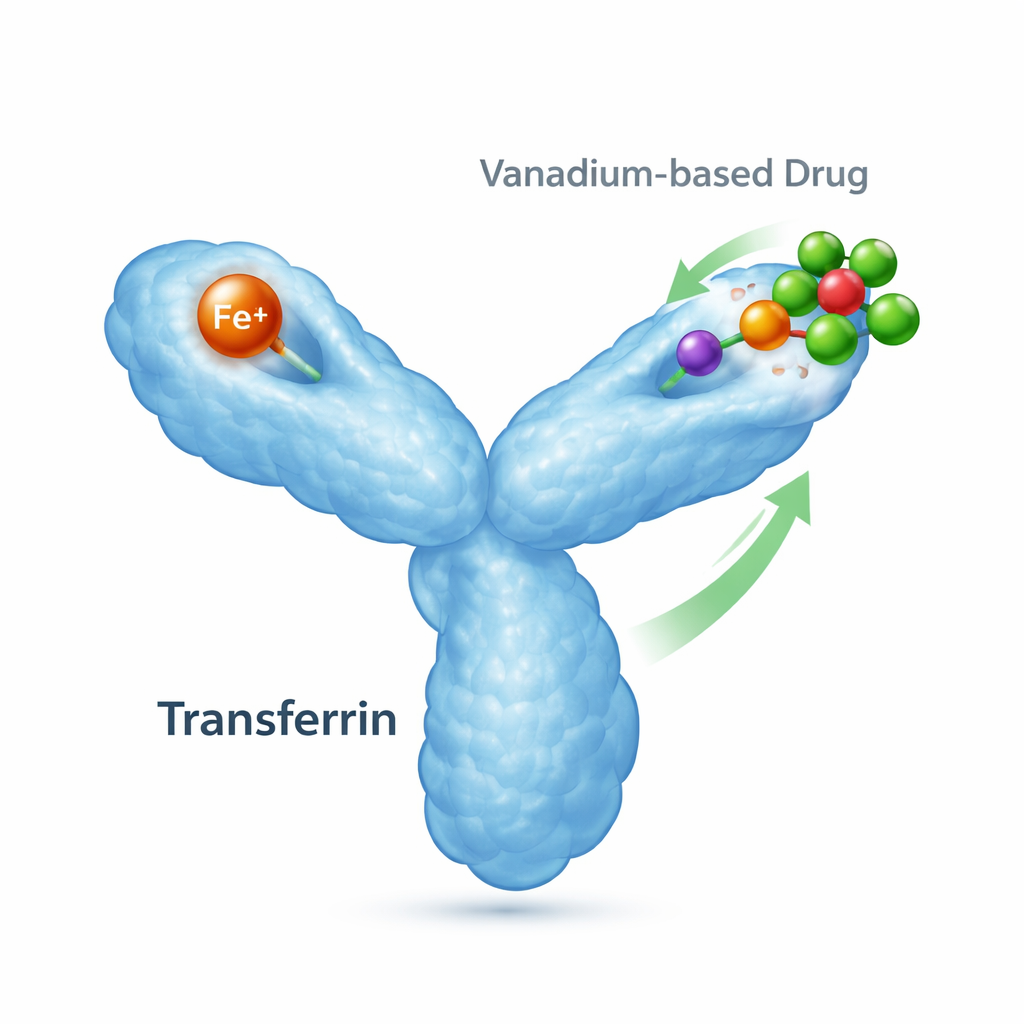
体内の鉄の運び屋とその副次的役割
トランスフェリンは約80キロダルトンのタンパク質で、主な役割は鉄を捕えてそれを必要とする細胞へ届けることです。二つの「ローブ」をもち、それぞれが一つの鉄イオンを結合できます。鉄の有無に応じて形を変え、鉄が結合するとローブは閉じ、鉄がないと開いた状態のままです。細胞表面の特異的受容体はこれらの鉄を含む形を認識して取り込み、トランスフェリンは鉄の恒常性と細胞の健康にとって中心的な存在です。しかしトランスフェリンは医療由来を含む他の金属も結合し得るため、金属ベースの薬がどこへ行き、どのように作用するかに影響を及ぼす可能性があります。
トランスフェリン上のバナジウムの形のスナップショット
研究者らは、bis(acetylacetonato)oxovanadium(IV)と呼ばれるよく研究されたバナジウム候補薬(しばしば[VIVO(acac)₂]と表記)に注目しました。以前の研究で、この化合物または水中で派生した種がトランスフェリンに付着し得ることは示されていましたが、その詳細な結合様式は見られていませんでした。X線結晶構造解析を用いて、研究チームはC末端ローブにのみ鉄を持つトランスフェリン(“FeC”型)の高分解能構造を、バナジウム薬処理の前後で得ました。バナジウム処理した結晶では、元の薬そのものではなく、変化したバナジウム–酸素クラスターが鉄を欠くN末端ローブに結合しているのが観察されました。これにより、ヒトのトランスフェリンに付着したバナジウム断片の初の直接的な構造像が得られました。
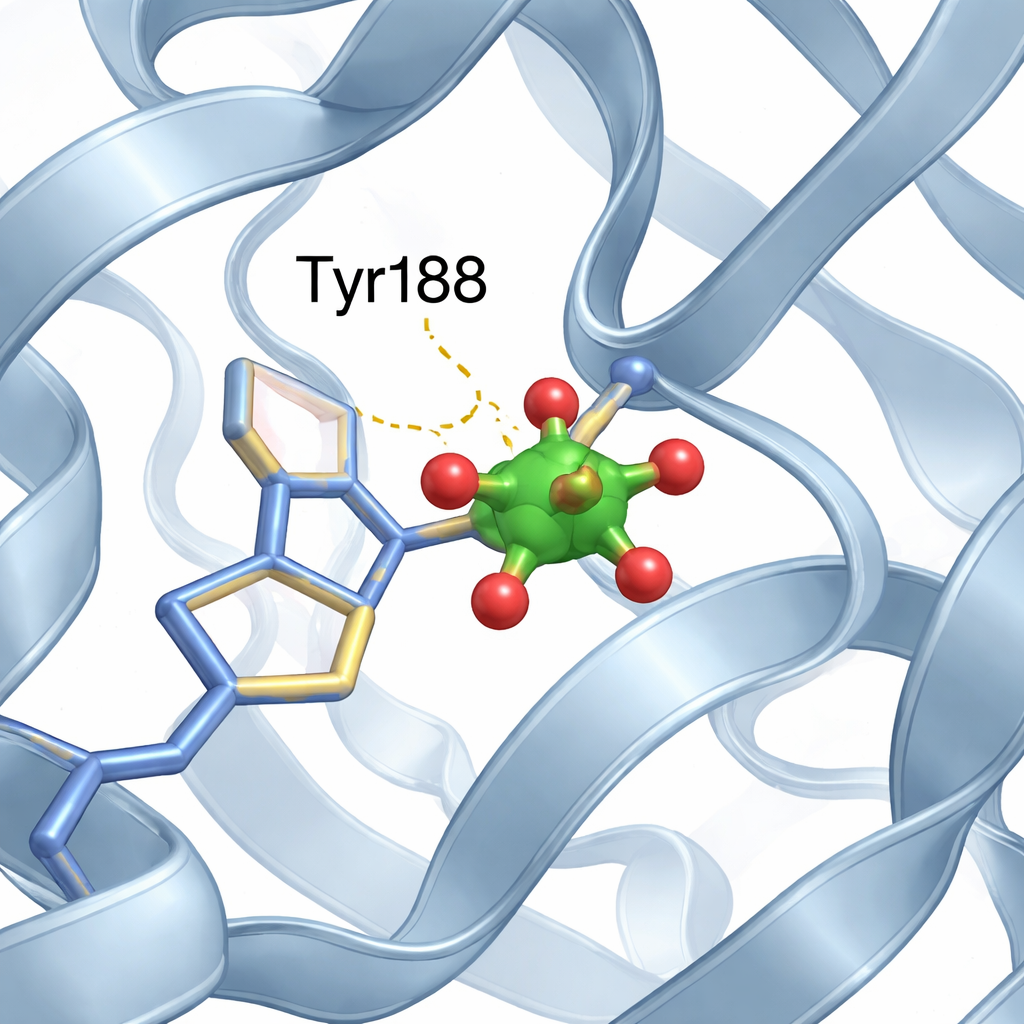
小さなバナジウムクラスターが居場所を見つける
Nローブの鉄結合部位内で、研究チームは二つのバナジウム原子と酸素原子からなる小さなクラスターを同定しました。これは修飾された「ジバナデート」ユニットとして最もよく表現できます。クラスターの酸素の一つは、チロシン188(Tyr188)という特定のアミノ酸の酸素に取って代わられ、タンパク質と金属クラスターの間に直接的な結合を形成していました。さらに、近接するタンパク質領域からの水素結合のような穏やかな相互作用がクラスターを安定化します。重要なのは、この新しい金属来訪者が鉄結合ポケットに入っているにもかかわらず、タンパク質全体は通常の開いたNローブと閉じたCローブの配列をほぼ変わらず維持している点です。バナジウム非存在時の構造とほとんど同一でした。
トランスフェリンがバナジウムの化学をどう変えるか
結晶化に用いられたpHと濃度の溶液中では、結晶で観察された二バナジウム種は通常なら少数派であり、より大きなバナジウム–酸素クラスターが優勢になる傾向があります。分光学的測定と理論的な種分布計算は、元のバナジウム薬が水中でゆっくりと酸化・分解して単純なバナデートイオンを生成し、それがさまざまなクラスターへと集合することを示唆します。結晶構造は、トランスフェリンがより大きなクラスターに比べてこの小さなジバナデート様の断片を選択的に安定化することを示しており、Tyr188でのぴったりした結合部位と支援する水素結合ネットワークを提供することで、混在する溶液中から特定の化学形を“選ぶ”役割を果たしていると考えられます。
細胞受容体との握手を保つ
トランスフェリンは鉄を届けるために細胞表面の受容体に結合する必要があるため、研究者らはこのバナジウムクラスターの付着がその重要な握手を乱すかどうかを調べました。非変性ゲル電気泳動とバイオレイヤー干渉計という感度の高い手法を用いて、バナジウム処理したトランスフェリンが未処理の鉄のみの形と比べてトランスフェリン受容体にどの程度結合するかを測定しました。両者はほぼ同一に振る舞い、非常に強いナノモーラー低濃度領域での結合を示しました。これは、Nローブに収まるバナジウムクラスターが受容体と相互作用する部位のトランスフェリンの形状を大きく変化させず、したがってタンパク質が細胞に認識されるのを妨げないことを裏付けます。
金属ベースの医薬にとっての意味
専門外の方への要点は、本研究がバナジウム薬の派生物が体の主要な鉄の輸送体に付着しても通常の機能を妨げない分子レベルのスナップショットを提供することです。トランスフェリンは鉄部位に特定の小さなバナジウム–酸素クラスターを捕捉し得る一方で、タンパク質の全体構造と受容体結合能は本質的に変わりません。これにより、バナジウム薬がトランスフェリンに結合した状態で循環し得る仕組みが説明され、異なるタンパク質が異なるサイズのバナジウムクラスターを好む可能性が浮き彫りになります。こうした知見は、血流中での挙動(どの形をとるか、どこへ行くか、どれくらいの時間持続するか)を予測・制御できる、より賢明な金属ベース治療薬を設計するために重要です。
引用: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
キーワード: バナジウム薬, ヒト血清トランスフェリン, 金属を基盤とする治療薬, タンパク質–金属結合, 構造生物学