Clear Sky Science · ja
RLRおよびcGAS‑STING自然免疫シグナル伝達経路の動的調節因子としての糖鎖付加
糖のタグが細胞のウイルス検知を助ける仕組み
私たちの細胞は常に侵入するウイルスを監視しており、この防御の大部分はタンパク質に付着した小さな糖のタグに依存しています。本レビューでは、糖鎖付加と呼ばれるこれらの糖タグが、単純なオン/オフスイッチではなく調光器のように主要な抗ウイルス経路を微調整する様子を解説します。この糖に基づく精密な制御を理解することは、ワクチンの強化、ウイルス感染治療、さらにはがんに対する免疫活性化の新しい手法を切り開く可能性があります。
細胞の早期警報システム
ウイルスが細胞に侵入すると、RNAやDNAといった手がかりが残されます。細胞内ではこの遺伝物質を監視する特殊な「警報」システムが働いています。RIG‑I様受容体(RLR)経路はウイルスRNAを検出し、cGAS–STING経路は細胞内の不適切な場所に現れたDNAを感知します。いったん活性化されると、両経路は化学的なカスケードを起動し、最終的にI型インターフェロンや炎症性分子の放出をもたらします。これらは近隣の細胞に警告を発し免疫防御を動員する強力なシグナルです。過剰でも不足でも有害になり得るため、細胞はこれらの警報を慎重に調節する必要があり、糖鎖付加はその主要な調節手段の一つです。 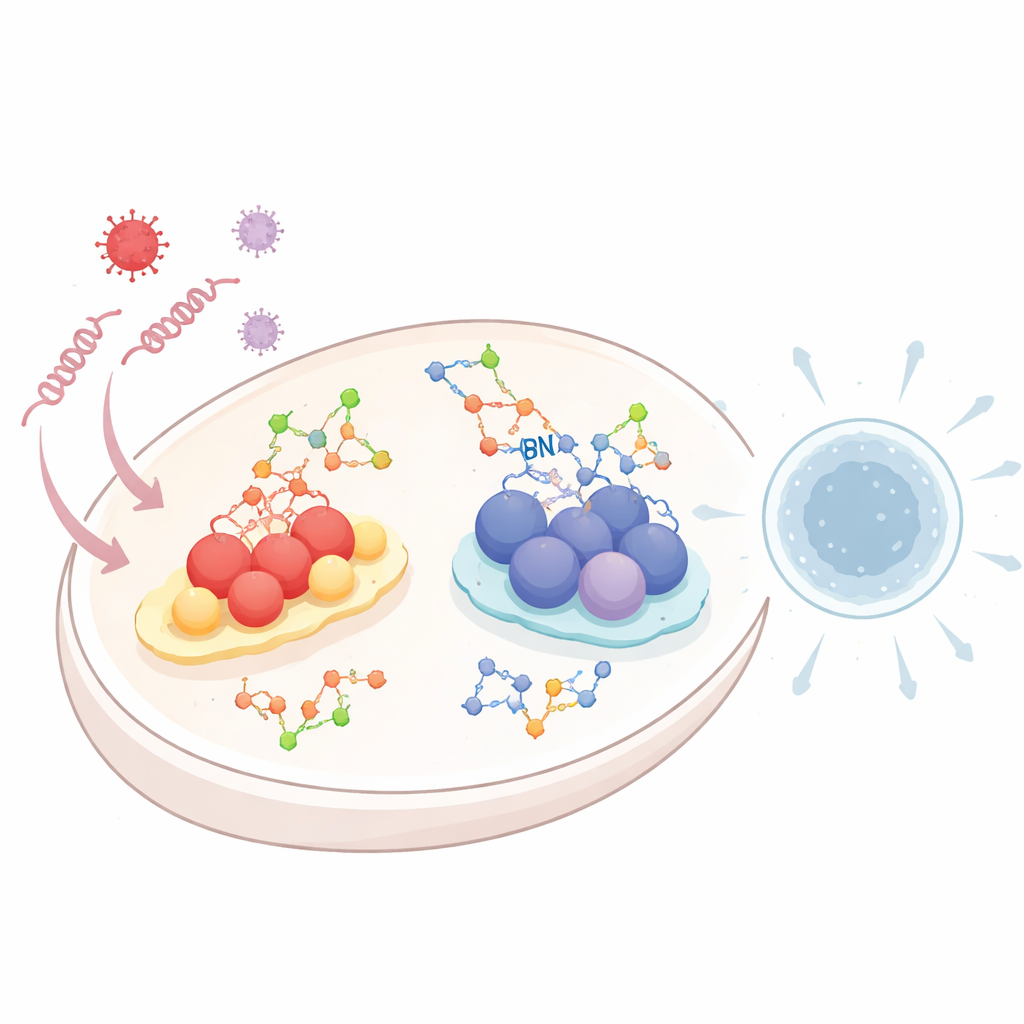
精密な制御装置としての糖被膜
糖鎖付加は、異なる細胞内部位でタンパク質に小さな糖単位を付け加えます。小胞体やゴルジといった細胞の輸送ネットワーク内では、大きなN結合糖鎖がタンパク質の正しい折りたたみ、安定性、適切な膜への輸送を助けます。一方で、O‑GlcNAc化と呼ばれるより簡素な形態は、細胞質や核のタンパク質に単一の糖を付けます。この最小限のタグは非常に動的で、栄養状態やストレスに応答して二つの酵素によって迅速に付加・除去されます。本レビューは、これら異なる糖の種類が免疫センサーを単純にオン/オフするのではなく、センサーの集積しやすさ、寿命、シグナル強度を調整することで機能することを示します。こうして糖鎖付加は細胞の代謝状態を感染に対する備えに直接結びつけます。
RNAセンサー経路の微調整
RNA検知を担うRLR系の中心的中継タンパク質であるMAVSはミトコンドリア上に局在し、重要なハブとして働きます。レビューは、MAVSへのO‑GlcNAc化が糖の付く位置によって抗ウイルスシグナルを促進したり抑制したりできることを示しています。特定の部位に付く糖タグは、特定のユビキチン鎖のようなさらなる修飾を促進し、MAVSが大規模なシグナルクラスターを形成してRNAウイルスに対する強いインターフェロン産生を駆動するのを助けます。別の部位の糖は、通常時にMAVSを分散・不活性に保ち、不必要な炎症を防ぎます。ウイルス感染や細胞の糖産生代謝経路の変化は、これらの活性化的および抑制的なタグのバランスを変化させます。IRF5など他の因子に対する関連修飾は、免疫系を有害な「サイトカインストーム」へ傾けることがあり、糖が多ければ良いというわけではないことを示しています。同時に、ウイルスはEGFRのような細胞表面タンパク質のN結合糖を利用して、上流のセンサーであるRIG‑Iを分解へ導き、抗ウイルス防御を鈍らせることがあります。
DNAセンサー経路の微調整
DNA検出を担うcGAS–STING経路も糖鎖付加によって強く影響を受けます。小胞体に局在する膜タンパク質STINGは、正しく折りたたまれ安定に存在し、DNA由来のメッセンジャーによって活性化された後にシグナルクラスターを組み立てるためにN結合糖鎖を必要とします。これらの糖がなければ、STINGは高次構造を形成せず、細胞区画を経由した適切な輸送を行えず、強力なインターフェロン放出が阻害されます。同時に、STINGの特定部位のO‑GlcNAc化は別種の化学的修飾を高め、クラスタリングと移動を促進してDNAウイルスに対する抗ウイルスシグナルを増幅します。ゴルジで構築される硫酸化グリコサミノグリカンと呼ばれる糖鎖は、活性化されたSTINGが長い重合体を形成し下流の酵素を呼び込むのをさらに助けます。ウイルスは自らの糖タンパク質を変化させたり、STINGを標的とする分解経路を活性化したりして反撃し、これらの糖修飾が付加・処理されるのと同じ細胞内空間で干渉することが多いです。 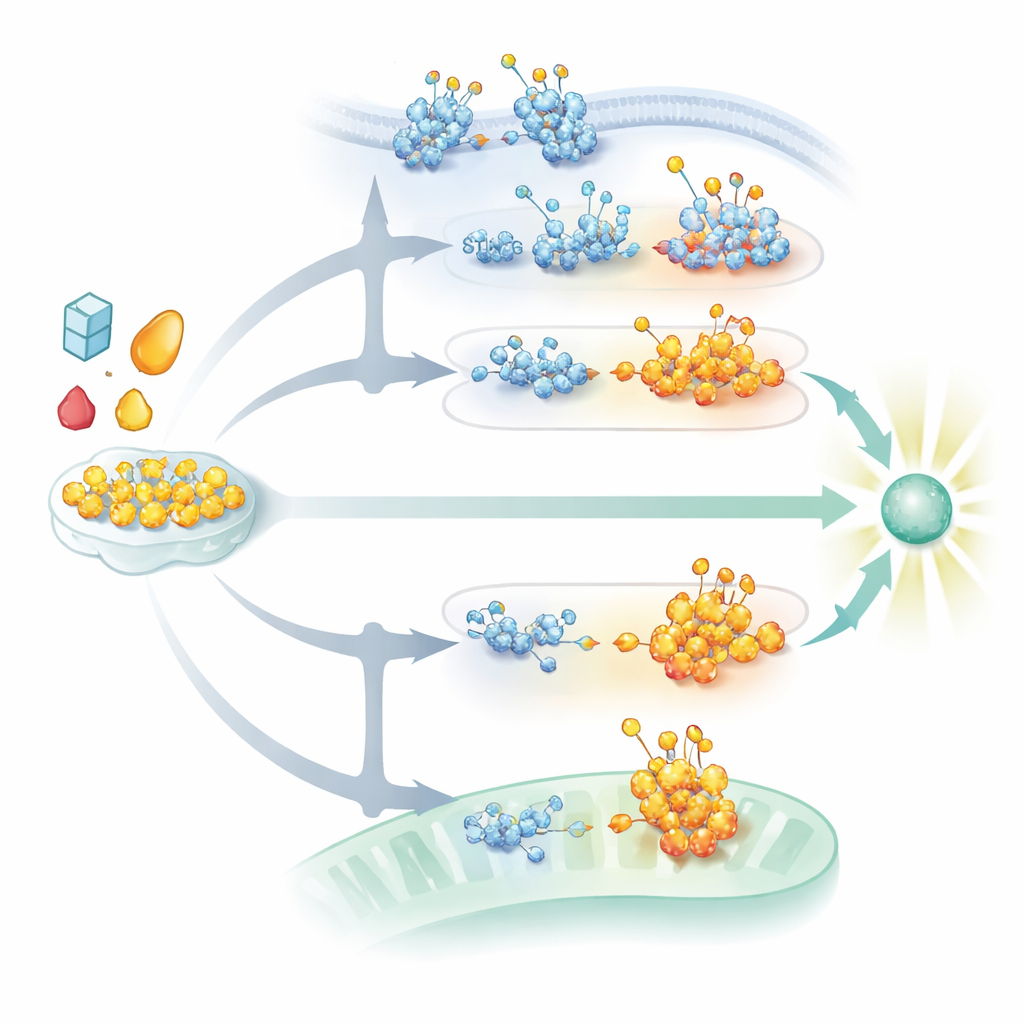
代謝、疾患、将来の治療法
O‑GlcNAc化の主要な糖供与体はヘキソサミン生合成経路という代謝経路で作られるため、栄養利用の変化は抗ウイルスシグナルに直接影響します。多くのウイルスはこの経路を自らに有利に働かせ、一方で実験的にヘキソサミン流を増強または阻害すると動物モデルで抗ウイルス応答が強まったり弱まったりします。レビューはこれらの機構をヒト疾患に結びつけます:腫瘍はしばしば糖鎖付加を再配線してインターフェロン信号を弱め、免疫から逃避します。慢性的な代謝ストレスや糖鎖処理の遺伝的欠損は有害な自己免疫へ傾けることがあります。著者らは、糖鎖付加を制御する酵素—特にO‑GlcNAcを付け外しするものや重要なN結合構造を作るもの—が有望だが困難な薬剤標的であると論じています。将来の治療は部位特異的かつ状況に配慮した作用を必要とし、感染、がん、炎症性疾患に対する保護を高めつつ新たな免疫バランスの乱れを引き起こさないように「グリココード」をそっと調整することが求められるでしょう。
日常の健康における大局観
日常的な観点から見ると、本稿は身体の最前線の抗ウイルス警報が孤立して動作するのではなく、細胞のエネルギー利用と糖化学に結び付いていることを明らかにします。ごく少数の重要なタンパク質に付く小さな糖タグが、逸脱したウイルスゲノムが穏やかな警告を引き起こすか、本格的な防御を招くか、あるいは危険な過剰反応を引き起こすかを決めます。この糖に基づく制御システムを解読し最終的に調整することを学べば、研究者はワクチンをより効果的にし、しつこい感染を排除し、腫瘍を免疫系にさらし、自己免疫疾患の暴走する炎症を鎮める治療法を設計できることが期待されます。
引用: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
キーワード: 自然免疫, 糖鎖付加, RLR経路, cGAS‑STING, O‑GlcNAc化