Clear Sky Science · ja
増殖速度駆動のモデルは表現型適応がBRAFV600E変異メラノーマの薬剤耐性を駆動することを示唆する
薬に適応して生き延びるがん細胞
標的薬は深刻な皮膚がんであるメラノーマの治療を大きく変えました。しかしこれらの薬はほとんど常に効かなくなります:一度縮小した腫瘍が再び成長し始めます。本研究は単純だが重要な問いを投げかけます。遺伝的変異だけに頼るのではなく、メラノーマ細胞は挙動を変えることで治療に「学習」して生き延びられるのか――そしてその学習が、ある投薬法が他より有効に見える理由を説明しうるのか?
感受性のある細胞から生存者へ
研究者たちは、BRAFという遺伝子に一般的な変化を持ち、この変化によりBRAF阻害薬に特に感受性を示すメラノーマ細胞に着目しました。以前の実験では、これらの細胞が異なる用量と異なる曝露時間で阻害薬エンコラフェニブにさらされました。各条件下で細胞がどれほど速く増殖するか、あるいは死ぬかを注意深く測定することで、著者らは細胞を大きく二つのカテゴリに分けました:薬を未経験の「薬感受性(drug-naive)」細胞と、少なくとも1週間薬環境にいた「薬適応(drug-adapted)」細胞です。薬未経験の細胞は治療なしではよく増殖する一方、薬によって強く抑えられるか死にます。これに対し薬適応細胞は薬存在下でよりよく増えるが、薬を除くとその利点を失います—これは生存が恒久的な遺伝子変化ではなく、可逆的で柔軟な状態変化に結びついていることを示唆します。
隠れた細胞挙動の地図
これらの変化を理解するために、研究チームは各がん細胞に「表現型状態」を割り当てる数理モデルを構築しました—非常に薬に敏感な状態から非常に薬剤耐性のある状態までの抽象的な位置を示す尺度です。二種類の細胞だけを仮定する代わりに、多くの中間状態を許容し、抵抗性の生物学的マーカーで観察される漸進的変化を反映しました。各状態と薬用量の組み合わせについて、正の純増殖率(分裂が細胞死を上回る)か負の純増殖率(細胞死が分裂を上回る)かを推定しました。これらの率はすべて格子状に配列され、「フィットネスマトリックス」として風景のように機能します:ある状態とある用量の組み合わせは細胞にとって繁栄する良い場所であり、別の組み合わせは致命的です。モデル内の細胞は治療のオン・オフに応じてこの地形を一歩ずつ移動できます。
細胞は有利な方向へ漂うのか登るのか?
鍵となる未知は、細胞がこの地形をどう移動するかでした。著者らは4つの可能な戦略を検討しました。ひとつは細胞が状態を変えない戦略で、この場合は最初から耐性細胞が存在しなければなりません。別の戦略では細胞は隣接する状態間をランダムにさまよい(泥酔者の散歩のように)、状況が改善するかどうかに関係なく移動します。残る二つの戦略では、細胞は自身の増殖率がより高くなる状態に向かって移動する傾向があり—ひとつは誤差を伴うノイズのある移動、もうひとつは常により良い生存へ強く登る移動です。チームがコンピュータシミュレーションを行い、特に薬を連続投与する場合と一週オン・一週オフのような断続的投与の場合の実験データと比較したところ、観察された結果を再現できたのは細胞がより高いフィットネスへ登る戦略だけでした:高用量の断続的投与は、同じ総投与時間で総薬量が多い連続投与よりも細胞数を抑えることができました。
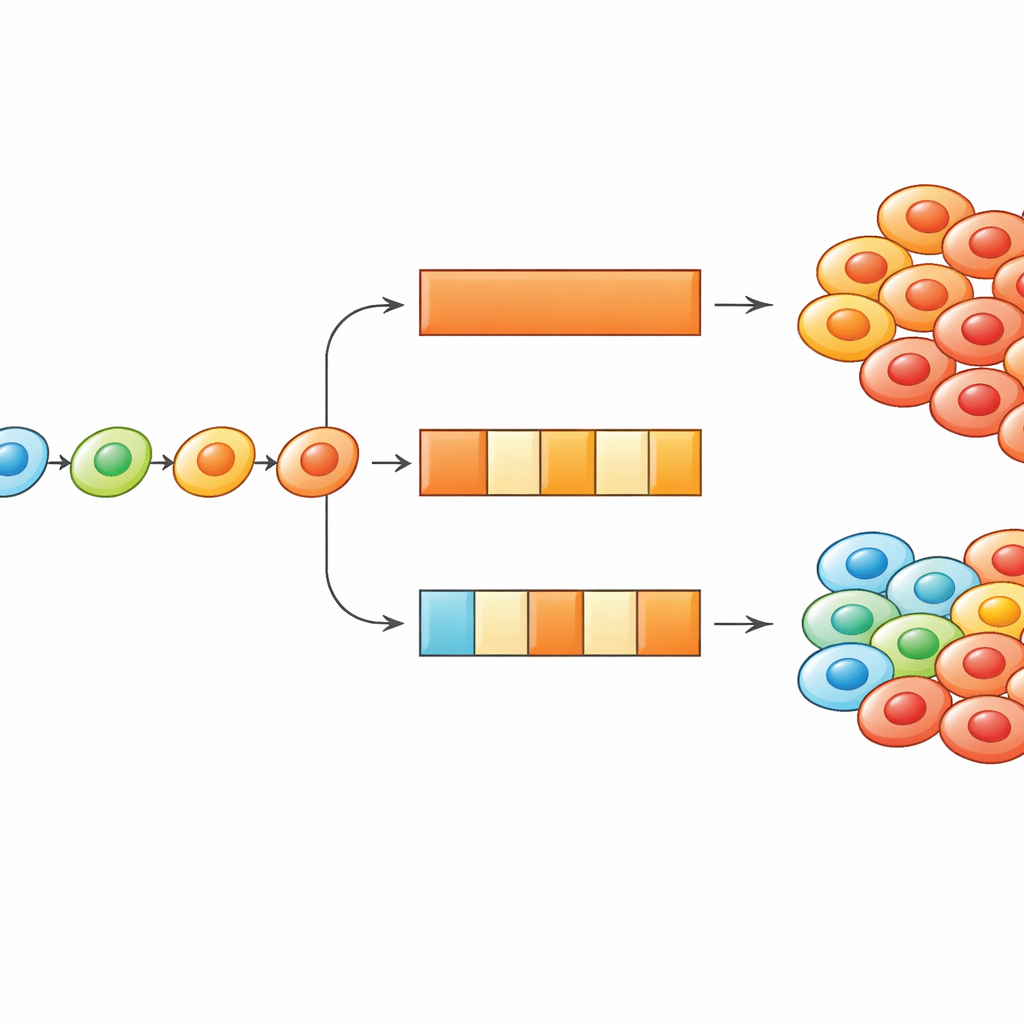
断続投与で適応をがんに不利に利用する
さらに掘り下げて、研究者たちはシミュレーションと単純化した方程式の両方を用いて、細胞が状態を変えられる頻度や薬オン・オフ期間の長さを探りました。細胞が指向性を持って適応する場合、治療スケジュールはこの適応を遅らせるか、逆に利用するように調整できることがわかりました。細胞が状態を更新できる頻度を短くする――概念的には表現型変化を可能にする生物学的機構を遅らせる――と、断続投与はより強力になる傾向があります。なぜなら細胞はすぐに高度に耐性のある状態へ登れなくなるからです。逆に、もし細胞が初めから強い耐性状態にあるなら、薬の休止期間は彼らがより感受性の高い状態へ戻る時間を与え、薬を再導入したときに細胞死の急増を引き起こします。本研究は投薬のタイミングと細胞適応の速度が組み合わさって、どのスケジュールが最適かを決めることを示しています。
将来のがん医療にとっての意味
一般の読者にとって中心的なメッセージは、がん細胞は単なる固定された敵ではなく、形を変える存在だということです。このメラノーマ系では、細胞は直面する条件下で増殖に有利な挙動へ積極的に向かうように見えます。著者らのモデルは、異なる恒久的なクローンを仮定しなくとも、この指向性を持つ適応だけで、断続投与が一定投与よりも有利に働く理由を説明しうることを示唆します。これらの結果は培養細胞から得られたものであり、患者治療に直接応用するにはさらなる作業が必要ですが、このアプローチは実用的な枠組みを提供します:がん細胞がどれくらいの速さで、どの方向に適応するかを測定することで、医師は腫瘍を攻撃するだけでなく、その表現型の「学習」を逃走経路ではなく行き止まりに導く投薬スケジュールを設計できる可能性があります。
引用: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
キーワード: メラノーマ, 薬剤耐性, 細胞可塑性, 断続的療法, 数理モデル