Clear Sky Science · ja
二量体化による淋菌(Neisseria meningitidis)キノール依存性一酸化窒素還元酵素の活性化の構造基盤
細菌はどのように免疫防御を出し抜くか
有害な細菌が体内に侵入すると、免疫細胞は一酸化窒素のような毒性分子を放出してそれらを殺そうとします。しかし一部の病原体はこの攻撃を無効化して生き延びる分子トリックを進化させてきました。本研究は、主要な細菌酵素がどのように二量体へと再構成されることで一酸化窒素の解毒能力を大幅に高めるかを原子レベルで明らかにし、この形状変化を理解することが新たな抗生物質設計への道を開く理由を示します。
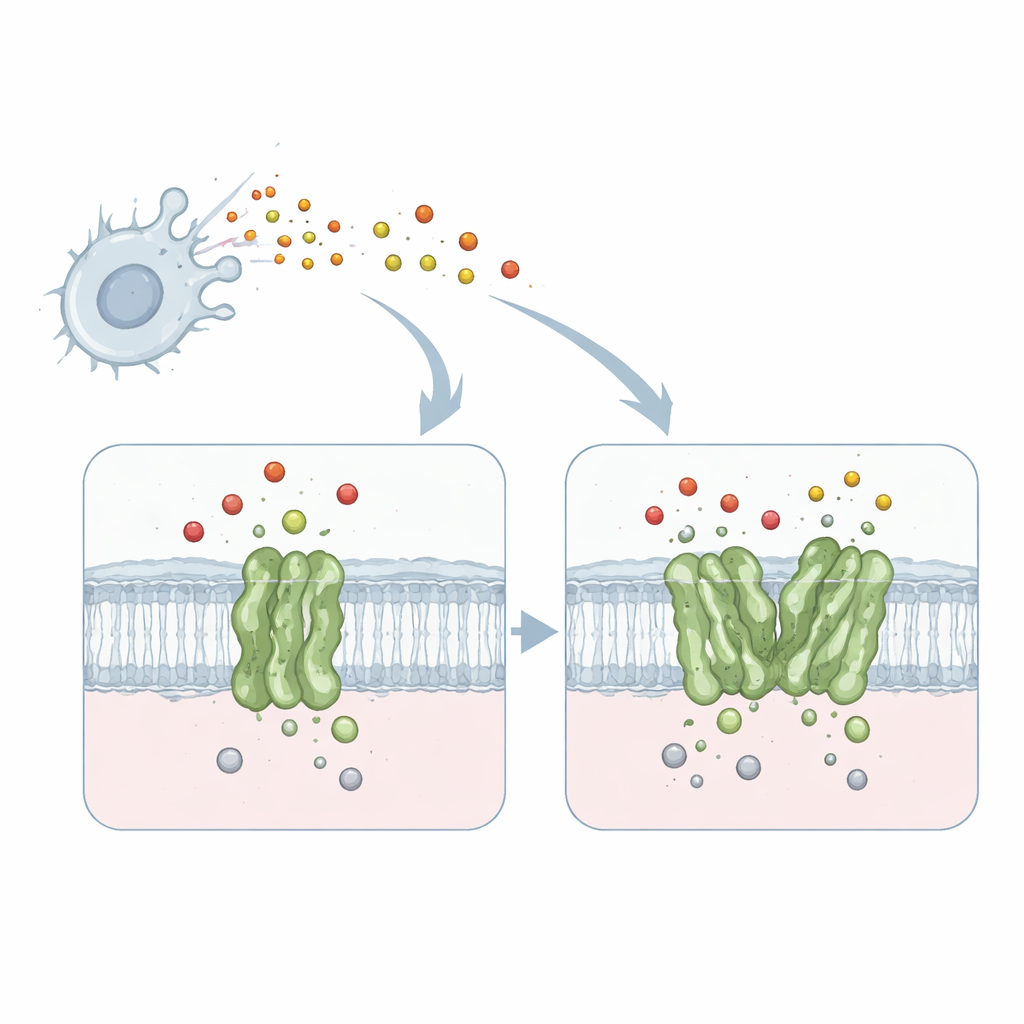
毒性ガスを無力化する小さな機械
本研究は髄膜炎を引き起こす細菌Neisseria meningitidis由来のキノール依存性一酸化窒素還元酵素(qNOR)という膜タンパク質に焦点を当てています。qNORは細菌の細胞膜に存在し、免疫系が産生する毒性の高い一酸化窒素をより無害な生成物へと変換します。この解毒により、微生物はヒトマクロファージのような敵対的環境下でも呼吸と増殖を続けられます。呼吸と一酸化窒素除去が病原体の生存に不可欠であることから、qNORは新規抗菌薬の魅力的な標的となります。
一つでも良いが二つならなお良し
以前の生化学的研究は、qNORが単量体(モノマー)または二量体(ダイマー)として存在し得ること、そして二量体のほうが一酸化窒素を中和する速度が2〜4倍速いことを示していました。なぜ同じ酵素を単に二つ並べるだけでこれほど性能が向上するのかは不明でした。この疑問に答えるため、研究者らは高分解能単粒子クライオ電子顕微鏡を用いて同一菌株由来のモノマー型とダイマー型qNORの詳細な三次元構造を取得しました。得られた解像度はほぼ原子レベルで、ダイマーが1.89オングストローム、モノマーが2.25オングストロームと、個々のアミノ酸側鎖、金属イオン、そして多数の水分子を特定できるほど鮮明でした。
柔軟なヘリックスが安定化のブレースに変わる
驚くべきことに、酵素の触媒中心—一酸化窒素が変換される金属中心—は両形態でほとんど同一に見えました。むしろ、重要な差異はやや離れた位置にあり、膜貫通ヘリックスTM10と、二つのqNORがペアになる際にTM10が別のヘリックス(TM2)とどのように接触するかに現れていました。モノマーではTM10は緩く固定されており、大きく揺れ曲がることができるとクライオEMデータの計算解析が示しました。ダイマーでは各パートナー由来のTM10が互いにロックして四本のヘリックス束を形成し、その運動が大幅に制限されます。この安定化により重要なアミノ酸であるグルタミン酸残基Glu563の位置が微妙に移動し、活性部位近傍の別のグルタミン酸Glu494に近づいて、反応に必要なプロトンの入り口となる経路がより集中的に整えられます。
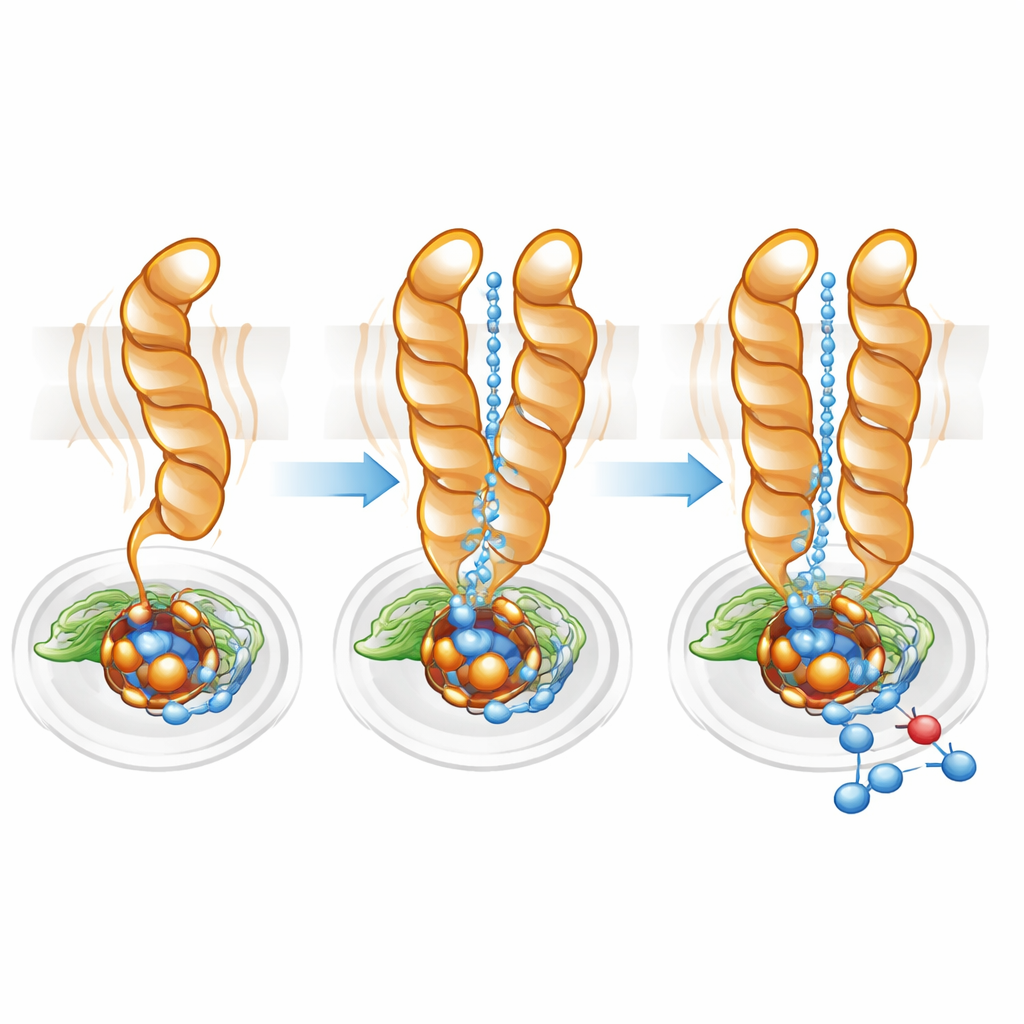
プロトン経路の微調整
プロトン(正に帯電した水素イオン)は、一酸化窒素還元反応が進行するために細胞内部から埋もれた活性部位へ効率よく運ばれる必要があります。経路マッピングソフトを用いた解析で、研究チームはモノマーとダイマーの両方に細胞質と活性部位をつなぐ親水性空洞を見出しました。しかしモノマーではこのチャネルはより広く拡散しており、TM10の高い可動性と一致します。ダイマーではTM10の固定された位置とGlu563の好ましい配向が、より直接的で整理された経路を定義するのに寄与していました。Glu563を同様の相互作用を形成できないアミノ酸に変異させると酵素活性は通常の10%未満に激減し、同時にダイマーの安定性も損なわれました。関連する位置での変異は活性部位に必須の非ヘム鉄の量を減少させました。これらの結果は、二量体形成とGlu563およびGlu494の精密な配置が構造的完全性と触媒効率の両方に密接に結び付いていることを示しています。
構造的知見を新治療へつなげる
本研究は、膜表面でのタンパク質の対合から活性部位深部での微細な調整へと至る明確な系を明らかにし、それがqNORの一酸化窒素除去効率を制御していることを示しています。簡潔に言えば、酵素の二つのコピーが結合すると、柔軟な領域がまっすぐになり硬化してプロトンを反応中心へ導く役割を果たし、酵素出力を高めます。創薬の観点では、活性部位を直接阻害するのではなく、二量体を引き離すかGlu563–Glu494相互作用を乱す分子を設計して酵素を遅いモノマー状態へと追い込むという非従来型の戦略が示唆されます。qNORや類似酵素は複数の危険で薬剤耐性のある病原体の生存に重要であるため、このような構造に基づくアプローチは次世代の標的型抗菌薬の開発に寄与する可能性があります。
引用: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
キーワード: 一酸化窒素の解毒, 細菌の呼吸, 膜タンパク質酵素, クライオ電子顕微鏡法, 抗菌薬ターゲット