Clear Sky Science · ja
NRF2活性化薬と核外輸送阻害剤セリネキソールは、NRF2非依存的機構を介してACE2、TMPRSS2、XPO1を含むネットワークを標的にしコロナウイルスを抑制する
細胞に“ノー”と言わせる薬
現在の多くのコロナウイルス治療はウイルス自体を標的にします。しかしウイルスは変異しやすく、新たな変異株がこれらの薬剤の効果を素早く弱めることがあります。本研究は別の戦略を検討します。すなわち、危険なSARS-CoV-2や季節性の弱い株に対して、私たち自身の細胞を感染に対してより受け入れにくくする方法です。細胞がいくつかの重要な門番タンパク質をどのように扱うかを調節することで、研究者らは既存の低分子化合物が実験室モデルで感染を大幅に減らせることを示しており、その作用は当初有名になった通常の抗ウイルス経路に依存しないことがわかりました。
コロナウイルス防御への新たな視点
研究チームは、NRF2というタンパク質が制御する細胞保護プログラムを活性化することで知られる化合物に注目しました。これらの化合物—4-オクチルイタコネート(4OI)、バルドキソロン(BARD)、およびスルフォラファン(SFN)—は、核外へタンパク質を輸送する蛋白質XPO1を阻害する薬剤セリネキソール(SEL)とともに試験されました。肺および腎臓細胞モデルでは、これら4剤はいずれも細胞を傷つけることなくSARS-CoV-2量を低下させ、複数の懸念変異株に対しても有効でした。驚くべきことに、NRF2を遺伝学的に欠失させるとウイルスはむしろ増殖しやすくなり、NRF2が本来は防御的であることが示されましたが、それでも薬剤はよく効き続け、彼らの抗ウイルス作用が別の経路から来ていることが明らかになりました。 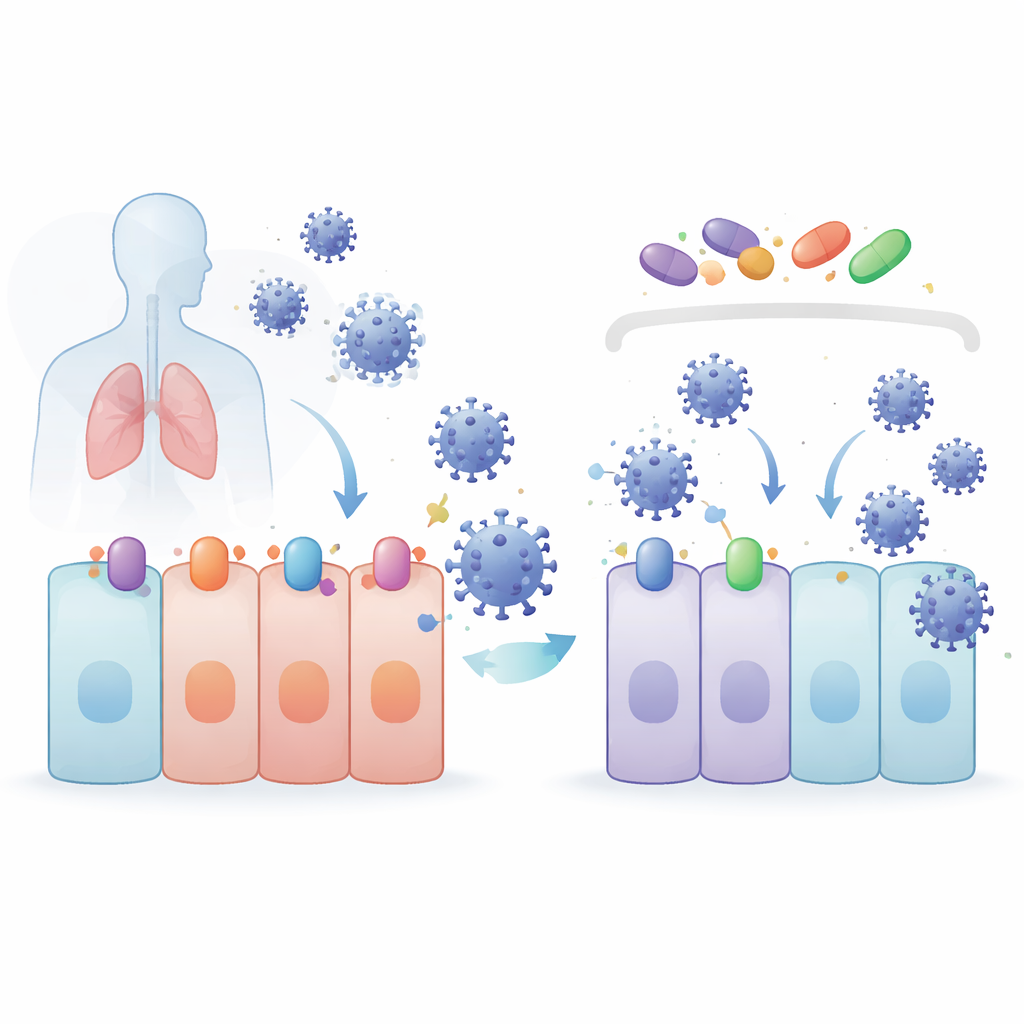
ウイルスの玄関を封鎖する
コロナウイルスは細胞表面の受容体タンパク質に結合して感染を始めます。SARS-CoV-2やその近縁種にとって主要な玄関はACE2であり、切断酵素のTMPRSS2が補助します。輸出蛋白XPO1も感染を助けるように見えます。研究者らは、4OI、BARD、SFN、SELのいずれもヒト肺細胞におけるACE2、TMPRSS2、XPO1の量を低下させることを見出しました。4OIとSELは特に感染前に存在すると強力で、コロナウイルスのスパイクタンパク質で包まれたウイルス様粒子の侵入を阻止しました。言い換えれば、これらの薬はウイルスが内部に入ってから遅らせるだけでなく、ウイルスが最初に扉を開けるために必要とする錠や取っ手を取り除く手助けをします。
細胞が主要なウイルス補助因子を分解する仕組み
さらに掘り下げると、チームは4OIがACE2タンパク質の分解を促進することを示しました。通常の条件ではACE2は数時間持続しますが、4OIがあると細胞表面から数分の一の時間で消失しました。この破壊にはNEDD4LとMDM2という二つの細胞内タグ付け酵素が必要で、これらはタンパク質に分解指示の分子タグを付けます。これらのタグ付け酵素を阻害すると4OIによるACE2除去能力は弱まりました。驚いたことに、通常のタンパク質分解装置であるプロテアソームは主要な経路ではありませんでした。代わりにACE2は細胞のリサイクルと廃棄システムであるリソソームに流されました。これらの薬はまた、STAT3という通常ACE2遺伝子の発現を高めるタンパク質の活性化を低下させることで、ACE2およびXPO1の遺伝子発現も低下させました。 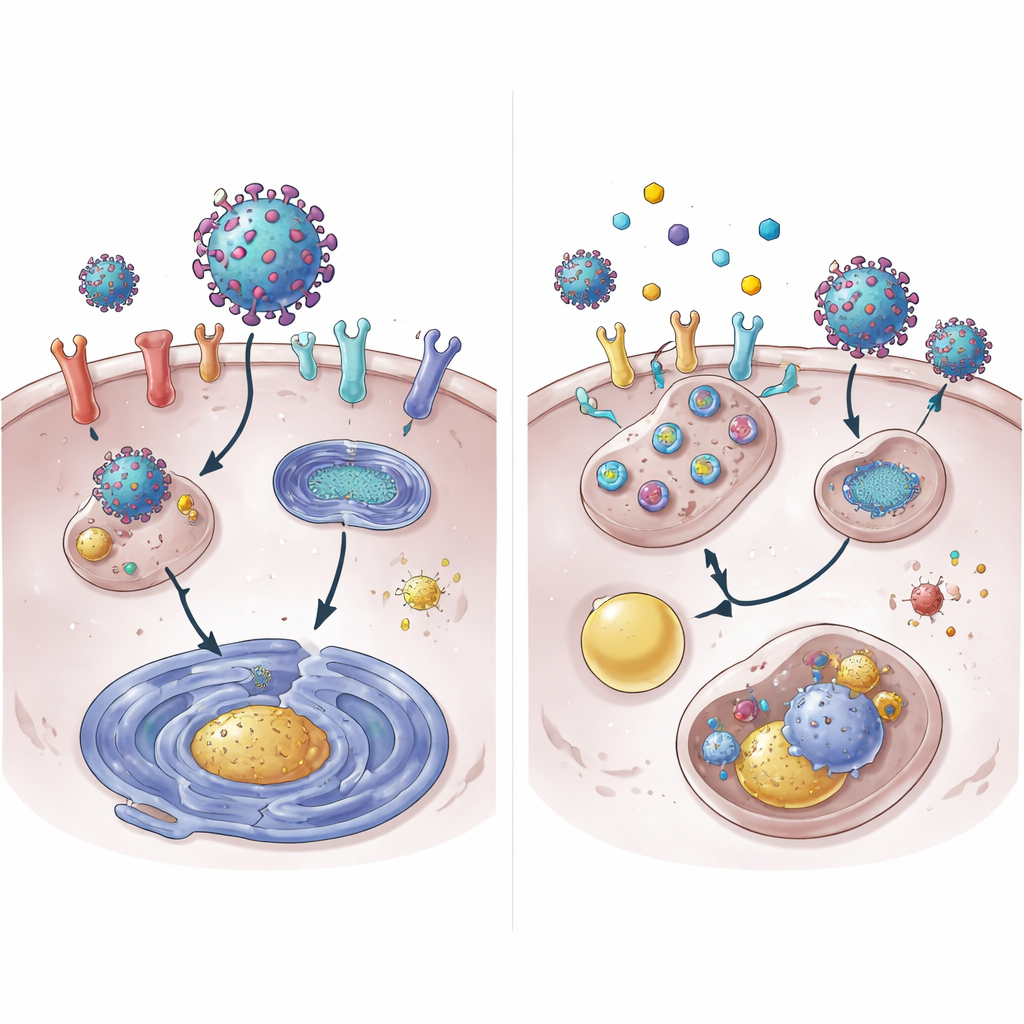
季節性コロナとXPO1の関連
次に科学者たちは、通常は軽い風邪を引き起こすが免疫不全の人では危険になり得る季節性コロナウイルスhCoV-229Eに着目しました。複製時に発光するように改変したウイルスを用いて、4剤はいずれも肺細胞や血管内皮細胞で229Eを強く抑制することを示し、これはNRF2が欠如していても同様でした。SARS-CoV-2とは異なり、このウイルスは別の受容体ANPEPを用いますが、薬剤はANPEPを変化させませんでした。代わりに、薬剤の効果はXPO1をどれだけ強く減少させるかと密接に一致しました。XPO1自体をノックダウンすると229Eの複製は大きく低下し、XPO1が乏しい細胞ではセリネキソールの効果はほとんど消えました。SELが最もXPO1依存で、BARDが最も依存度が低いという序列は、各化合物がわずかに異なる標的の組み合わせを持ちつつ、XPO1が多くの抗ウイルス作用の中心的ハブであることを示唆します。
将来の治療に向けての意味
専門外の方への要点は、ウイルスを直接攻撃するだけでなく、私たちの細胞を穏やかに再配線して感染しにくくすることでコロナウイルスに対抗することが可能である、ということです。培養ヒト細胞では、研究対象の化合物がSARS-CoV-2や一般的な風邪ウイルスが頼る重要な結合部位や補助経路を剥ぎ取り、これを主に当初注目されたNRF2経路に依存せずに行いました。これらの知見はまだ前臨床段階であり、すぐに医薬品へ直結するものではありませんが、ACE2、TMPRSS2、XPO1のような共通の宿主タンパク質ネットワークを標的にしてウイルス侵入を同時に低下させ、有害な炎症を抑え、組織を保護するという有望な道を示しています。
引用: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
キーワード: 宿主指向型抗ウイルス薬, コロナウイルスの侵入, ACE2とTMPRSS2, NRF2活性化剤, XPO1阻害