Clear Sky Science · ja
マウス視床下部視交叉上核におけるAVP受容体シグナル伝達の基盤となるVIPおよびGRPニューロンのヘテロ接合性
なぜ体内時計はリセットが難しいのか
長時間のフライト後に調子を崩したり夜勤で苦労したことがある人なら、体内時計が急なスケジュール変更を嫌うことはよく知っています。本論文はその問題の核心にある非常に具体的な疑問を投げかけます:脳のマスタークロックの内部で、なぜある神経細胞は強く時間信号に反応する一方で、そのすぐ隣の細胞はほとんど無視するのか?マウスのこの小さな時計回路内で単一の化学信号を追跡することで、著者らは“時差ぼけ”に直面した際に体内時計の頑固さを決定するのに寄与する隠れた細胞サブグループを明らかにします。 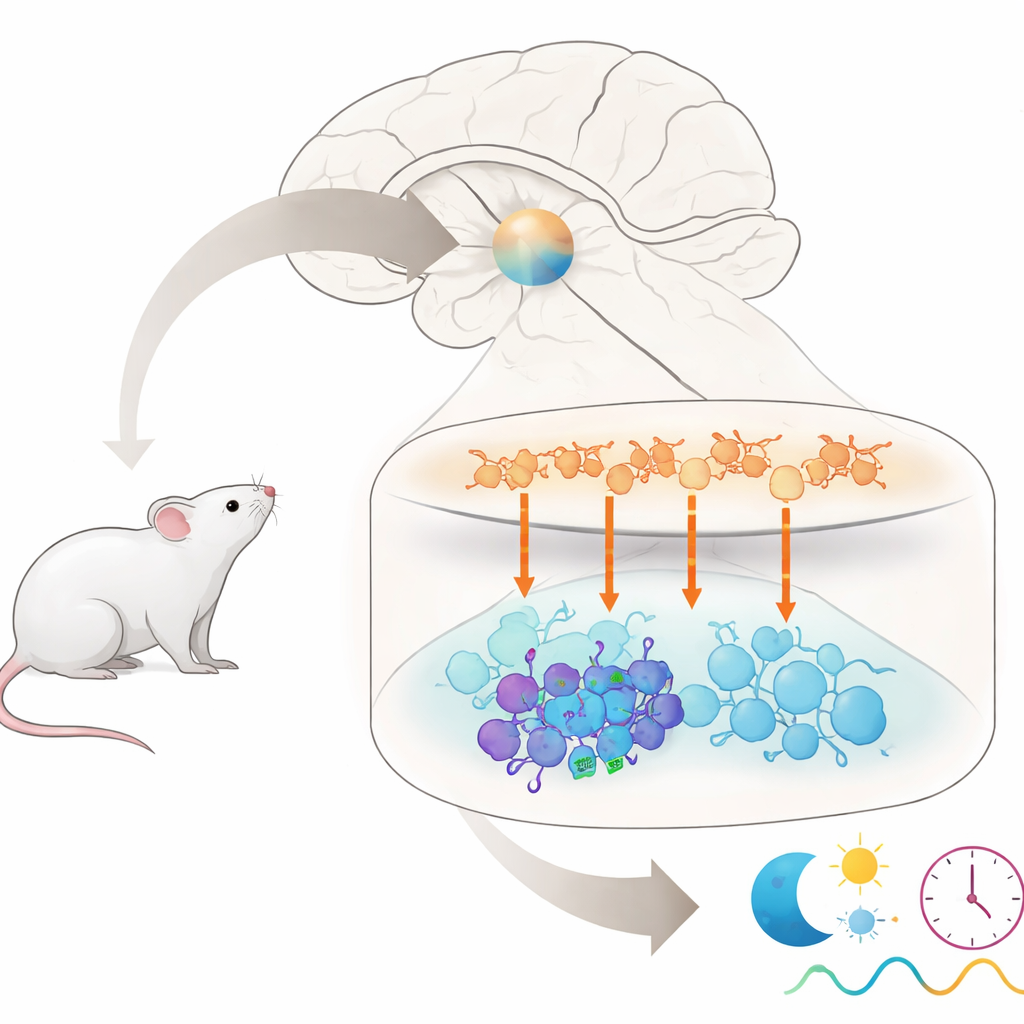
多様な役割をもつ小さな時計
哺乳類のマスタークロックは視交叉上核(suprachiasmatic nucleus, SCN)と呼ばれる脳の小さな領域にあります。約2万個の神経細胞しか含まないものの、異なる化学伝達物質で互いにやり取りするいくつかの明確なグループで構成されています。上部の“シェル”領域の細胞は主にアルギニンバソプレッシン(AVP)という伝達物質を放出し、下部の“コア”領域の細胞はしばしば血管作動性腸管ペプチド(VIP)やガストリン放出ペプチド(GRP)など別の伝達物質を放出します。これらのグループは協調して24時間リズムを生み出し、睡眠やホルモン放出、その他多くの生理機能を支配します。しかし、コアのどの細胞がシェルのAVP細胞からの信号を実際に受け取っているかは不明でした。
送信細胞から受信細胞への配線をたどる
研究者らはまず、シェルのAVP細胞が物理的にどのようにコアのVIPおよびGRP細胞と接続しているかをマッピングしました。彼らはウイルスを用いてAVPニューロンの出力繊維と接触点の可能性を標識し、脳スライスを染色してこれらの繊維がどこで終わるかを観察しました。AVP繊維はVIPおよびGRPの両方に見かけ上の接触部位を形成していましたが、その比率は異なっていました:およそ4分の1のVIP細胞と半数以上のGRP細胞にこれらの付着が見られました。これはAVPニューロンが両タイプのコア細胞に到達していることを示しますが、どの細胞が実際に信号に応答するかはまだ明らかではありませんでした。そのためチームは、光遺伝学(青色光でAVPニューロンを活性化する手法)を用い、VIPおよびGRPニューロンでの細胞活性化のマーカーであるc-Fosの発現を観察しました。
AVPを本当に“聞く”小さなVIPサブ群
AVPニューロンが光で刺激されると、多くのAVP細胞自身が予想通りc-Fosを発現しました。重要なのは、コアのVIP細胞の小さなサブセットもc-Fos活性化を示したことです。これらのVIP細胞は光感受性タンパク質を直接発現していなかったため、AVP入力によって間接的に駆動されていることを示しています。対照的に、GRP細胞はAVP接触を受けていてもめったにc-Fosを示しませんでした。著者らは次に、敏感なRNAイメージング法を用いてV1aとして知られるAVP受容体の遺伝子発現をこれらの集団で探しました。その結果、V1aはVIP細胞のごく一部にしか存在せず、GRP細胞ではほとんど検出されませんでした。したがって、多数のVIPニューロンの中でV1a陽性の小さなサブグループがAVP信号を受け取り応答するよう特別に調整されており、一方で大半のGRPニューロンはそうではないようです。 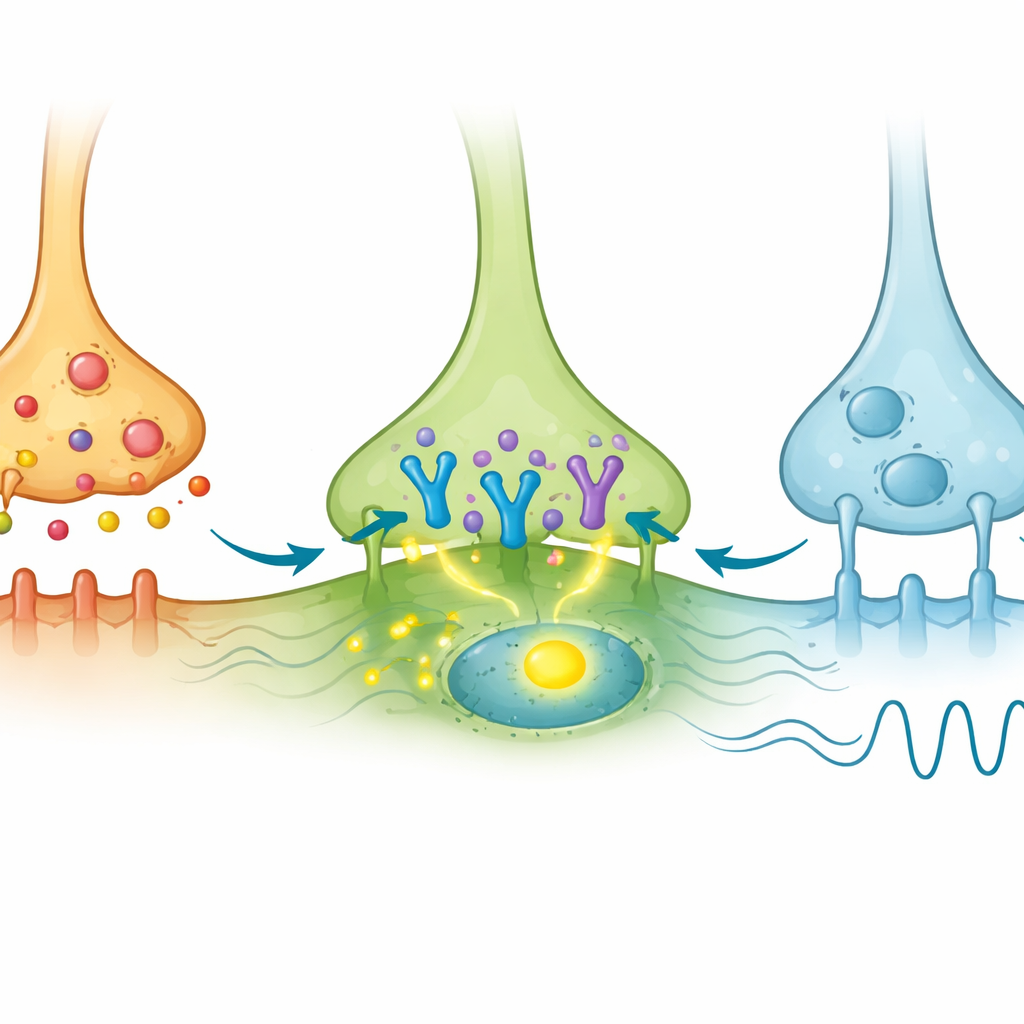
小さな細胞群が時差ぼけ回復を左右する仕組み
これらのV1aを持つVIPニューロンの機能を調べるため、研究者らはV1a受容体をVIP細胞だけから除去したマウスを作成しました。これらの動物は暗転恒常条件下で正常な1日のリズム長を維持し、VIPニューロンにおけるこの受容体は時計の基本的なテンポを設定するために必須ではないことを示しました。しかし、光–暗サイクルを8時間前進または遅延させて時差ぼけを模倣すると、改変マウスは正常な同腹子よりも行動パターンを速く調整しました。特に前進時や雄で顕著でした。別の実験では、脳全体またはSCN特異的にV1aを欠失させても同様の“時差ぼけ耐性”行動が観察されました。これらの新しい結果は、V1a受容体を持つごく小さなVIPニューロン群が、時計全体の硬さ(柔軟性のなさ)に対して過大な影響を及ぼし得ることを示唆します。
時間感覚に対する示唆
日常的な言い方をすれば、この研究は脳の中央時計内でAVP産生ニューロンが上層のタイムキーパーのように働き、V1a受容体を介して下層の選ばれたVIPニューロンへ信号を送ることを示しています。その少数のVIP細胞がネットワーク全体を保ち、光–暗サイクルの急激な変化に対して抵抗し、シフト後の時計のリセットを遅らせます。彼らのAVP感受性受容体を取り除くとシステムはより容易にシフトし、マウスの時差ぼけ様の調整が緩和されます。時計ニューロンのこの隠れた多様性を明らかにすることで、本研究は我々の時間感覚を安定化する配線図をより詳細に描き出し、将来的に類似経路を人間で標的化することが時差ぼけや他のリズム障害の管理に役立つ可能性を示唆します。
引用: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
キーワード: 概日リズム(サーカディアンクロック), 視交叉上核, バソプレッシンシグナル伝達, VIPニューロン, 時差ぼけ