Clear Sky Science · ja
FLVCR1関連感覚ニューロパシーの基盤にあるミトコンドリアのエネルギー不全
痛みを感じる神経の電力が切れるとき
生まれつきほとんど痛みを感じられない人がいます。一見するとそれは恩恵のように思えますが、痛みという警告信号がないと、やけどや骨折、感染、ひどい場合は失明まで引き起こしてしまい、むしろ不幸を招きます。本研究はこうした痛み喪失のまれな一形態を調べ、思いがけない犯人を突き止めます──神経細胞内の小さな発電所、すなわちミトコンドリアのエネルギー産生が深刻に乱れることです。
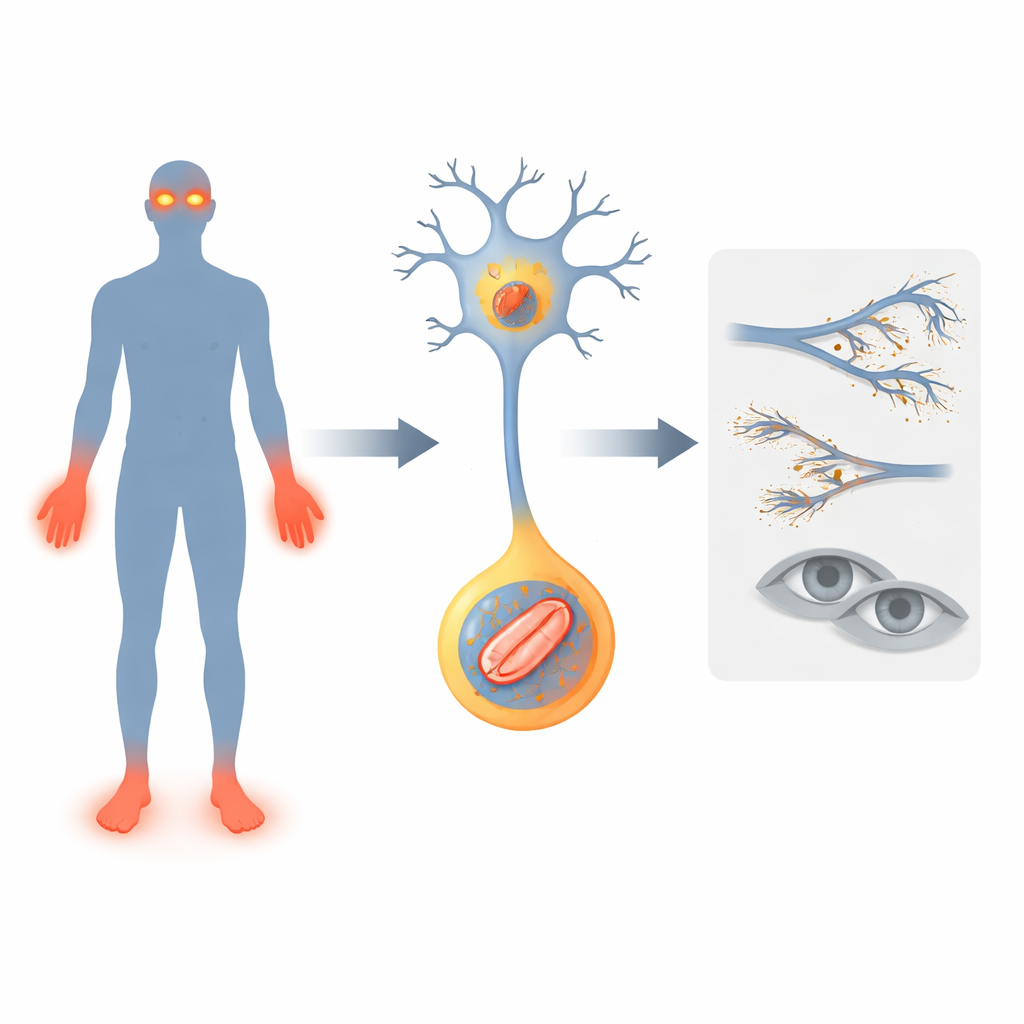
警報を消す遺伝子
研究者たちはFLVCR1という遺伝子に注目しました。この遺伝子はすでに痛覚を失わせるまれな神経疾患と関連づけられており、歩行障害や進行性の視力低下を伴うことがあります。研究ではFLVCR1に変異を持つ新たな2人の患者を報告しています。両子とも幼少期から運動発達の遅れ、転倒の頻発、深い感染、傷に気づかないために指や足趾の損傷を経験しました。1人は網膜色素変性という変性性の眼疾患を発症し、夜盲をきたしました。これらの症例はFLVCR1異常の臨床像を広げ、この遺伝子が痛覚を担う神経や網膜の光受容細胞の維持に重要であることを裏付けます。
小さな魚で病気を再現する
発達中の感覚神経にFLVCR1がどのように関わるかを調べるため、研究チームはゼブラフィッシュを用いました。透明な胚を持つため神経細胞を直接観察できます。魚の遺伝子フレーバント(flvcr1a)の発現を遺伝学的手法で下げると、脊柱に沿って触覚や痛みを感知するニューロンの塊である脊髄神経節(dorsal root ganglia)が減少しました。行動的には、自発運動が減り、尾を軽く刺激しても短距離しか泳がず、感覚反応が鈍くなっていました。これまでのマウスモデルは早期に死亡して感覚神経を解析できなかったため、ゼブラフィッシュはFLVCR1関連の神経障害と行動を詳細に追跡できる初めての生体モデルとなります。
三つの障害経路が細胞の発電所に集中する
FLVCR1は細胞膜に存在し、いくつかの重要な物質の管理を担います。これまでの研究は、膜脂質の構成要素であるコリン、酵素を駆動する鉄含有色素であるヘム、そして細胞内画分間のカルシウム移動の取り扱いに関与すると示唆していました。研究者たちはFLVCR1変異を持つ4人の患者から皮膚線維芽細胞を採取し、健常者や症状のない保因者からの細胞と比較しました。患者細胞ではコリン濃度が低下し、細胞膜がより流動的になっており、ミトコンドリアが要求する繊細な脂質環境が乱れる可能性が示されました。また、ミトコンドリア内でヘム合成に寄与する重要酵素ALAS1の活性が低下していたものの、全体のヘム含量はほぼ正常に見えました。同時に、小胞体とミトコンドリアの接触部位(カルシウムが通常ミトコンドリアへ流入する場所)が短く、頻度も減少し、ミトコンドリアへのカルシウム流入が減っていました。コリン不足、ヘム合成の低下、カルシウム移動の弱化という三つの問題が、いずれもミトコンドリア機能障害を示唆していました。
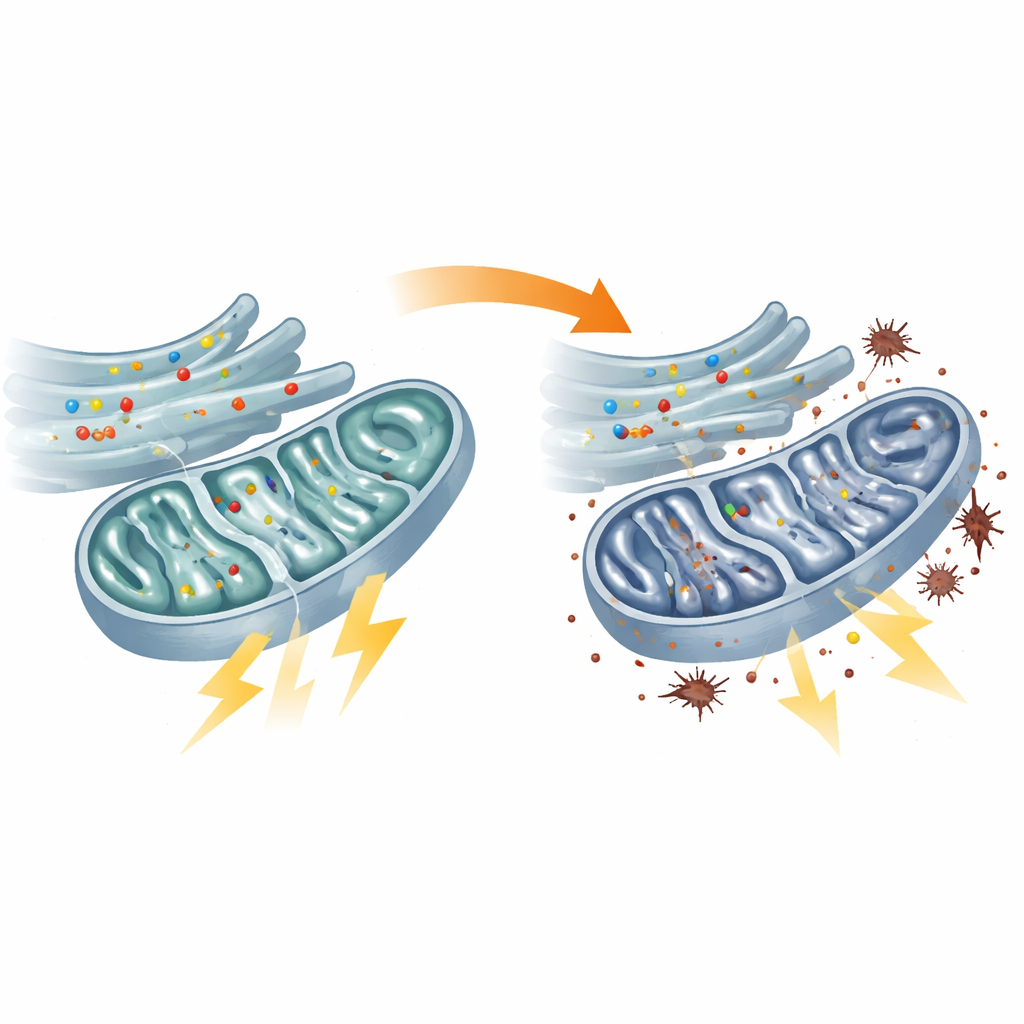
飢えたミトコンドリアと酷使される代替システム
エネルギー代謝の直接的な検査は、患者由来の線維芽細胞のミトコンドリアが機能不全に陥っていることを確認しました。中心的な燃料処理ハブであるTCA回路は遅くなり、いくつかの重要酵素の活性が低下し、通常は燃料をATPという細胞のエネルギー通貨に変換する呼吸鎖の働きも鈍化していました。その結果、ミトコンドリア内のATP量は減少しました。細胞は代償としてミトコンドリア外で行われる、効率の低い糖分解(解糖系)を亢進させました。このエネルギー戦略の転換は代償コストを伴い、ストレスを受けたミトコンドリア機構から電子が漏れ出し、脂質過酸化という膜脂質に対する酸化的損傷が増大しました。これらと同様の欠陥はflvcr1aを減少させたゼブラフィッシュでも見られ、ミトコンドリア故障が感覚ニューロパシーの動物モデルに直接結び付けられました。
細胞のエネルギーを高めることが将来の治療につながる手がかり
励みとなることに、これらの欠陥の一部は実験室で改善できました。患者細胞でミトコンドリアへのカルシウム流入を増やすチャネル蛋白MCUを過剰発現させると、エネルギー産生が回復し、酸化的損傷の指標が低下しました。ヘムの前駆体である5-アミノレブリン酸(ALA)を供給すると、TCA回路活性、呼吸鎖機能、ATP量が改善しましたが、長期曝露は以前の研究で有害とされていることに注意が必要です。追加のコリンは膜流動性を正常化し、脂質損傷を軽減しましたが、短期的にはエネルギー出力の改善は限定的でした。これらのレスキュー実験は、単一の経路だけが責任を負うのではなく、コリン、ヘム、カルシウム取り扱いの広範なネットワークの乱れがミトコンドリアを慢性的な低パフォーマンスに追い込んでいることを示唆します。
なぜこの発見が患者にとって重要なのか
FLVCR1変異が分子レベルから細胞、全生物までどのような影響をもたらすかをたどることで、本研究はミトコンドリアのエネルギー不全がこのタイプの痛覚喪失ニューロパシーとそれに伴う視力障害の駆動因子であると提案します。感覚ニューロンや光受容器は長い軸索を維持したり、光に敏感な構造を絶えず再生したりするため、エネルギー需要が特に高く、ミトコンドリア出力が低下すると脆弱になります。ゼブラフィッシュモデルと患者由来細胞は、ミトコンドリア代謝を強化する治療法を実用的に検証する場を提供します。コリン補給、制御されたヘム増強、ミトコンドリアのカルシウム取り込みを高める薬などの治療法は、動物モデルや臨床試験で慎重に評価される必要がありますが、本研究の核心メッセージは明白です:脆弱なニューロンの電源を回復することで、自然が与えた最も重要な警告信号である痛みを生まれながらにして感じない人々を将来守る助けになるかもしれません。
引用: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
キーワード: 感覚ニューロパシー, ミトコンドリア機能不全, FLVCR1, 痛覚無感覚, 神経のエネルギー代謝