Clear Sky Science · ja
前臨床核酸治療薬研究におけるモデル選択
遺伝子を薬に変える
核酸療法は、従来の多くの薬がタンパク質を阻害するのとは異なり、さらに一段階上の遺伝子メッセージのレベルで作用する新しいタイプの医薬品です。本総説は、患者に届ける前にこれらのRNA標的薬を評価するために研究者がどのように適切な実験室および動物モデルを選ぶかを解説します。一般読者が関心を持つ理由は、賢いモデル選択により希少な小児疾患から心臓病のようなより一般的な病態まで、より速く、安全で効果的な治療が実現する可能性があるためです。
これらの遺伝子医薬は何が違うのか?
核酸治療薬(NAT)は、アンチセンスオリゴヌクレオチド(ASO)や小干渉RNA(siRNA)といった短い配列を含みます。タンパク質標的の形状や化学に依存するのではなく、これらの薬は塩基対形成(DNAやRNAに見られるA‑T や G‑C の相補性)によって標的を認識します。そのためプログラム可能であり、変更したいRNA配列が分かれば、従来の化学による長い探索を経ずとも多くの候補を迅速に設計できることが多いです。難しいのは「活性化合物を作れるか」ではなく、「現実的な生物学的環境で本当に機能するかどうかをどう測るか」です。配列の一文字の違いが活性を左右しうるため、適切な試験系の選択が極めて重要になります。
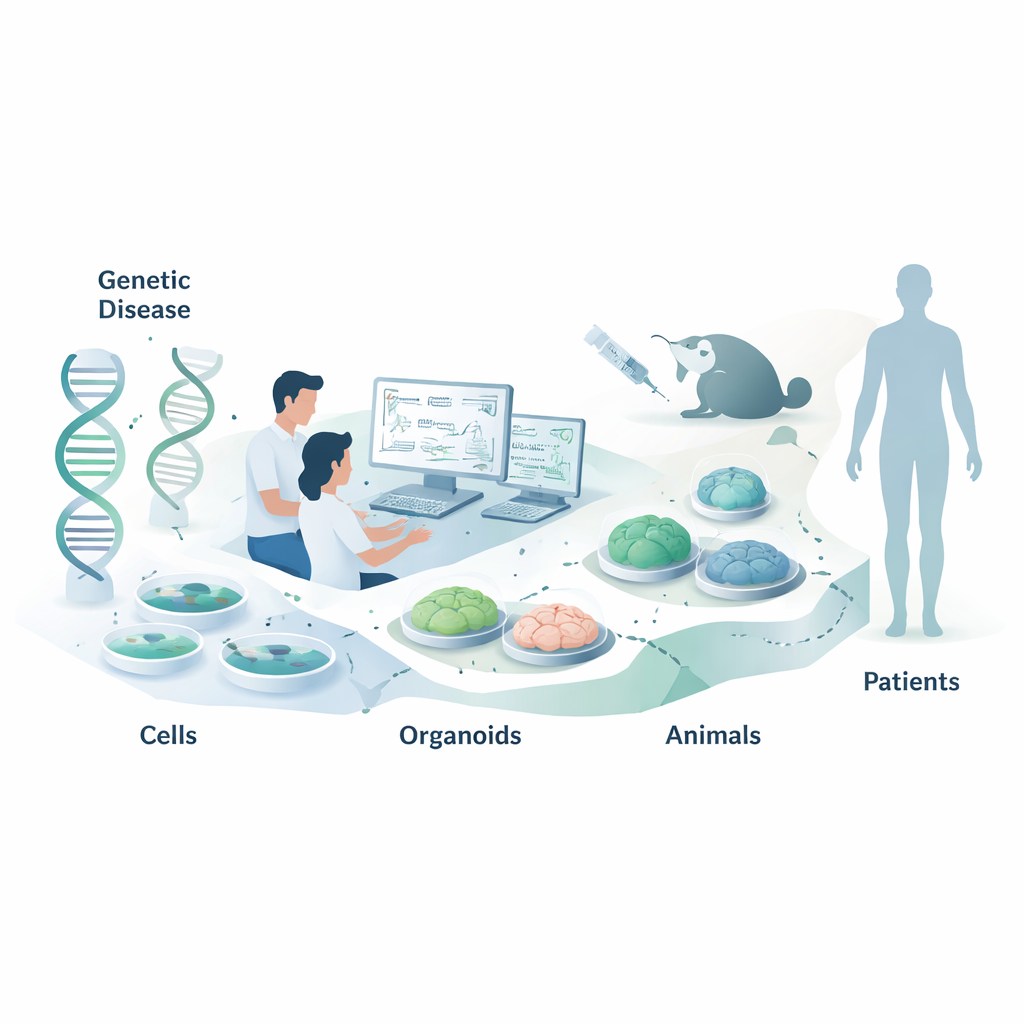
単純な細胞試験:速いが全てを語らない
多くのNATの最初の段階は、標的RNAを自然に発現しているHeLaやHEK293などの培養が容易な細胞株のパネルです。研究者は大量の候補ASOやsiRNAを添加し、PCRやウェスタンブロットなどの手法で標的RNAや対応するタンパク質がどれだけ減少するかを測定します。患者由来の細胞を用いれば、その人固有の遺伝的背景をより正確に反映でき、欠陥がある遺伝子コピーだけを沈黙させる「アレル選択的」薬の検証も可能です。自然な遺伝子発現が都合よく起きない場合は、人工的なミニ遺伝子や、RNAが切断または正しくスプライスされると発光するレポータープラスミドを導入することもあります。これらの系は多数のデザインを迅速に比較するのに強力ですが、自然なRNA構造や細胞種特異的なプロセシングなど重要な要素を見落とす可能性があるため、より現実的なコンテキストでの確認が必要です。
分子レベルの修正から実際の細胞挙動へ
多くのNATは単に欠陥RNAを破壊するだけでなく、スプライシングを変えて修復することを目指します。慎重に設計されたASOは、有害なエクソンをスキップさせる、欠落した断片を回復させる、あるいはコードを破壊する「偽エクソン」の挿入を防ぐといった作用をもたらします。こうした変化が実際に細胞機能を改善するかを見るために、研究者はRNAやタンパク質量だけの単純な読み出しを越えます。患者由来の細胞では、酵素活性が回復するか、肺細胞のイオン輸送が正常化するか、免疫細胞のシグナル伝達が正しく応答するかを評価します。近年では、患者の幹細胞から育てた三次元オルガノイド(ミニ組織)を用い、心臓の拍動や脳ネットワークの活動など複雑な挙動を再現することが増えています。これらの3次元モデルは実臓器に近い一方で、実行は難しく、遅く、費用も高いため、現実性と処理能力のバランスを取る必要があります。
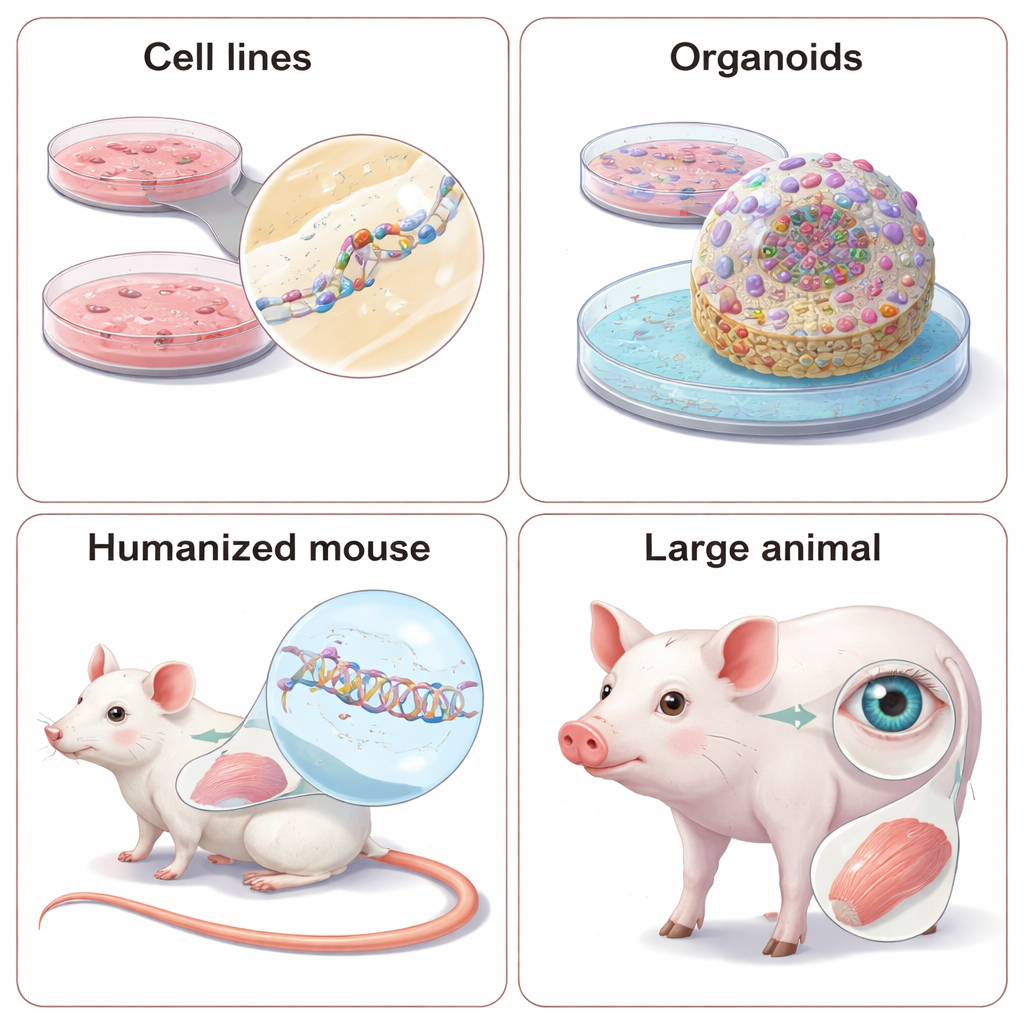
なぜ動物モデルが依然重要なのか — そしてヒト化の方法
全身代謝や器官間相互作用、行動といった疾病の特徴はシャーレ内では再現できないことがあります。こうした点を評価するためにNATは生体動物で試験されます。これらの薬は正確なRNA配列に依存するため、研究者は選択を迫られます:動物の遺伝子バージョンに一致する「代替(サロゲート)」薬を設計するか、動物自体をヒトの遺伝配列を持つように再設計するか。代替ASOやsiRNAは、確立されたマウスモデルで遺伝子を低下させることで症状改善の可能性を示しますが、ヒト標的薬を完全に模倣するわけではありません。ヒト化モデル—ヒト遺伝子の一部または全コピーを持つマウスやミニブタなど—は臨床候補の実薬を評価できますが、作成には相当の時間とコストがかかり、種間の遺伝子制御の微妙な違いが依然として驚きを生むことがあります。本総説はまた、眼や筋肉の疾患では解剖学的にヒトに近い大型動物の利用が増えている点も強調しています。
展望:より賢いモデルと推測の削減
著者らは、核酸医薬に万能の「最良」モデルは存在せず、むしろ各プロジェクトが高速で単純なアッセイから出発し、より複雑でヒトに近いシステムへ段階的に進む、という個別の道筋が必要だと結論づけています。規制当局や資金提供者が動物使用の削減を促す中で、高度なオルガノイド、オルガンオンチップデバイス、計算モデルがより大きな役割を担うと期待され、とりわけどの配列や化学修飾が有効かを予測する機械学習ツールと組み合わせることで効果が高まります。最終的には、各モデルの強みと盲点を理解し、分野横断でベストプラクティスとデータを共有することで、プログラム可能な遺伝学的アイデアを患者にとって安全で効果的な医薬品へとより確実に変えていけるでしょう。
引用: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
キーワード: 核酸治療薬, アンチセンスオリゴヌクレオチド, siRNA, 前臨床モデル, 遺伝子治療