Clear Sky Science · ja
二価カチオンの選択的結合がヌクレオソームの力学を再形成し、ヒストン尾部の動態を解放する
微小なイオンが私たちのDNAをどう扱うか
すべての細胞の内部では、何メートルにも及ぶDNAを折りたたみ、詰め込みつつ、必要に応じてアクセス可能にしておかなければなりません。本稿は、細胞内に普通に存在する二つの無機イオン、マグネシウムとカルシウムがどのようにしてDNAのタンパク質への巻きつき方を微妙に変え、遺伝情報のパッケージングの密度や読み取りやすさに影響するかを探ります。原子レベルでこれらの相互作用をシミュレーションすることで、イオン濃度の変化が局所的なDNA構造を硬くしたり緩めたりし、染色体の構築に寄与する柔らかいヒストン尾部の挙動を変えることを明らかにしています。
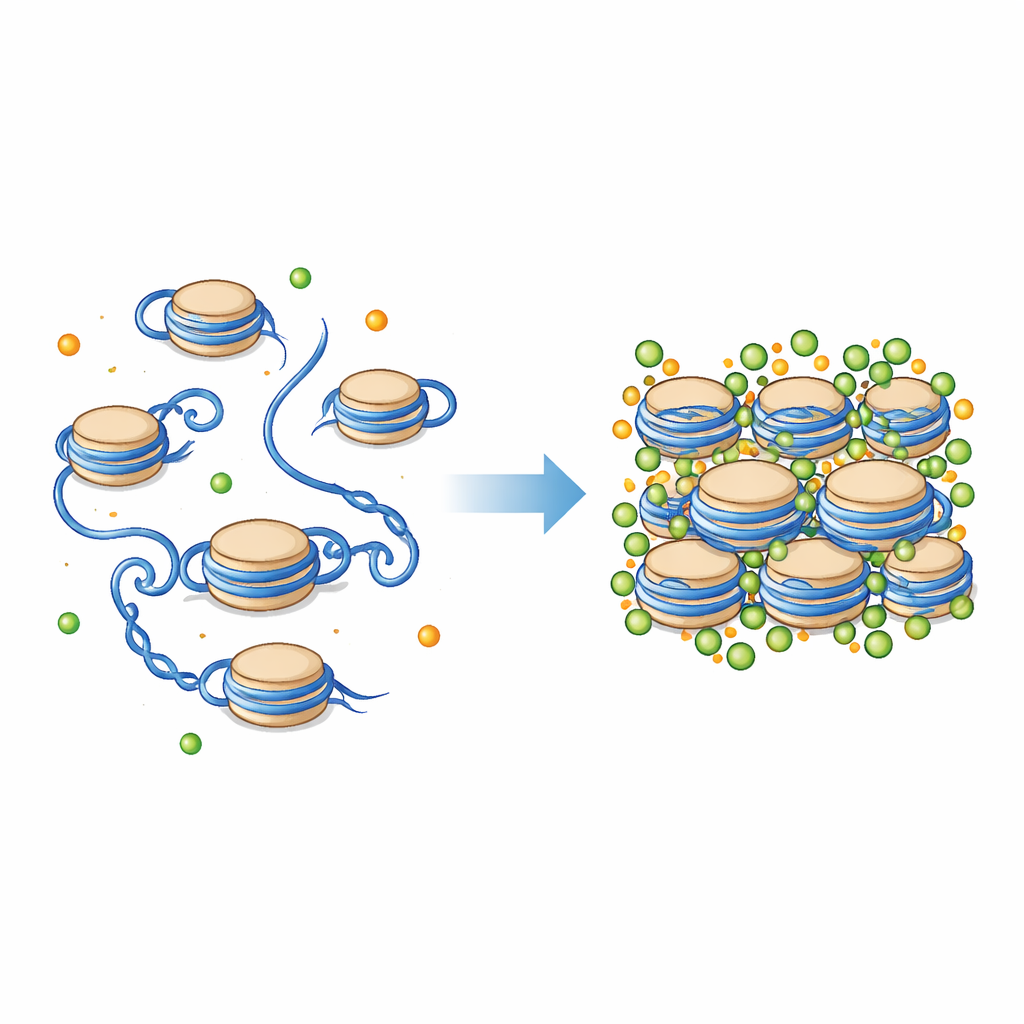
染色体パッキングの核となるビーズ
細胞内のDNAはむき出しのままではなく、ヌクレオソームと呼ばれるタンパク質のスプールに巻き付いています。各ヌクレオソームは短いDNAの断片がヒストンタンパク質の塊の周りに巻かれ、外側には柔軟な尾部が伸びています。これらが並んでクロマチンの基本的な「ビーズ・オン・ストリング」構造を作り、それがさらに折り畳まれてより高密度の繊維を形成します。ヌクレオソームの周囲には負電荷の粒子が多く存在し、その中にはマグネシウム(Mg²⁺)やカルシウム(Ca²⁺)も含まれます。これらのイオンは染色体の凝縮を助けることが知られていますが、ヌクレオソームやヒストン尾部の微細な力学にどのように影響するかは直接見るのが難しい点でした。
原子が密集する世界をシミュレートする
これらの詳細を明らかにするため、著者らはDNA、タンパク質、水、イオンのすべての原子を明示的にモデル化した大規模なコンピュータシミュレーションを合計81マイクロ秒にわたって実行しました。マグネシウムとカルシウムの濃度を系統的に変え、シミュレーションにおけるイオンの振る舞いを記述する異なる手法を試し、ヒストン尾部の有無でヌクレオソームを比較しました。シミュレーションで得られたイオン結合パターンを実験データと比較することで、実際のヌクレオソームがこれらのイオンをどのように引き付けるかを最もよく再現する精緻なモデルを特定しました。マグネシウムはDNAの溝を好み、カルシウムはDNAの骨格や特定の酸性タンパク部位に結合しやすいことが示されました。
イオンがDNAを圧し、コアを硬化させる仕組み
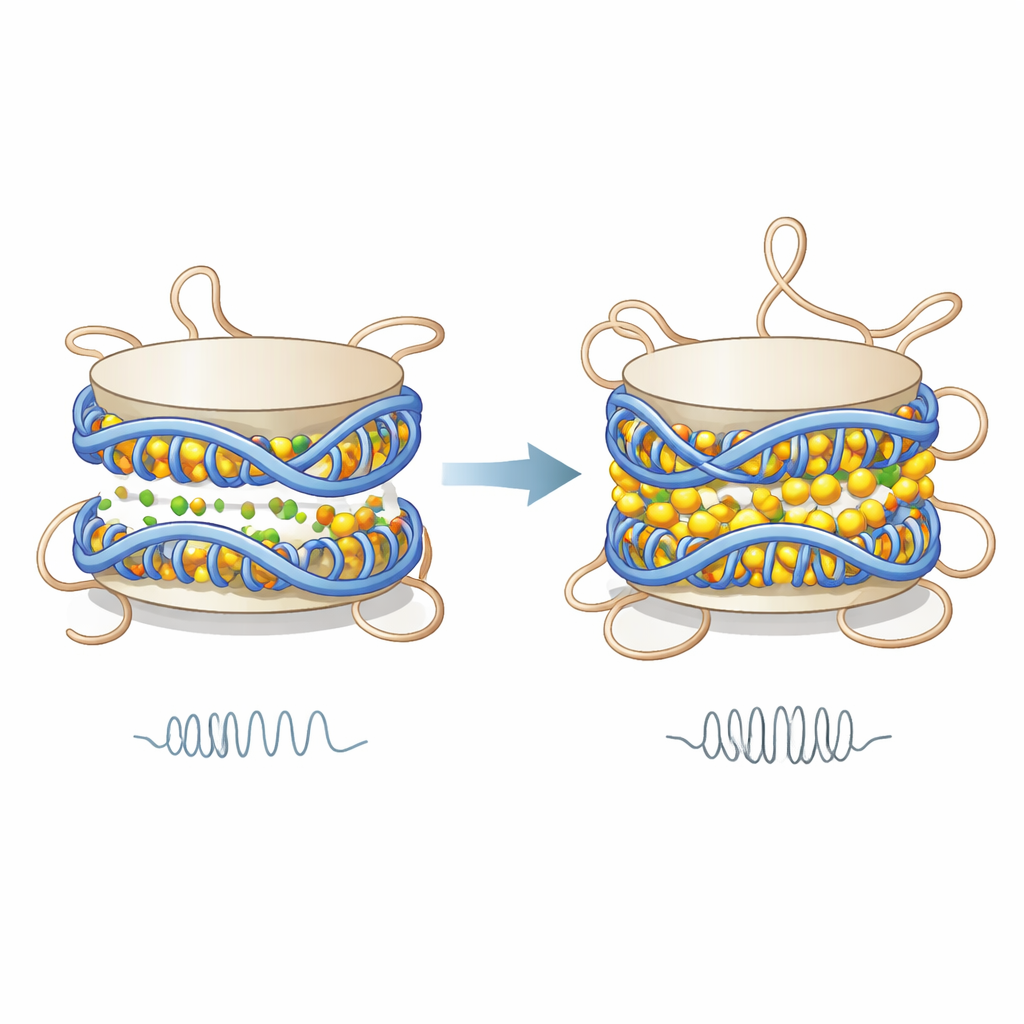
シミュレーションは、二価イオンがDNA表面およびヌクレオソームを巻く二重のDNAターンの狭い空間に集まることを示しています。これらのイオンはDNAの強い負電荷を部分的に中和することで、隣接するDNAターン間の電気的反発を和らげます。その結果、二重のDNAコイルは互いにより近づき、ヌクレオソームはわずかに短くなり、ヌクレオソームを小さな弾性円筒として扱うモデルで測定したときに機械的剛性が増します。この剛性の増加はDNAが剥がれたり大きくアンラップすることによるのではなく、間隔のわずかな変化や特定のDNA領域がより協調して動くこと、つまり一体としてより硬く動くようになることから生じます。
柔らかいヒストン尾部を解放する
DNAコアがより凝縮して剛性を増す一方で、柔軟なヒストン尾部は逆の反応を示します。低イオン条件下では、これらの尾部にある正に帯電したアミノ酸が負に帯電したDNAに密着し、多くの安定した接触を形成します。マグネシウムやカルシウムがDNAに結合すると、これらの電荷を遮蔽して尾部とDNAの引き付けを弱めます。著者らは、特にH3ヒストン由来の尾部とDNAの接触が減少し、DNA上での滞留時間が短くなり、尾部が取り得る位置の範囲が広がることを見出しました。つまり、尾部はより頻繁で短い出会いを重ねるようになり、動的になって隣接するヌクレオソームに届きやすくなる可能性があります。
遺伝子制御とクロマチン状態への含意
これらの結果は、マグネシウムとカルシウムがクロマチンに対して二重の役割を果たすことを示しています。DNAの巻きつきを引き締めヌクレオソームの剛性を高めることで、よりコンパクトで柔軟性の低いクロマチンを促進します。同時に、ヒストン尾部とDNAの接触を緩め尾部の運動を活発化することで、化学的修飾の標的や調節因子が認識しやすい部位を露出させます。核内のイオン濃度はシグナルやエネルギー消費に伴って変動するため、この研究は細胞環境の小さな化学的変化がヌクレオソームの機械的性質とその規制尾部のアクセス性を調整し、遺伝子活性の開閉の窓を開け閉めする助けになることを示唆しています。
引用: Hu, G., Zhang, H., Xu, W. et al. Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics. Commun Biol 9, 365 (2026). https://doi.org/10.1038/s42003-026-09648-1
キーワード: クロマチン, ヌクレオソームの力学, マグネシウムとカルシウムイオン, ヒストン尾部, 遺伝子制御