Clear Sky Science · ja
HCN2チャネルにおける環状ヌクレオチドのエントロピー駆動および負の協同性結合にはサブユニット間経路が必要である
心臓の小さなペースメーカースイッチは化学信号をどう感知するか
一拍ごとの心拍や多くの脳リズムは、細胞膜に開閉する微小なチャネルに依存しています。これらHCNペースメーカーチャネルは電位によって制御されるだけでなく、環状ヌクレオチドと呼ばれる小さなメッセンジャー分子によっても調節されます。本研究は一見単純だが重要な疑問を投げかけます:これらの小さな分子はHCN2チャネルにどのように協調的に結合し、その過程の微細な欠陥がどのようにてんかんなどの障害に寄与しうるのか?
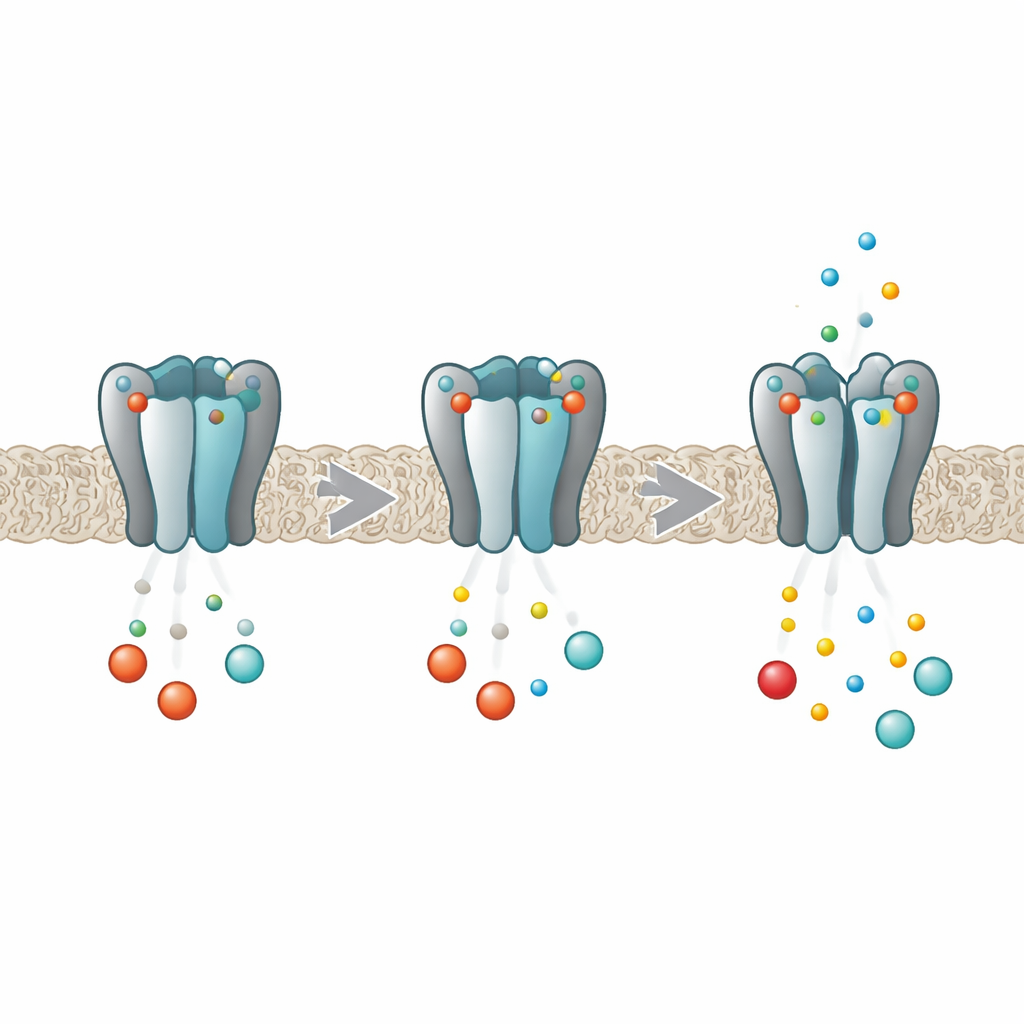
体のリズムのための分子ディマー
HCNチャネルは心臓や脳細胞の電気活動に対するディマー(明るさ調節)スイッチのように働きます。各チャネルは四つの同一タンパク質サブユニットから構成され、これらが中央のイオン通路を形成します。各サブユニットの内部にはcAMPやcGMPといった環状ヌクレオチドを取り込むポケットが存在します。これらのメッセンジャーが結合すると、通路が開きやすくなりペースメーカー電流が増加します。先行研究は、HCN2変異体では各ポケットに独立して結合が起こるのではなく、四つの部位が互いに影響し合い、最初の分子が後からの分子より結合しやすくなる──負の協同性と呼ばれる振る舞い──を示すことを明らかにしました。新しい研究は、この四つのサブユニットが結合過程中にどのように“会話”するのかを解明しようとしました。
隣のサブユニットを感じ取るサブユニット
研究者らは計算シミュレーションと単離したHCN2チャネルトレイル片の実験測定を組み合わせました。長時間の分子動力学シミュレーションを用い、環状ヌクレオチドポケットと孔に連結するいわゆるCリンカーを含むチャネルの尾部領域が、cAMPやcGMPが異なる数だけ結合したときにどのようにたわみ振動するかを観察しました。彼らは、あるサブユニットにメッセンジャーが結合しても、そのサブユニットだけが安定化するわけではないことを見出しました。むしろ、結合は近傍のサブユニットの安定性を微妙に変え、時にはより剛直に、時にはより柔軟にするなどの影響を及ぼし、全体の形状はほとんど変わらないにもかかわらず隣接サブユニットへの影響が生じました。これらの隣接間の影響は占有している部位の数や環状に並ぶ位置に依存しており、負の協同性から期待される挙動と一致していました。
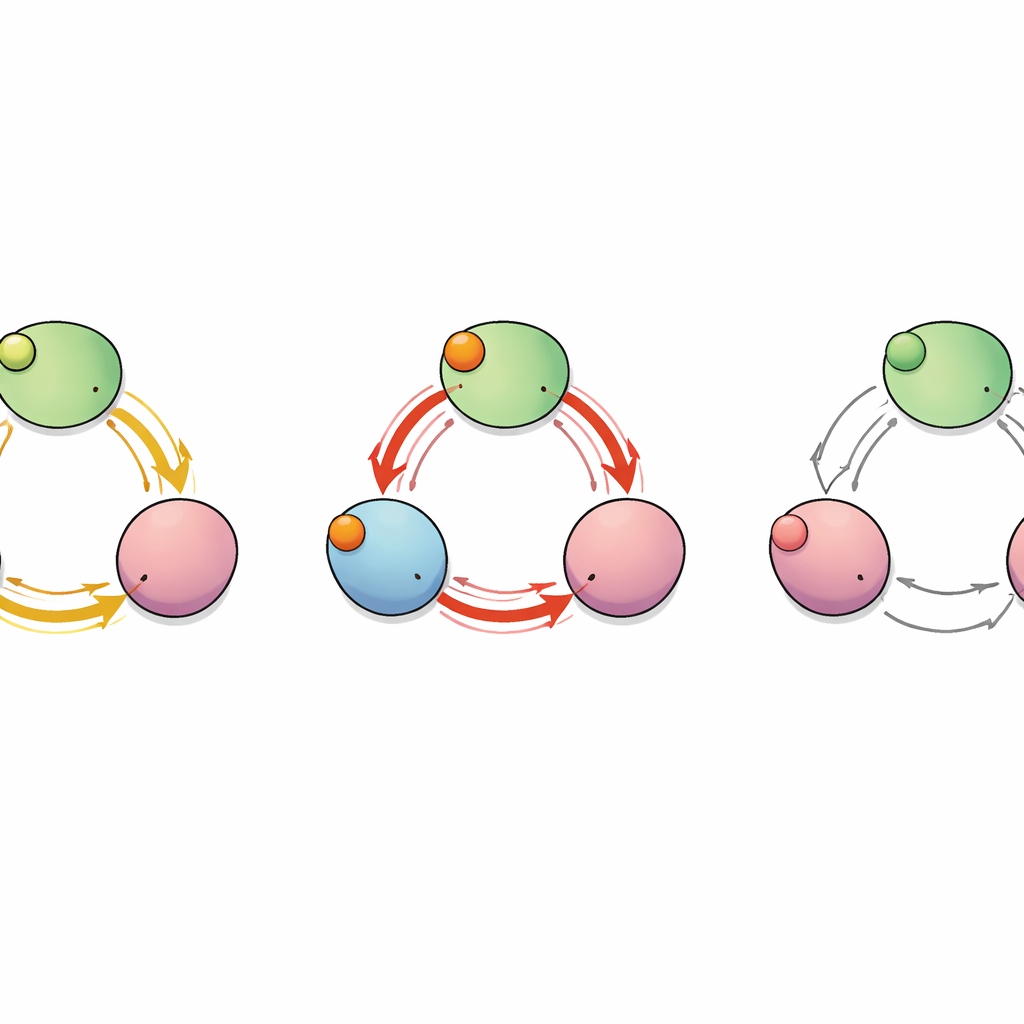
サブユニット間の隠れた経路
結合という“信号”がタンパク質内をどのように伝わるかを写し取るため、チームはチャネルを相互作用するアミノ酸のネットワークとして扱いました。シミュレーション中にどの残基が相関して動くかを計算し、グラフ理論の手法で結合ポケットから孔を制御するCリンカーへと至る最短かつ効率的な伝達経路を同定しました。この解析によりいくつかの経路が明らかになりましたが、特に二つが際立ちました:一つは単一サブユニット内にとどまる経路、もう一つはサブユニット間を横断して隣接サブユニットへ跳ぶ経路です。このサブユニット間経路に沿って、位置488のグルタミン酸(E488)が多くの最短経路を通過する重要なハブとして振る舞い、協同性結合の重要な中継点であり得ることが示唆されました。
会話を断つ変異
著者らは次に、精製したチャネルトレイル片を使った実験でこの経路の重要性を検証しました。彼らはE488と、経路が到達する隣接サブユニット上にあるチロシン459(Y459)を変異させました。動的光散乱法により、変異体タンパク質も四量体複合体として組み立てられることは確認されましたが、野生型で見られたようなリガンド結合に伴うサブユニット間の強い引き締まりはもはや観察されませんでした。等温滴定熱量測定ではさらに大きな変化が明らかになりました:野生型HCN2は二段階の結合事象を示し、最初の高親和性段階は主にエントロピーの増大(内部運動の増加)によって駆動され、その後に三つの低親和性段階が続きました。対照的にE488やY459の変異体は、この有利なエントロピー的ブーストを欠き、特徴的な負の協同性を失って単一の穏やかな親和性結合モードしか示しませんでした。
微妙なエントロピー変化が重要な理由
これらの要素を総合すると、本研究はHCN2チャネルを特定の“会話経路”で結ばれた四つのサブユニットからなる動的な環として描き出します。最初の環状ヌクレオチドが結合すると、それはE488やY459を介して環の遠隔部位の運動性を修正し、後続の結合事象を不利にして孔の応答を調節します。この効果は大きな構造変化によるものではなく、内部の柔軟性――静的スナップショットでは見えないが機能に不可欠なエントロピーの変化――によって駆動されます。サブユニット間経路上の重要残基を破壊する変異はこの“会話”を消し、負の協同性を失わせ、特発性全般性てんかんなどの疾患と関連します。一般読者への要点は、心臓や脳の生命に関わるスイッチはサブユニット間の精密に調整された分子的“ささやき”に依存しており、これらを理解することで正常なリズムと異常が生じたときの仕組みが説明できるということです。
引用: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
キーワード: HCN2イオンチャネル, 環状ヌクレオチド結合, 負の協同性, アロステリック伝達, てんかん変異