Clear Sky Science · ja
小分子がアロステリックにSecA依存の分泌を活性化する
細菌の出荷ドックをフルスロットルにする
細菌は膜の小さなゲートを通して絶えずタンパク質を輸出することで生き延びます。これらの輸出は細胞壁の構築、毒素の分泌、ストレスへの適応など感染の中核をなすプロセスに寄与します。本研究はHSI#6と呼ばれる小さな化合物を報告します。これは通常の輸送装置を阻害するのではなく、むしろそれを過剰に活性化し、選択性を低下させるという異例の作用を示します。このスイッチの仕組みを理解することで、新たな抗菌戦略の発見や必要に応じてタンパク質分泌を増強するバイオテクノロジー用途への応用が期待されます。
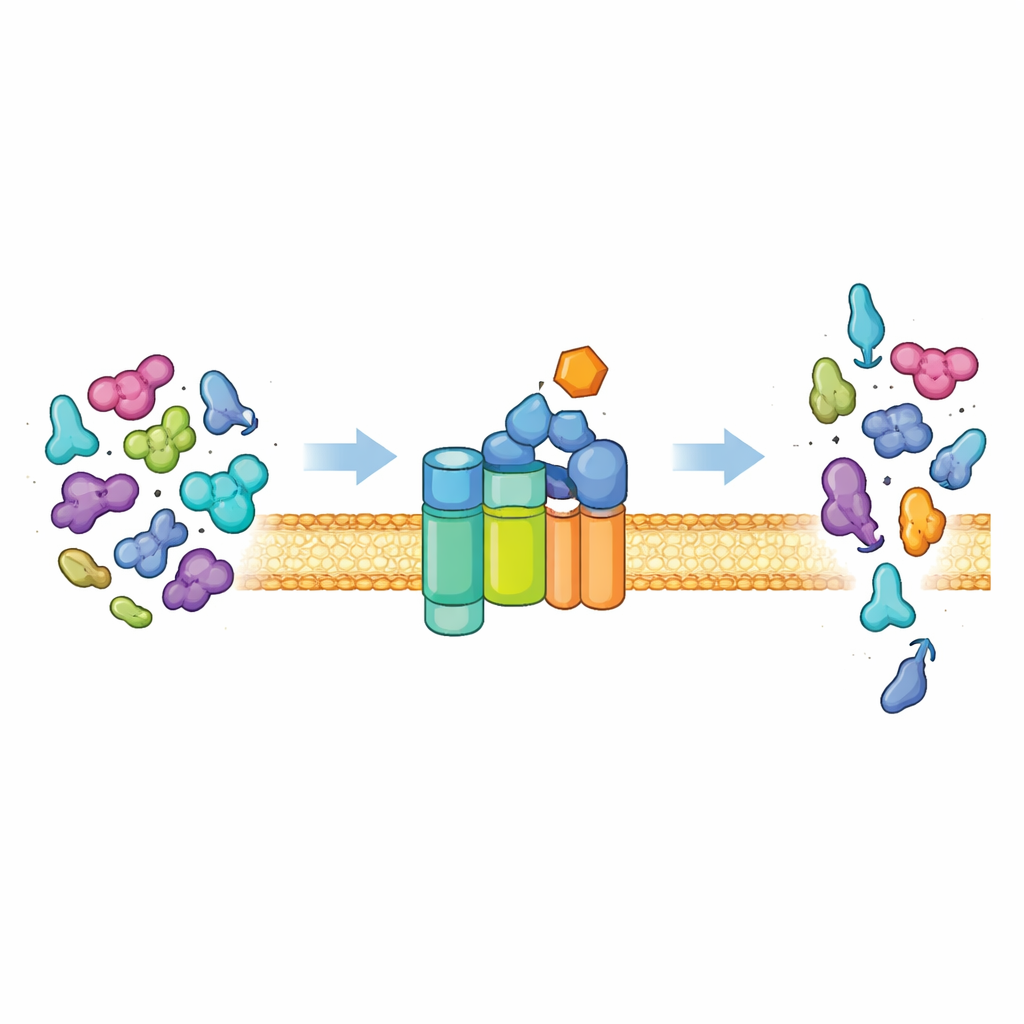
細胞のタンパク質出口ゲート
ほとんどの細菌はSecシステムとして知られる普遍的経路を用いてタンパク質を細胞外へ輸送します。その中心は膜チャネル(SecYEG)と、ATPという細胞燃料を消費して伸長中の非折りたたみタンパク質鎖をチャネルに押し出すモータタンパク質SecAです。通常、このシステムは選択的で、主にシグナルペプチドと呼ばれる特別な宛先タグや本体にある追加の特徴を持つ“前駆体”タンパク質を輸出します。これらの特徴はSecAを低活性の静止状態から強力なモータへ切り替えるために必要です。適切な信号の組み合わせを示すタンパク質だけが完全な活性を引き出せるため、細胞は正しい貨物を輸出し、通常の細胞質タンパク質を安全に内部に保ちます。
モータを目覚めさせる小分子
研究者らは細菌のタンパク質分泌と増殖に影響を与える化合物を探索するスクリーニングでHSI#6を発見しました。生化学的試験により、HSI#6はマイクロモルの親和性でSecAに直接結合し、ATPの利用効率を変化させることが示されました。溶液中ではSecAがATPをより強く保持するようになり、SecAがチャネルに結合した状態ではHSI#6はATP結合を改善すると同時にATPの回転速度を上げます。このパターンはアロステリック活性化因子の特徴です:ある部位に結合して離れた活性部位の挙動を変える分子です。天然のタンパク質クライアントとは異なり、HSI#6は貨物として作用する必要はなく、SecAの内部ダイナミクスを調整してトランスロケース全体を触媒的に活性化させます。
選択的フィルターから多用途ナノマシンへ
HSI#6が結合すると、Secシステムは従来の輸出タグを要求しなくなります。試験管内実験では、この化合物は標準的な前駆体の分泌をほぼ2倍に増やし、既知のSecA阻害剤であるアジ化ナトリウムに対する耐性を高めました。さらに注目すべきは、HSI#6がシグナルペプチドをまったく欠くタンパク質や通常は細胞質に存在するタンパク質の輸送を、野生型の機構で可能にしたことです。生細胞では、アルカリホスファターゼを用いたレポーターで同様の効果が観察されました:細胞質性タンパク質を分泌酵素に融合した場合、HSI#6の存在下で分泌活性が急増したが、タンパク質の発現量自体は変わりませんでした。言い換えれば、HSI#6は輸出を通常のクライアント識別から実質的に切り離し、十分に非折りたたまれた任意のタンパク質に対して広く作用する輸出ポンプにSecシステムを変貌させます。
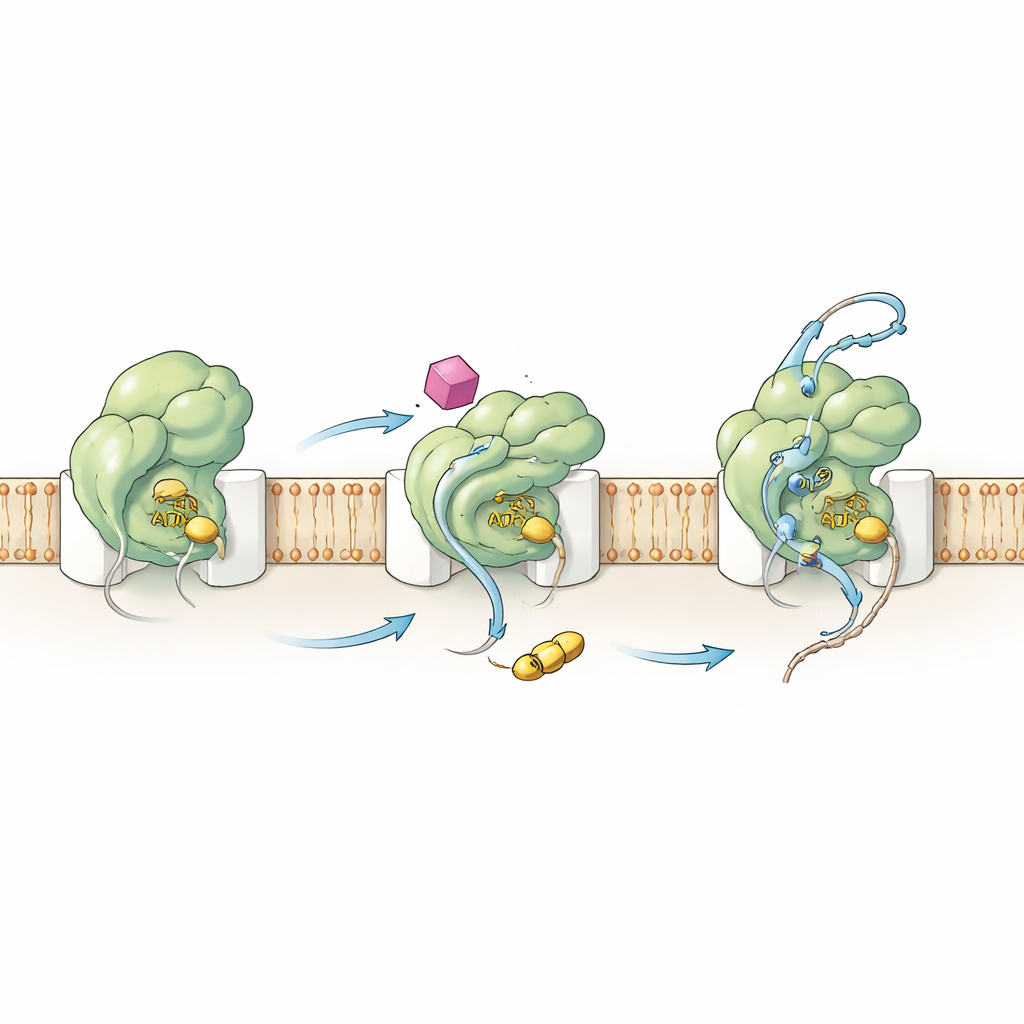
内部からモータを再配線する
HSI#6がこの挙動を引き起こす仕組みを理解するため、研究チームはSecAの化学的性質と運動を調べました。速度論的測定は、化合物が重要な活性化ステップを前倒しにすることを示しました:SecA–チャネル複合体はタンパク質クライアントが結合する前に触媒的に活性化されます。HSI#6はまた、通常は遅く律速となる消費済み燃料(ADP)の放出を助け、それによりATPサイクルの高速化を支えます。水素–重水素交換質量分析を用いて、著者らはHSI#6がSecAの異なる領域の柔軟性をどのように再形成するかをマッピングしました。化合物はクライアントを感知しチャネルへ接続する部分を選択的に緩め、一方でおそらく結合部位を備える足場領域を硬くします。結果として現れる運動パターンは、すでに結合状態にある“オン”のトランスロケースに似ており、HSI#6はクライアントがなくても活性化された形を安定化する—場合によってはチャネルに結合したモノマー型SecAを支持する—ことを示唆します。
医学とバイオテクノロジーでの意義
小分子がSecAをアロステリックに活性化し、その通常のクライアント選択性を剥ぎ取れることを示した本研究は、中心的な細菌機構を制御する新たな方法を明らかにします。感染症の観点では、このような強制的で制御不能な分泌はエネルギーを浪費させ輸出プログラムを混乱させることで病原体を弱体化させ得るため、HSI#6様の活性化剤は抗生物質設計の魅力的な出発点となります—また同じ調節機能を標的にする将来の阻害剤設計の指針にもなり得ます。バイオテクノロジーでは、同じ原理を再利用して有用な組換えタンパク質の分泌を強化できる可能性があり、改変したシグナルペプチドや複雑な遺伝子改変を必要としません。要するに、本研究は細菌のタンパク質“出荷ドック”を化学的に再プログラムできることを実証し、微生物と戦うための新たな道と、それらを微小な工場として活用するための道を開きます。
引用: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
キーワード: 細菌のタンパク質分泌, SecAトランスロケース, アロステリック活性化, 小分子調節因子, 抗菌薬探索