Clear Sky Science · ja
LncRNA P4HA2-AS1はTRIM32によるULK1のK63ユビキチン化とオートファジーの異常を介して腎間質線維症を促進する
なぜ腎臓の瘢痕化が重要なのか
慢性腎臓病は世界中で数億人に影響を与え、しばしば透析や移植が生命維持の唯一の手段になるまで静かに進行します。この機能低下の中心にあるのは、正常な腎組織が徐々に硬く機能しない物質に置き換わる「瘢痕化」と呼ばれる過程です。本研究は単純だが重要な問いを立てます:腎細胞内のどの分子スイッチがこれら有害な瘢痕化へと導き、それらのスイッチは元に戻せるのか?
腎細胞に潜むRNAスイッチ
腎臓は精緻な管状ネットワークを使って血液を濾過します。尿の流れの閉塞、高血糖、あるいは血流の急な途絶によりこれらの尿細管が損傷を受けると、細胞間に瘢痕組織を沈着させる反応が起きます。研究者らは複数の損傷モデルを持つマウスの腎臓を健常な腎臓と比較し、どの遺伝子が発現しているかを読み取るRNAシーケンシングを用いて探索しました。その結果、P4HA2‑AS1と呼ばれる比較的知られていない長鎖非翻訳RNAが、損傷して瘢痕を形成する腎臓や実験室でストレスを受けたヒト腎細胞で一貫して増加していることを発見しました。このRNAは主に細胞の液胞状の部分に存在し、そこで他のタンパク質を制御している可能性が示唆されます。 
RNAを減らして腎臓を守る
P4HA2‑AS1が単なる傍観者なのか、ダメージの能動的な駆動因子なのかを検証するため、研究チームはマウスおよび培養したヒト腎細胞でこのRNAの量を減らしました。片側の尿管を結紮して長期閉塞を誘導する確立されたマウスモデルでは、ウイルスを用いた標的デリバリーでこのRNAを低下させると、瘢痕化の多くの指標が改善しました:尿細管の保持、細胞間のコラーゲンやその他の瘢痕タンパク質の減少、血液中の腎機能マーカーの改善です。培養皿内のヒト腎細胞でも、P4HA2‑AS1を減らすと強力な瘢痕化シグナルであるTGF‑βへの応答が抑えられ、フィブロネクチンやコラーゲンなどの線維化促進因子の産生が低下しました。これらの実験は、このRNAが単なる損傷の指標ではなく、瘢痕化プロセスを能動的に促進することを示しています。
オートファジー:維持管理から有害へ
研究者らは次に、このRNAがどのようにダメージを引き起こすかを問いました。遺伝子発現とイメージングのデータは、損耗したタンパク質や細胞小器官を分解する細胞の組み込みリサイクルシステムであるオートファジーを指し示しました。通常、オートファジーは健康的な維持管理プロセスですが、過度に長期間にわたって活性化されると、損傷した腎臓を不適応な修復と瘢痕化へと押しやることがあります。ストレスを受けた腎細胞ではP4HA2‑AS1がオートファジーの流れを増強し、リサイクル小胞の蓄積を招きました。RNAを阻害すると、この過剰なリサイクルは細胞および閉塞マウスの腎臓で正常に近いレベルへ戻りました。オートファジー開始の中心的酵素であるULK1を欠くマウスも瘢痕化から保護され、これらの動物ではP4HA2‑AS1を過剰発現させても損傷が悪化しなくなり、このRNAの効果がこの経路に結び付くことを確固たるものにしました。
三部構成の分子連鎖
さらに掘り下げるため、チームは生化学的な“釣り”手法でP4HA2‑AS1に物理的に結合するタンパク質を同定しました。その中で際立っていたのがTRIM32で、他のタンパク質にユビキチンという小さな『旗』を付ける酵素です。RNAはTRIM32に結合して分解から保護し、腎細胞内のその量を上昇させます。安定化したTRIM32は、次にULK1に特定のタイプのユビキチン鎖(K63鎖)を付加します。この鎖はULK1を破壊に送り込むのではなく、むしろ機能を高めてオートファジーの誘導能を強化します。研究者らがマウスでTRIM32を除去するか、腎細胞でこれをサイレンシングすると、瘢痕化と過剰なオートファジーはいずれも減少しました。P4HA2‑AS1を阻害した細胞にTRIM32を再導入すると瘢痕反応が部分的に回復し、この酵素が連鎖の重要な中間リンクであることを示しました。 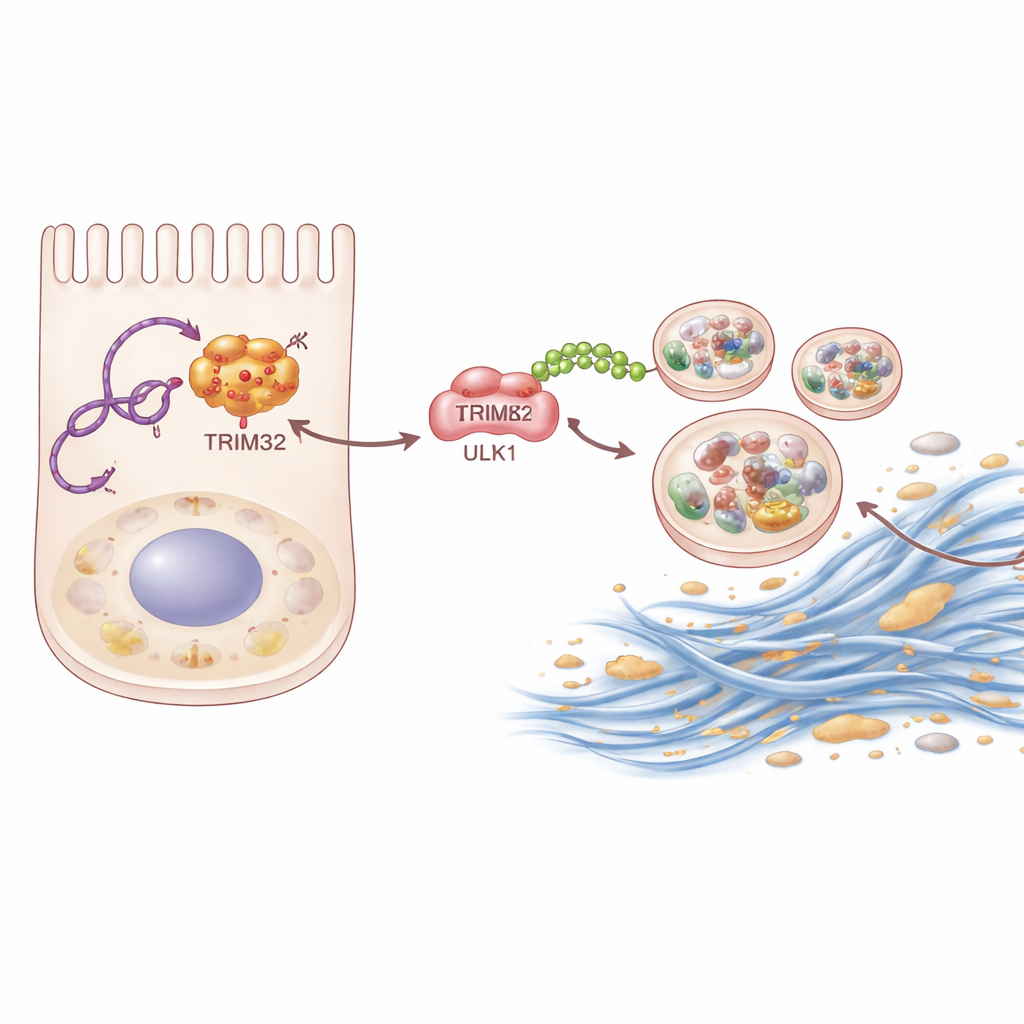
柔らかい腎臓へ向かう新たな道
総じて、本研究は長鎖非翻訳RNA、タンパク質のタグ付け、細胞のリサイクルを腎臓の瘢痕組織の蓄積につなぐ、これまで知られていなかった分子経路を明らかにしました。損傷した腎臓ではP4HA2‑AS1が上昇し、TRIM32を安定化させ、ULK1を過剰に活性化してオートファジーを有益な範囲を超えて駆動し、最終的に線維性タンパク質の蓄積と機能喪失を促します。専門外の読者に向けた結論はこうです:腎臓の瘢痕化は不可避なブラックボックスではなく、薬で狙える可能性のある同定可能なスイッチによって駆動されているということです。P4HA2‑AS1–TRIM32–ULK1軸を標的にし、問題のRNAを減らす、TRIM32を抑える、あるいはULK1の活性を微調整することで、いつか慢性腎臓病の進行を遅らせたり予防したりする新たな治療法が提供される可能性があります。
引用: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
キーワード: 慢性腎臓病, 腎線維症, オートファジー, 長鎖非翻訳RNA, 腎尿細管