Clear Sky Science · ja
ヒストン脱メチル化酵素KDM7Aは線維化誘導性マクロファージの分化と肺線維症の進行を負に制御する
肺の瘢痕化が誰にとっても重要な理由
肺に頑固な瘢痕ができると、呼吸は日常的な苦労になります。この状態は肺線維症と呼ばれ、何百万人もの人に影響を及ぼし、現在のところ治癒法はなく、損傷の進行を遅らせる薬があるのみです。本研究では、マクロファージと呼ばれる免疫細胞の内部に存在する、肺の瘢痕化を抑える分子レベルの“ブレーキ”が新たに明らかにされました。このブレーキの理解は、肺線維症だけでなく、有害な瘢痕化と制御不能な炎症が連動する他の疾患に対する新たな治療法への道を開く可能性があります。
形を変える免疫細胞の物語
マクロファージは組織を巡回し、破片を除去し、損傷修復を助ける最前線の免疫細胞です。しかし彼らは形を変える存在でもあり、状況によっては炎症を促進する戦闘型になり、別の状況では瘢痕形成を促す修復型になります。特に瘢痕促進型と呼ばれるプロフィブロティック・マクロファージ(Fib-Mac)は肺線維症と強く関連しています。これらの細胞は線維芽細胞を活性化する分子を産生し、線維芽細胞は過剰なコラーゲンやその他のマトリックス成分を沈着させて肺を徐々に硬化させます。著者らは、マクロファージ内部の遺伝的“設定”が、これらの危険なFib-Macになるか、よりバランスの取れた保護的な状態に留まるかをどのように決めているのかを明らかにしようとしました。
ゲノムに隠されたエピジェネティックなブレーキ
チームはまず、DNAの折りたたみや遺伝子のオン・オフを微調整する既知のエピジェネティック因子を数百個スキャンしました。ヒトおよびマウスのマクロファージでRNAシーケンシングを行ったところ、マクロファージが線維化を促す修復状態へと押し込まれるときに、KDM7Aという酵素が強く活性化されることが分かりました。KDM7Aは“ヒストン脱メチル化酵素”であり、DNAが巻き付くヒストンタンパク質から特定の化学タグを除去します。この発現パターンは、KDM7Aがマクロファージが瘢痕促進のアイデンティティへと傾き始めた際に作動する内部の負帰還ブレーキとして働く可能性を示唆していました。
これを検証するために、研究者らはKdm7a遺伝子を欠損させたマウスを用い、化学療法薬ブレオマイシンによって肺損傷を誘導しました(肺線維症の標準的モデル)。損傷の初期では、正常マウスとKdm7a欠損マウスの肺組織は類似して見えました。しかし3週間後には、Kdm7aを欠くマウスでより広範な瘢痕形成、小さな肺胞の崩壊、線維化を定量化する“Ashcroftスコア”の上昇が認められました。コラーゲン産生やその他の線維化関連経路に関わる遺伝子はこれらのノックアウトマウスでより活性化しており、Kdm7aの消失が肺を長期にわたる有害な瘢痕形成に対して脆弱にすることを裏付けました。
KDM7Aがマクロファージを瘢痕促進運命からどう逸らすか
単一細胞RNAシーケンシングを用いて、著者らは損傷を受けたマウスの個々の肺細胞を詳細に解析しました。その結果、Kdm7aが欠損すると肺の支持組織に存在する特定のマクロファージサブセットが劇的に拡大し、Arg1、Spp1、Trem2といった遺伝子を発現する強いFib-Macシグネチャを帯びることが分かりました。培養マクロファージでの追加実験は、Kdm7aを除去するとFib-Macマーカー遺伝子が増強され、コラーゲン産生や持続的な活性化を支える代謝経路へと細胞の代謝が再配線されることを示しました。言い換えれば、KDM7Aは通常、マクロファージを線維化を促す状態へと駆り立てる遺伝的・代謝的プログラムの両方を抑制しています。
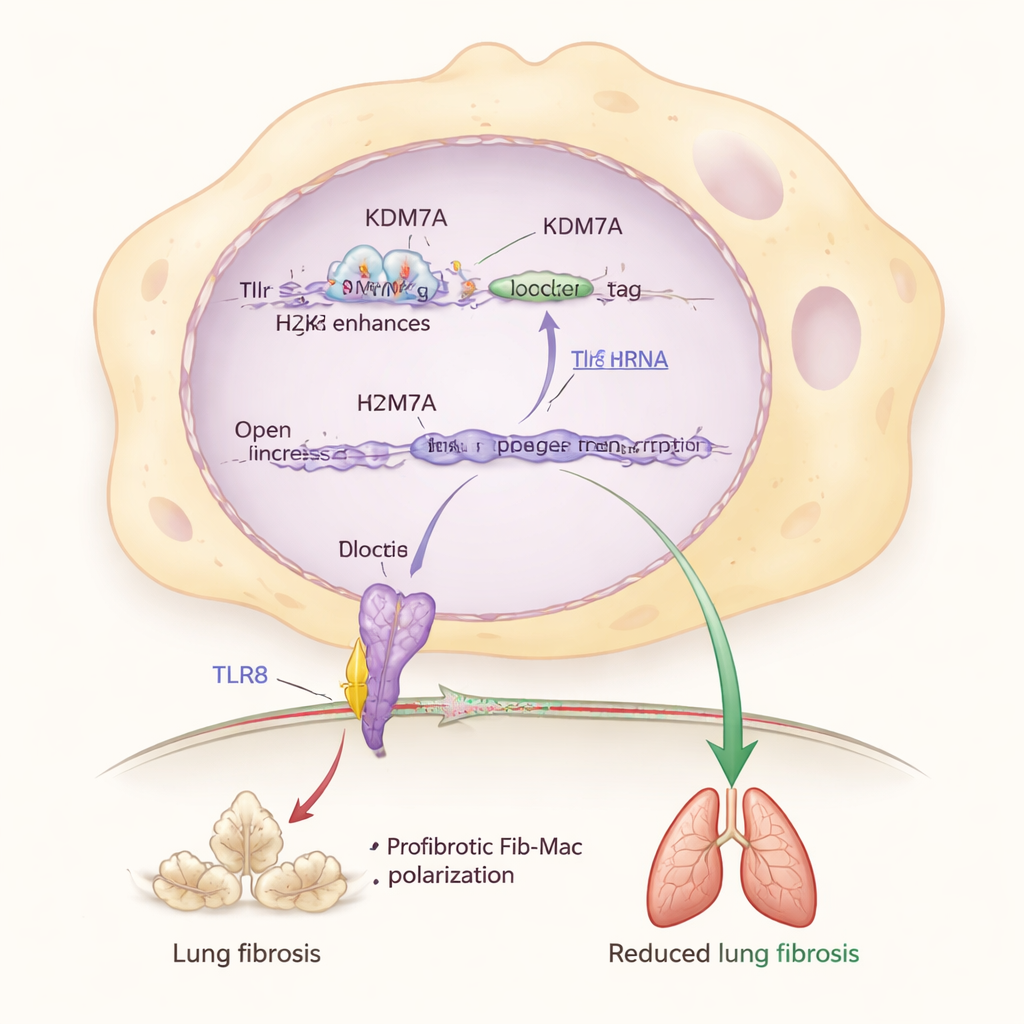
さらに掘り下げると、研究者らはこのブレーキ系の重要なパートナーとしてTLR8というセンサータンパク質を同定しました。TLR8は免疫細胞内のRNA断片を検出します。KDM7AはTlr8遺伝子近傍のエンハンサー領域から抑制的な化学マーク(H3K27me2)を除去することでTlr8遺伝子の発現を維持するのに寄与していることが分かりました。Kdm7aが無効になるとこのマークが蓄積してTlr8レベルが低下し、Fib-Macの特徴が強まります。マクロファージでTlr8を直接減少させても同様に線維化的アイデンティティが促進され、一方でTLR8を活性化または過剰発現させると、Kdm7aが欠損している場合でも細胞を元に戻すことができました。これにより、KDM7A–TLR8経路が過剰な瘢痕化から肺を守る分子回路の中心に位置することが示されます。
老化した肺からヒト疾患へ
これらの発見をヒトに結びつけるため、研究チームは線維化肺疾患患者の肺組織を調べました。非疾患対照組織と比べて、線維化した肺にはFib-Macマーカーを持つマクロファージがはるかに多く存在しましたが、これらの細胞ではKDM7AおよびTLR8の発現が著しく低下していました。特発性肺線維症患者の既存の単一細胞データセットを再解析しても同様のパターンが確認され、Fib-Macシグネチャが上昇するにつれKDM7A発現が低下していました。さらにマウスの大規模アトラスを探索すると、雄のマクロファージにおけるKdm7aおよびTlr8の発現は加齢とともに低下し、これは高齢男性における肺線維症のリスク上昇を反映していました。これらは、年齢や性に関連したKDM7A–TLR8ブレーキの弱体化が、誰が重度の肺瘢痕化に脆弱かを部分的に説明する可能性を示唆します。
将来の治療への意味
簡潔に言えば、この研究は我々の免疫系に、修復に役立つ細胞が過度に暴走して永続的な瘢痕の駆動要因になることを防ぐ内部の安全機構があることを示しています。KDM7AはTLR8を介してマクロファージがプロフィブロティックなモードにロックされるのを防ぎ、損傷後に柔軟で機能的な肺組織を維持するのに寄与します。このシステムが遺伝的欠損、加齢、その他の要因で崩れると、マクロファージは“瘢痕増幅因子”になりやすく、線維化を悪化させます。エピジェネティックなブレーキの存在を明らかにしたことで、本研究は将来的にKDM7A活性を高める薬剤、あるいはその効果を模倣する手法、あるいは慎重にTLR8を刺激する治療が、既存の抗線維化療法を補完し、進行性で生命を脅かす肺瘢痕化に対するより良い防護を提供する可能性を示唆しています。
引用: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
キーワード: 肺線維症, マクロファージ, エピジェネティクス, KDM7A, TLR8