Clear Sky Science · ja
シアル脂質の認識とSiglec-6の結合は細胞膜との相互作用に依存する
細胞が「味方」と「敵」を見分ける仕組み
免疫系は常に自分の細胞を監視し、落ち着いているべきか攻撃するべきかを判断しています。この監視の重要な一端は、細胞表面にある糖鎖構造を認識することにあります。本研究は、ヒトの免疫受容体の一つであるSiglec-6が、これらの糖鎖だけでなく周囲の細胞膜自体も利用して、結合の判断を特に精密に行っていることを明らかにしました。その一風変わった戦略は、体内の免疫シグナルの微調整の説明に寄与するとともに、標的を絞った治療法の新たな道を開く可能性があります。
免疫細胞上の糖を感知する見張り役
Siglecは免疫細胞上に存在し、シアル酸を含む糖鎖を認識する受容体群で、「自己」と「非自己」を識別する役割を果たします。多くのSiglecはこれらの糖と結合するために、アルギニンという単一の高度に保存されたアミノ酸残基に依存します。このアルギニンを除くと通常は結合が失われます。しかしSiglec-6は例外的で、以前の研究ではこの重要なアルギニンが変異していても糖を含む脂質の一部に結合できることが示されていました。本研究は、Siglec-6がなぜそのような規則を破ることができるのか、そしてそれが肥満細胞、記憶B細胞、ヒト胎盤細胞における役割にとって何を意味するのかを解明することを目的としました。
Siglec-6が探している特別な脂質
細胞表面では、関連する糖鎖はタンパク質にも脂質にも提示されます。本研究はガングリオシドと呼ばれる糖脂質群、特にGM1、GM2、GM3という密接に関連する3種類に焦点を当てています。これらはいずれも膜から突き出したシアル酸で終端した「ヘッド」を一つ持ちます。以前の実験では、Siglec-6は膜の一部として存在するGM1には強く結合する一方、GM2やGM3にはほとんど結合しないことが示されましたが、それらの糖ヘッドは非常に似ています。現実的な膜の詳細な計算機シミュレーションにより、著者らはGM1とGM3のシアル酸が同様に露出してアクセス可能であることを確認しました。言い換えれば、単純な物理的アクセス性がGM1を特別にしているわけではありません。代わりに、GM1の先端にある追加の糖――末端ガラクトース――がシグレック6を膜に対して正しく位置づける重要な要素として浮かび上がりました。
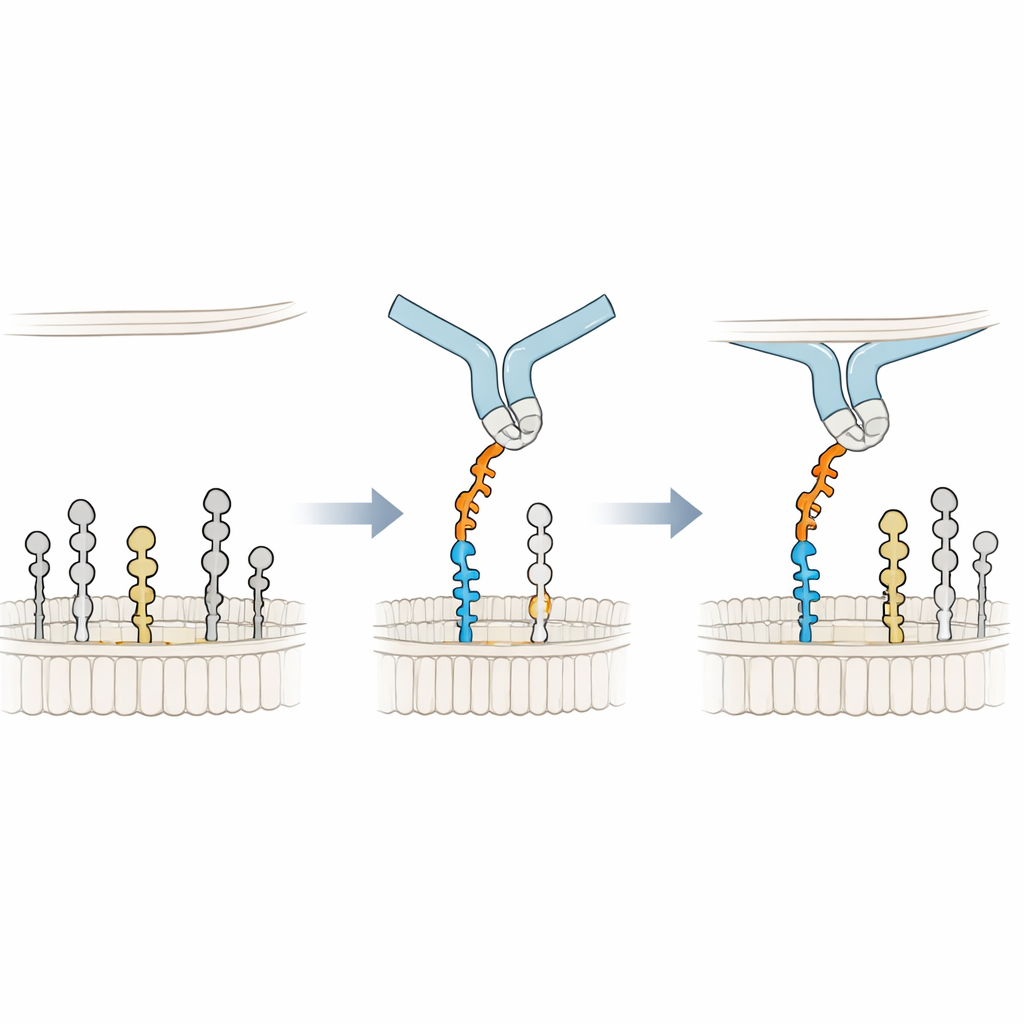
より強い把握のために膜に寄りかかる
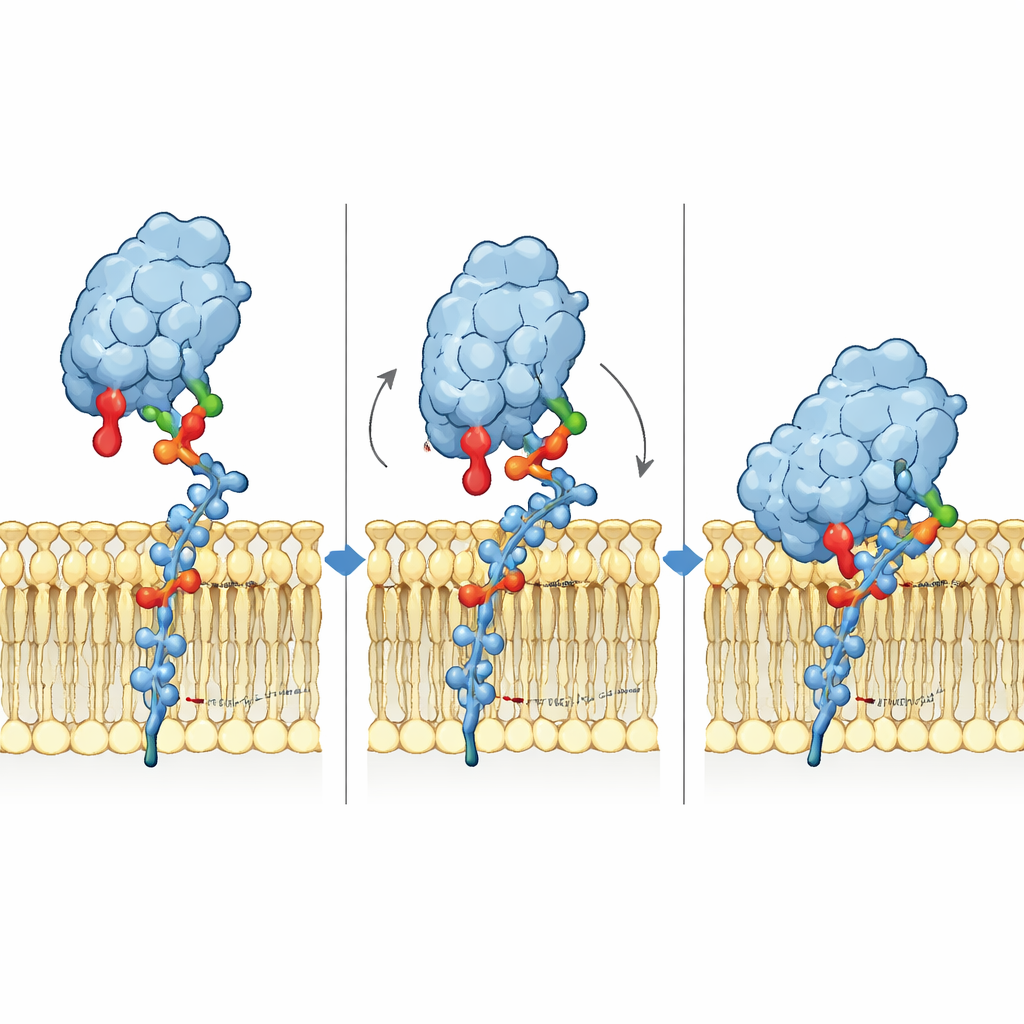
結合機構を原子レベルで理解するため、研究者らは膜中でGM1に結合するSiglec-6の3Dモデルを構築し、長時間の分子動力学シミュレーションを行いました。その結果、Siglec-6は依然としてその典型的なアルギニン(Arg122)を用いてシアル酸と接触するものの、その接触は時間とともに断続的であることがわかりました。複合体を安定化しているのは新しい要素で、近傍のトリプトファン(Trp127)が膜の脂肪部分に食い込み、隣接するリジン(Lys126)が周囲脂質の帯電したヘッドグループと相互作用します。この膜への“くさび”は通常の糖–アルギニン相互作用を補い、脂質環境から結合エネルギーを事実上借りる働きをします。GM1の末端ガラクトースを除いてGM2を模した場合、Siglec-6の柔軟なループが空いた空間に入り込み、受容体を膜から引き離してこの膜補助的な把握を破壊し、安定した結合が失われる理由を説明しました。
機構を検証する実験
チームは次に、これらの計算上の示唆を生細胞および生化学的アッセイで検証しました。彼らは細胞に正常型または変異型のSiglec-6を発現させ、GM1を含む蛍光リポソームや小さな脂質ディスクに対する結合性を測定しました。典型的なアルギニンを変異させると、GM1が膜に存在する状況では結合はわずかに減少するにとどまり、Siglec-6がその環境でこの残基のみに依存していないことを確認しました。対照的にTrp127を変異させるとGM1含有リポソームへの結合はほぼ完全に消失し、Trp127とLys126の両方を変異させると結合はほとんど消えました。しかし同じ変異体は膜外で提示されたGM1類似の糖には正常に結合し、Siglec-6の基本構造は保たれていることが示されました。ネイティブ質量分析では、Siglec-6がGM1だけでなく一般的なホスホリピッドにも結合できること、そしてこの脂質相互作用はTrp127を除去すると消えることが明らかになりました。驚くべきことに、Siglec-6はGM1を欠く「裸の」リポソームにもTrp127依存で付着し得ることが示され、まず膜をサンプリングし、その後GM1に出会うと固定化される可能性を示唆しています。
遊離糖が語る別の物語
同じ三つのガングリオシドを膜の一部ではなく遊離した糖断片としてテストした場合、Siglec-6は他のファミリーと似た挙動を示しました。溶液中ではGM1、GM2、GM3に対していずれも同様に弱い親和性で結合し、典型的なアルギニンが必須でした。Arg122の変異は結合を大きく減少させた一方で、Trp127の変異はほとんど影響を与えませんでした。この対照は、Siglec-6が糖を膜上で出会うか遊離形で出会うかに応じて実効的に機構を切り替えることを示しています。膜上では糖ヘッド、GM1の末端ガラクトース、直接的な膜接触の協調的な連携に依存し、溶液中では古典的なアルギニン中心の認識様式に戻ります。
免疫制御にとっての意義
総じて、この研究はSiglec-6が膜の物理的文脈を利用して特異性を研ぎ澄ます精緻なセンサーであることを明らかにしました。周囲の脂質に部分的に係留することで、非常に似たガングリオシドの中からGM1を選択的に認識し、一般的な「シアル酸読み取り」受容体を特定の表面パターンを高精度で検出する装置に変えています。この膜補助的戦略はこれまで研究されたSiglecの中ではユニークに思われ、免疫応答を調節する特定の糖脂質シグネチャーや胎盤のような特定組織をSiglec-6が走査する助けになっている可能性があります。この二重の認識モードの理解は、Siglec-6の糖と膜の感知という異例の組み合わせを利用した治療法や診断ツールの設計に役立つでしょう。
引用: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
キーワード: Siglec-6, ガングリオシド, 細胞膜, 糖脂質の認識, 免疫制御