Clear Sky Science · ja
ATM阻害はAAV誘導のアポトーシス経路活性化を抑えることでノックイン効率を向上させる
遺伝子編集をより確実にするために
CRISPR遺伝子編集は遺伝性疾患の治療や耐性作物の開発、強力な研究ツールとして期待されています。しかし、その最も有用な手法のひとつである、ゲノム上の特定部位に新しいDNAを正確に挿入する「ノックイン」は依然として効率が低いままです。本研究は、なぜある細胞は新しいDNAを受け入れやすく、他はそうでないのかを探り、アデノ随伴ウイルス(AAV)という遺伝子治療で主要に使われる供与体を用いる場合に、正確な改変をより頻繁に行わせる方法を明らかにします。
DNA修復をリアルタイムで観察する
正確な遺伝子挿入を助ける要因や妨げる要因を理解するために、研究者らはマウス胚性幹細胞内に複雑な「ダッシュボード」を構築しました。この三重レポーターシステムは三色の蛍光マーカーを使い、同じ細胞内でCRISPR切断の有無、正確なノックインの発生、あるいはドナーDNAがより粗い修復経路で組み込まれたかを追跡します。フローサイトメトリーで色の組合せを読み取ることで、テンプレートに基づくクリーンな編集をエラーが多い挿入や未編集の細胞から分離できます。この並行追跡により、古いPCRベースの試験よりもはるかに高い解像度で各結果に寄与するDNA修復経路を描くことが可能になりました。
二つのドナーDNA、二つの全く異なる反応
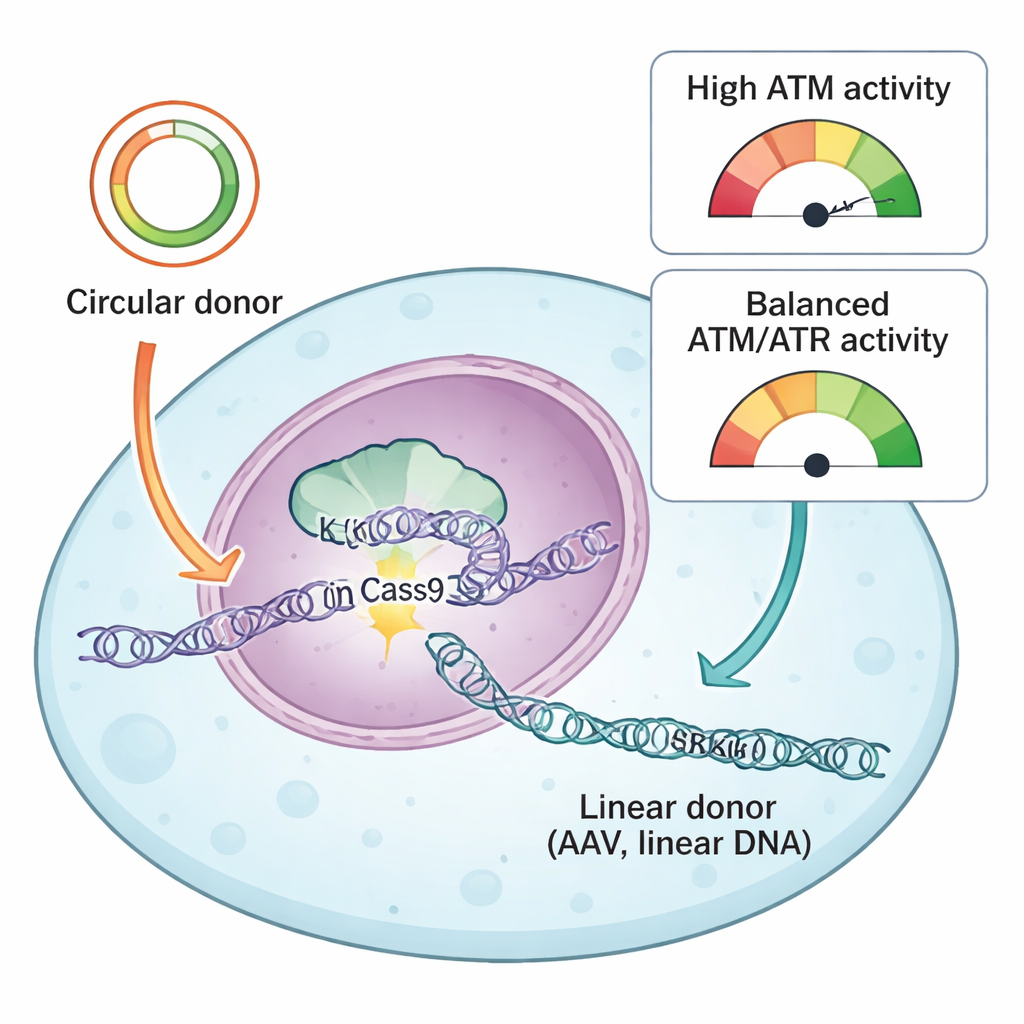
チームはCRISPR修復を導くために一般的に使われる二種類のドナーDNA、すなわち円形プラスミドと線状のAAV由来DNAを比較しました。どちらも新しい配列を挿入する位置を示す相同アームを持ちますが、細胞内に入る物理的な形が異なります。円形プラスミドは閉ループの二本鎖DNAである一方、AAVドナーは通常一本鎖の線状分子として到達します。彼らはこのレポーター系とDNA損傷応答タンパク質を標的とする薬剤ライブラリを用いて解析し、ある重要なタンパク質であるATRが両方のドナータイプでノックイン成功に一様に不可欠であることを見いだしました。ATRを阻害すると正確な挿入が著しく減少し、逆にKEAP1–NRF2経路を介してATR活性を穏やかに高めると、特にAAVドナーでノックイン効率が上がりました。
DNA保護が裏目に出るとき
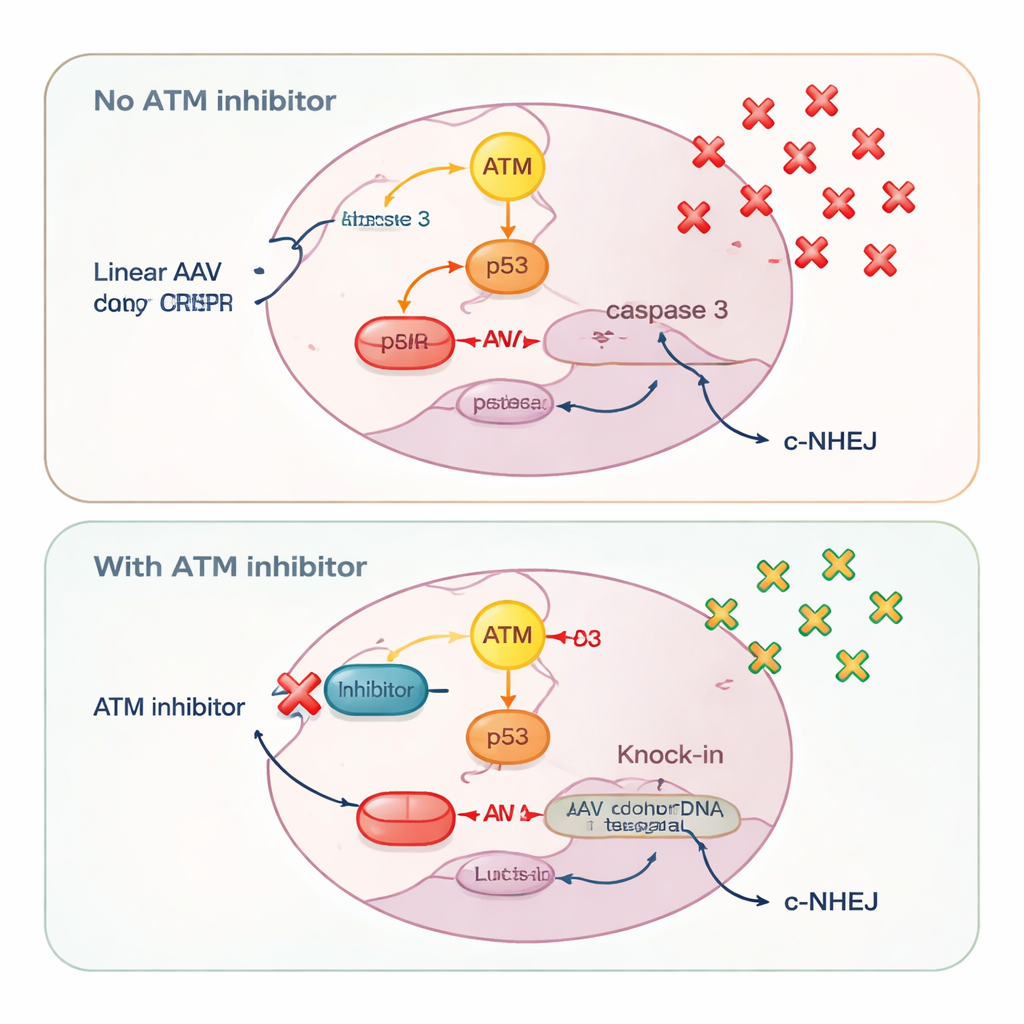
別のDNA損傷センサーであるATMは、ドナー依存的にきわめて異なる振る舞いを示しました。円形プラスミドドナーでは、ATM阻害は正確なノックインとエンド結合による挿入の両方を減少させ、二本鎖切断の修復を助けるという古典的な役割と一致しました。しかし線状DNA――AAV、自家相補型AAV、あるいは直線化されたプラスミドいずれの場合でも――ATM阻害は逆の効果を示し、ノックイン効率を高めました。研究者たちはこの効果を、細胞が線状DNAの急増をどのように解釈するかに帰しました。高用量のAAVは強くATMを活性化し、それがp53とカスパーゼ3をオンにしてプログラム細胞死を誘導しました。多くのコピーのドナーDNAを取り込んだ細胞ほどノックイン成功の確率が高い一方で、同時にこの警報系によって殺されやすいという状況が生じていたのです。
最も準備の整った細胞を救う
ATM阻害剤を加えることで、研究者らはATM–p53–カスパーゼ3の死亡経路を抑制しました。これにより高量のドナーDNAを保持する細胞が救われ、正確なノックインを完了するのに十分な時間生存する細胞が増えました。ウイルスゲノムコピー数の測定は、ATM阻害が細胞内に保持されるAAV分子の数を増やすことを裏付けました。同時にATM阻害は、古典的な非相同末端結合という高速で切断をつなぐ修復経路をわずかに弱め、これがコア酵素であるDNA-PKの活性低下として示されました。この競合する修復選択肢を弱めることが、より多くのCRISPR切断を迅速なパッチ修復ではなく相同組換えベースのノックインへと誘導しました。
今後の遺伝子治療にとっての意味
非専門家向けの要点は、私たちをDNA損傷から守る同じ細胞保護機構が、特に大量のウイルス性ドナーDNAが用いられる場合に、意図せず正確な遺伝子編集を妨げる可能性があるということです。本研究は、そのような保護機構を穏やかに調整する――ATRを維持しつつ線状ドナー(たとえばAAV)が存在する間だけATMを一時的に抑える――ことでCRISPRノックインの信頼性と効率を高められることを示しています。こうした戦略は、遺伝子治療、細胞工学、疾患モデルの改良に寄与し、より多くの細胞が意図した変化を受け入れつつ不必要な細胞喪失を避ける助けとなるでしょう。
引用: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
キーワード: CRISPRノックイン, AAV遺伝子編集, DNA損傷応答, ATM阻害, ゲノム工学