Clear Sky Science · ja
CISH:既存および新興のがん免疫チェックポイントとの比較と併用における重要な細胞内チェックポイント
がんと闘う細胞のブレーキを外す
がん免疫療法は多くの患者の見通しを変えましたが、それでもなお大部分の人々がほとんど利益を得られないか全く得られないのが現実です。本研究は、体内のT細胞—免疫系の実働部隊—を強化する新たな手法を探ります。対象はCISHと呼ばれる内部の「ブレーキ」を無効化することです。細胞表面のスイッチに作用する現在の薬とは異なり、この戦略は細胞内部に埋もれた制御系を標的とし、がんが隠れようとする場合でも改変T細胞が腫瘍を見つけ出し破壊する能力を飛躍的に高めることを目指します。
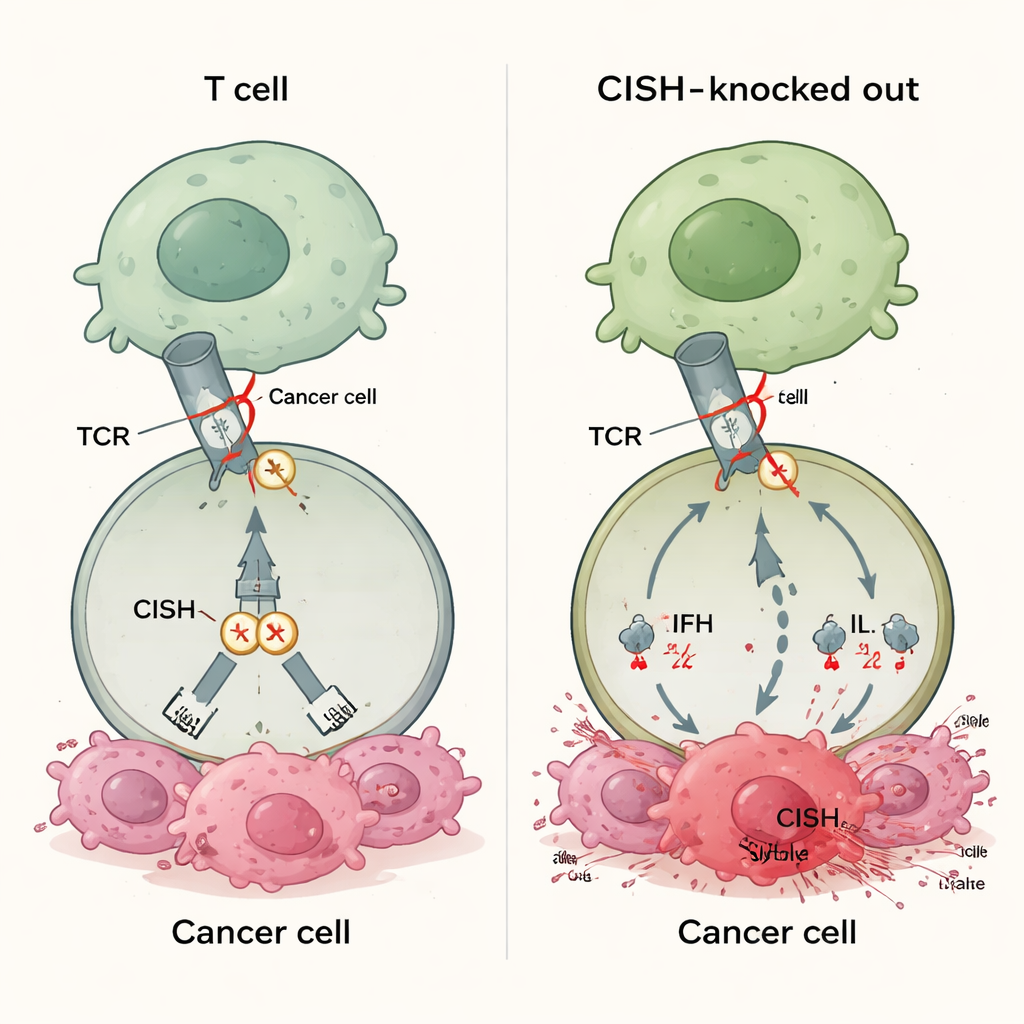
新しいタイプの免疫ブレーキ
承認されている多くの免疫療法薬は、T細胞表面のPD-1のようなタンパク質を阻害します。これらの薬は腫瘍が対応するリガンド(例:PD-L1)を示している場合にのみ働き、多くのがんはそもそも十分な量のそのようなパートナーを発現しないか、時間とともにそれを失います。これが今日のチェックポイント療法に30~60%の患者が反応しない理由の一端を説明します。CISHはT細胞内部に位置する別のクラスのブレーキに属します。T細胞受容体が標的を感知するとCISHがオンになり、重要なシグナル伝達タンパク質の分解を促して信号を弱めます。この作用は腫瘍由来のリガンドに依存しないため、CISHをオフにすることで、PD-L1の状態や他のバイオマーカーにかかわらず、多くのがんタイプでT細胞応答を強化できる可能性があります。
既存のチェックポイントとの直接比較
研究者らはCRISPR遺伝子編集を用いてCISHを除去し、得られたT細胞をPD-1欠損や他のいくつかの細胞内ブレーキ欠損の細胞と比較しました。T細胞を弱く刺激した条件—抗原をわずかしか示さない腫瘍を模す状況—では、CISH欠損細胞はインターフェロンγ、TNF-α、IL-2などの主要な免疫メッセンジャーをはるかに多く産生しました。これらの細胞はまた“多機能性”が高く、個々のT細胞が同時に複数の役割を果たせることが強力な抗腫瘍活性の特徴です。対照的に、単にPD-1を除去してもこうした低シグナル条件下では効果が見られませんでした。複数の試験において、CISH喪失はRASA2、CBLB、SOCS1、REGNASE1、HPK1、PTPN1/2などの他の候補となる内部チェックポイントをノックアウトするよりも、活性化、殺傷能、持続的な記憶様T細胞の形成を強く高めました。
他の細胞内スイッチとの協働
T細胞シグナルは多くの重複する経路によって制御されているため、チームはCISH除去を他のブレーキの除去と組み合わせることで相加的な利益が得られるかを検討しました。多重CRISPR編集を用いると、CISHをSOCS1、HPK1、またはRASA2とともに削除すると、弱い刺激下で有益なサイトカインの産生がさらに増加することがわかりました。一般的なKRAS変異を用いた腫瘍モデルでは、KRAS特異的受容体で設計したT細胞はCISHを除去するとがん細胞の殺傷能が向上し、CISH喪失をSOCS1またはRASA2の除去と組み合わせるとその効果はより強くなりました。これらの結果は、CISHがT細胞生物学において冗長ではない重要なノードを制御し、選択された相手と協働して腫瘍特異的殺傷を鋭くできることを示唆します。
巧妙ながんに強いCAR-T細胞を作る
次に著者たちは臨床的に重要な設定、すなわちB細胞マーカーCD19を標的とするCAR-T細胞に注目しました。治療逃避のためにターゲットを放出したり減らしたりする腫瘍を模すため、異なるレベルのCD19を発現する白血病細胞を作成しました。CISH欠損のCAR-T細胞は、CD19が希少な場合でもがん細胞を破壊する能力が著しく向上し、さらに活性化や細胞呼び寄せのシグナルを多く分泌しました。同時に、T細胞を弱めたり腫瘍成長を促したりすることで知られる分子(ガレクチン-1、ガレクチン-3、可溶性4-1BB、IL-1α、糖タンパク質EMMPRIN/CD147など)の量は低くなりました。これらの変化は、特に拮抗的で抗原量の少ない腫瘍環境に対してより攻撃的で抑えにくいCAR-T細胞を示唆します。
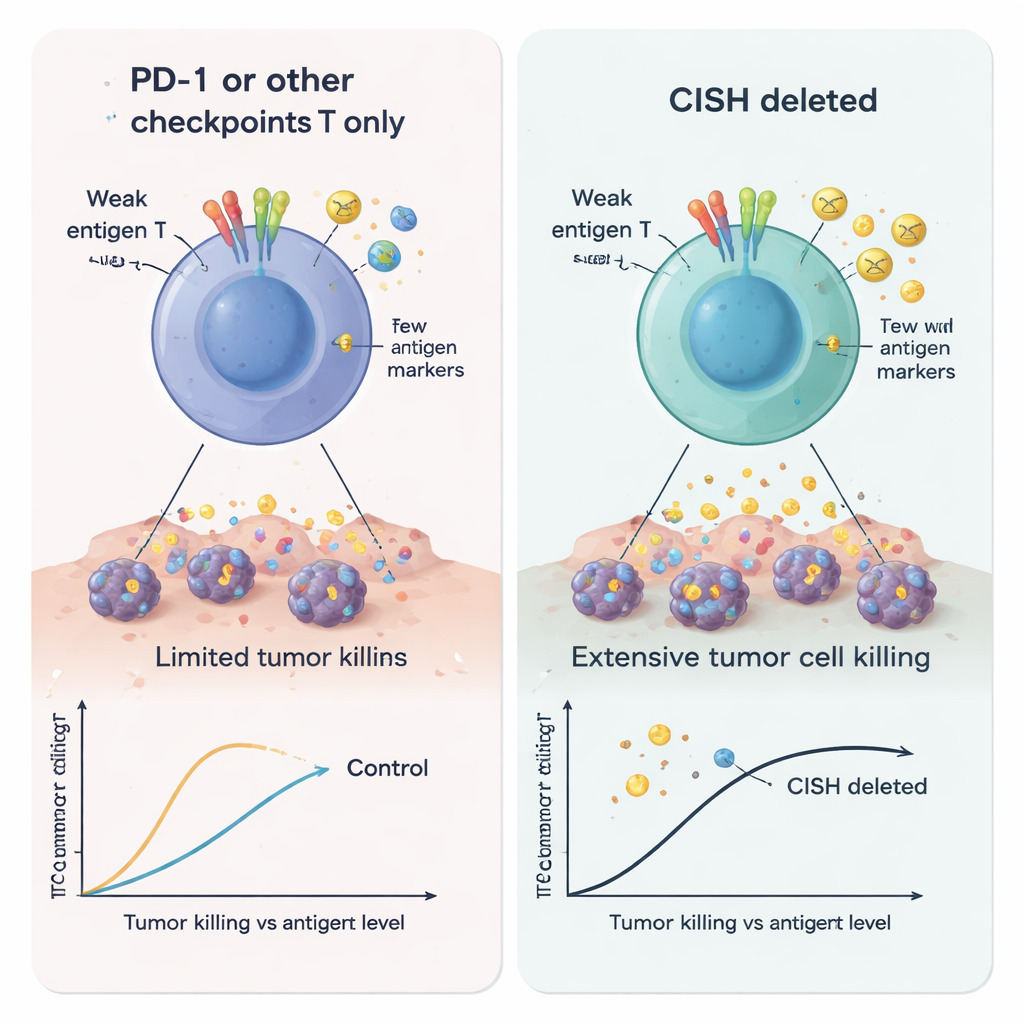
研究室から患者へ
試験管や培養皿を越えて、CISHを標的にするという考えはすでに患者へ到達しています。進行大腸がん患者に対してCISHを除去した腫瘍浸潤リンパ球を用いた先駆的なヒト試験では、複数の既往治療に抵抗していたにもかかわらず完全奏効が得られ、その効果は2年以上続いています。CISHが微弱な腫瘍信号に対するT細胞の感受性を高める強力で薬剤化可能な内部チェックポイントであることを実証することで、この研究はその顕著な臨床成績を説明し、遺伝子編集細胞であれ経口薬であれ、この内部ブレーキを安全に緩めてがん免疫療法の適用範囲を広げる今後の治療開発を支持します。
引用: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
キーワード: がん免疫療法, T細胞, CAR-T療法, 免疫チェックポイント, CRISPR遺伝子編集