Clear Sky Science · ja
α-SNAPの病原性変異は重要な疎水性ループを隠すことで膜脂質結合を損なう
ごく小さなタンパク質の変化が脳発達を乱す仕組み
脳の細胞は常に小さな泡状の小胞に荷物を乗せて輸送しており、それを助けるタンパク質であるalpha-SNAPがその配送を成立させる中心的役割を担っています。マウス系統「hyh」として知られる希少なalpha-SNAPの変異は、脳形成や体液の恒常性に深刻な障害を引き起こします。本研究は一見単純ながら重大な問いを投げかけます:alpha-SNAPの一文字の置換は膜への付着を妨げ、それが脳の異常の重要な原因になりうるのか?
多機能な細胞の荷役作業員
通常、alpha-SNAPは小胞のドック作業員のように働き、小胞が細胞膜と融合して荷物の放出やリサイクルが行えるように助けます。SNAREと呼ばれる一連のタンパク質群やATPを使う機械NSFと協働して膜を引き合わせ、その後システムを次のサイクルにリセットします。この古典的役割に加え、alpha-SNAPはオートファジー(細胞のセルフクリーニング)、細胞死、カルシウム取り込み、エネルギー感知などのプロセスの制御にも関与します。これらの機能はすべて、いずれの形でも膜の油性表面に触れ、部分的に挿入するalpha-SNAPの能力に依存しています。
隠れたループと問題を起こす変異
先行研究は、alpha-SNAPがタンパク質の片端近くにある短い油性の「ループ」を用いて膜にフックすることを示していました。正常なタンパク質ではこのループが外側に突き出し、膜の外層に潜り込むことができます。hyhマウスでは、105番目のアミノ酸が置換されてM105I変異が生じます。著者らはこの変化がタンパク質の立体構造にどう影響するかを計算機シミュレーションで調べました。その結果、変異体はわずかにコンパクトになり、疎水性ループを水や膜から内側にしまい込むようなねじれを生じることが分かりました。その結果、変異体は膜に対してより平坦な角度で近づき、粘着性の低い領域で膜に押し付ける傾向が強まり、接触時間と挿入深度の両方が低下します。結合エネルギーの計算もこれを支持し、野生型は低エネルギーで強く結合する状態に落ち着く一方、変異体はより弱く浅い接触を好みました。
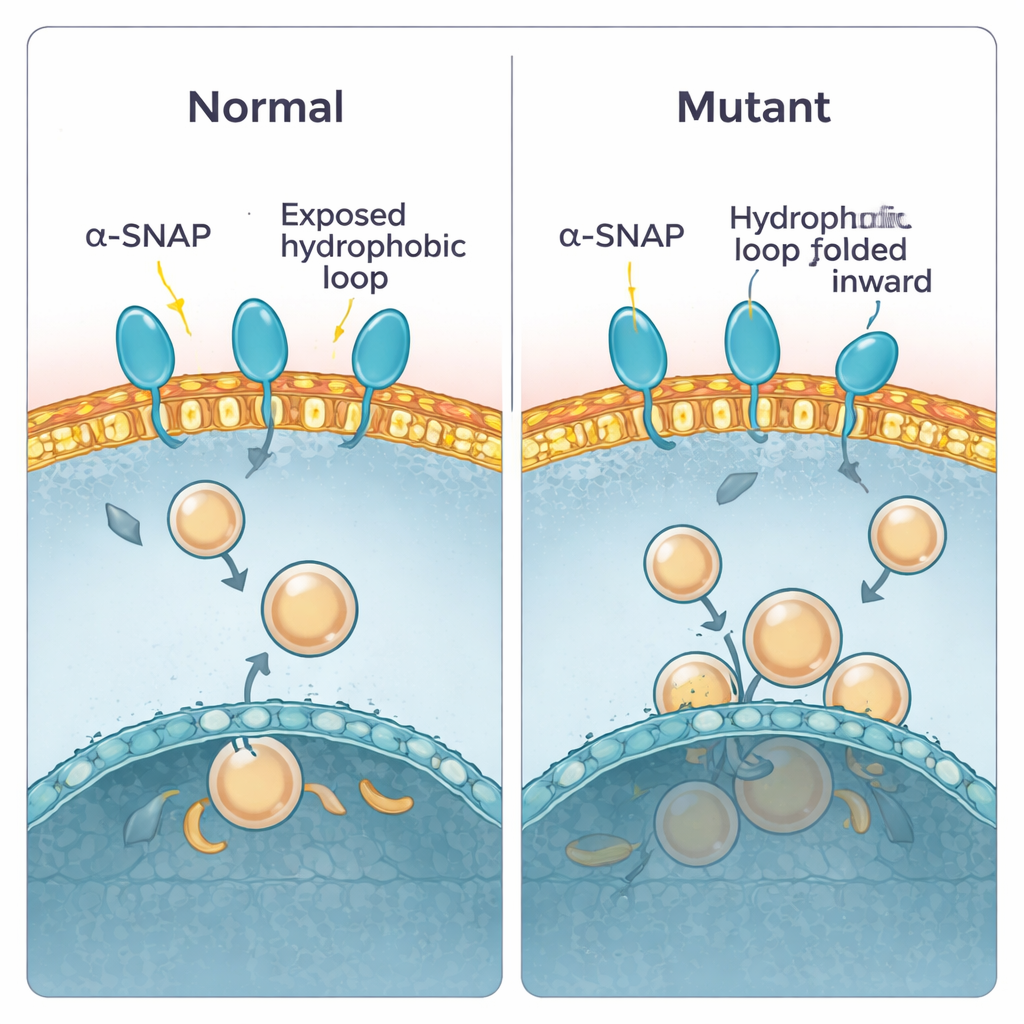
実験室で予測を検証する
これらの予測を確かめるため、研究チームは正常型と変異型のalpha-SNAPを精製して、さまざまな実験系で挙動を試しました。まず、水相と油相に分離する界面活性剤を用いる実験で、水と膜のどちらを選ぶかを模倣しました。正常なalpha-SNAPは均等に分配し、部分的に油性の表面を持つという予想に一致しましたが、変異体は油相へ入りにくく、その油性領域が実際により埋もれていることを示唆しました。次に、細胞から作製した平坦な細胞膜シートとタンパク質を接触させ、結合スポットの数をイメージングしました。ここでも正常型は膜上に点在しましたが、変異型の結合は著しく減少しました。最後に、脳由来脂質で作った人工小胞(リポソーム)を糖度勾配で浮かせる実験を行いました。野生型alpha-SNAPは細胞膜脂質を豊富に含む小胞とともに上方に移動しましたが、変異体は遅れ、細胞内膜組成に近い小胞でない限り結合が弱いままでした。
発達中の脳での影響
研究者らは次に、神経細胞が新生される時期の発達マウス胎児の脳に注目しました。細胞内容物を可溶画分と膜結合画分に分けることで、hyh脳ではalpha-SNAPの総量自体がすでに減少していることを示しましたが、より重要なのは膜に付着している割合が正常マウスに比べて不釣り合いに低い点でした。さらに膜の種類ごとに分画すると、最も大きな喪失は細胞の外側表面であるプラズマ膜に見られ、内部膜はそれほど影響を受けていませんでした。顕微鏡観察でも同様の結果が得られました:正常組織ではalpha-SNAPが既知の表面マーカーと一致する蜂の巣状のパターンで細胞を縁取っていましたが、hyh脳ではこの鮮明な境界標識が薄れ、より拡散した細胞内の光り方に変わり、変異タンパク質が小胞融合やシグナル伝達が活発な細胞縁に留まれないことを示していました。
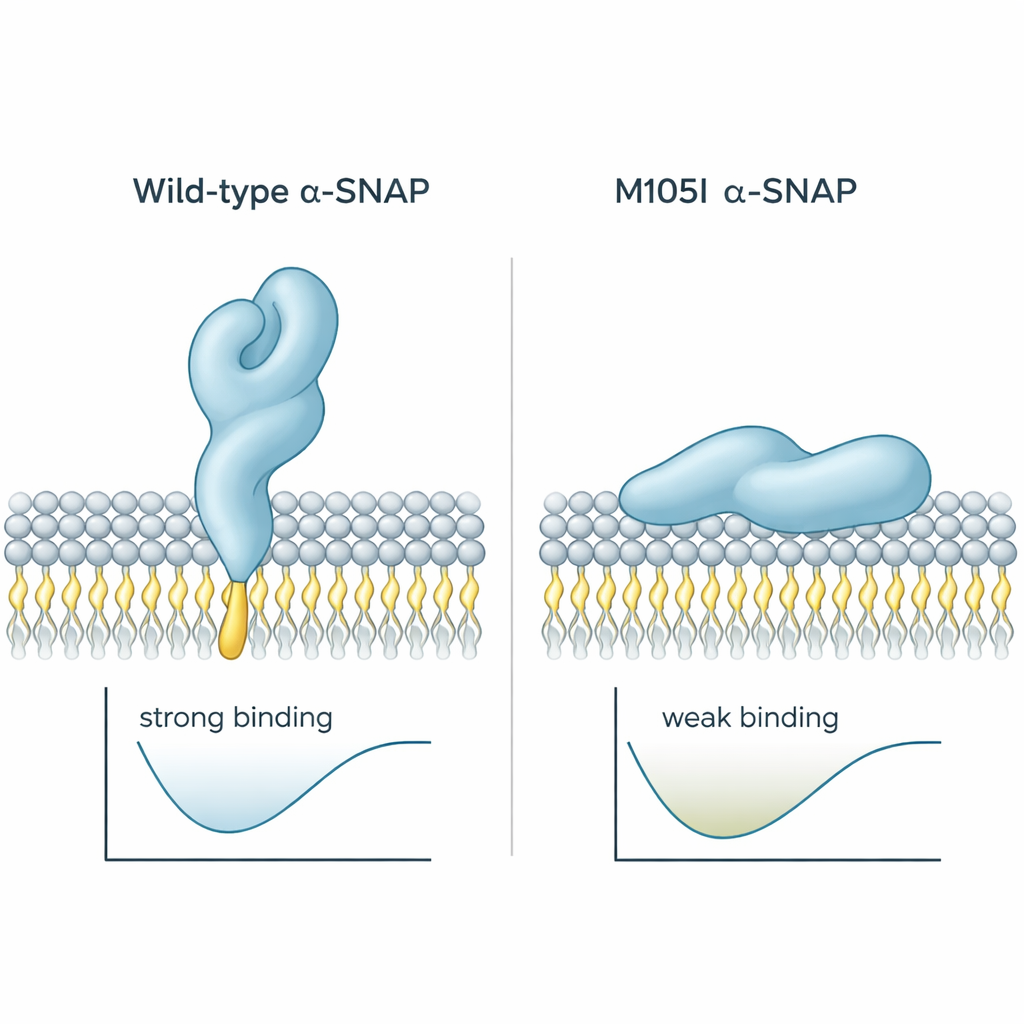
疾患への示唆
総じて、本研究はM105I変異が単にalpha-SNAPの量を減らすだけでなく、膜をつかむ重要なループを隠すように折り畳みを変え、プラズマ膜への掴みを困難にして融合機構を配置する適切な向きを取りにくくすることを示しています。発達中の脳では、細胞表面での正確なシグナル伝達や資材の供給が不可欠であり、この微妙な構造的欠陥がhyhマウスに見られる水頭症や皮質の誤配線などの欠陥に寄与している可能性が高い。専門外の読者へのメッセージは明快です:たった一つのタンパク質の形の微小な変化が、細胞のコミュニケーションの仕方を変え、それによって脳の作られ方を変え得るということです。
引用: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
キーワード: alpha-SNAP, 膜結合, タンパク質変異, 脳発達, 小胞融合