Clear Sky Science · ja
がん細胞におけるAurora kinase A/PHB2相互作用とミトファジーを調節するカプサイシン由来プロヒビチンリガンドの開発
なぜ唐辛子の化合物ががんに関係するのか
唐辛子の辛味はカプサイシンという小さな分子に由来し、これが細胞内のタンパク質に結合します。本研究はその馴染み深いスパイスに対する意外な展開を探ります:研究者たちはカプサイシンを設計し直して、がん細胞の“発電所”であるミトコンドリアに焦点を当て、これらのエネルギー工場を良好な状態に保つ過程を抑える新たな薬剤様分子を作り出しました。がん細胞は増殖を支えるために効率的なミトコンドリアに強く依存しているため、この支援システムを選択的に妨げられれば、新しい抗がん療法の道が開ける可能性があります。
細胞の発電所とその内部の清掃隊
ミトコンドリアは常に新しいユニットの構築と損傷したもののリサイクルのバランスを取っています。リサイクル側はミトファジーと呼ばれ、品質管理のように機能します:傷んだミトコンドリアはタグ付けされ分解され、より健康なものは残ります。多くのがん細胞はこのバランスを乗っ取り、弱いミトコンドリアを除去して大量のATP(細胞のエネルギー通貨)を産生する“スーパーパフォーマー”を濃縮します。しばしば腫瘍で過剰発現するタンパク質Aurora kinase A(AURKA)は最近ミトコンドリア内で、Prohibitin‑2(PHB2)およびオートファジーアダプターのLC3と協働し、ミトファジーを促進してがん細胞の高いエネルギー産生を支える複合体を形成することが見いだされました。
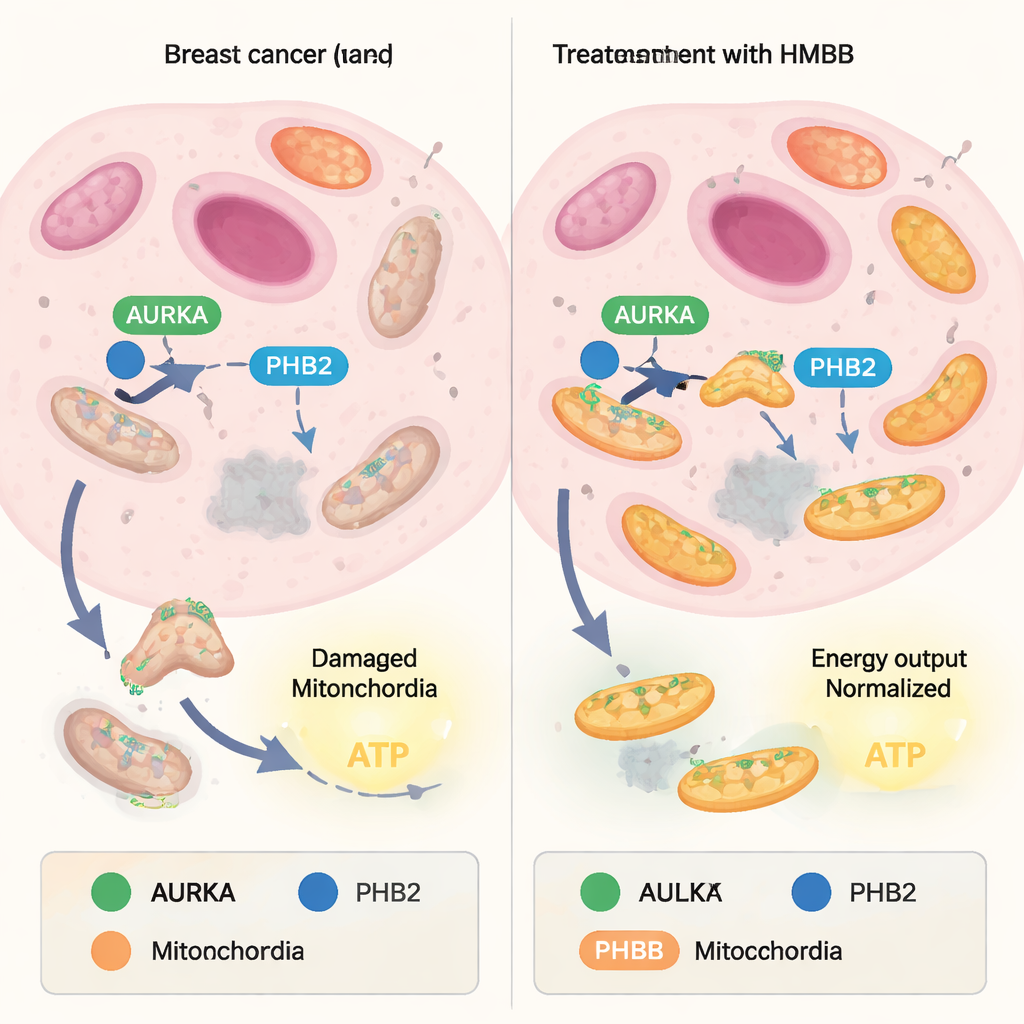
辛味のカプサイシンから作られた分子ツールへ
以前の研究では、キサントフモールという天然化合物がPHB2に結合してAURKA–PHB2–LC3複合体を撹乱し、ミトファジーを阻害してミトコンドリアのATP産生を低下させることが示されていました。しかしキサントフモールの化学構造は薬剤開発には理想的ではありません。本研究では著者らは別の天然のPHBリガンドであるカプサイシンに着目し、それをより実用的なツールに作り変えられるかを検討しました。まず生きた乳がん細胞でイメージング手法(FRET/FLIM)を用い、タグ付けされた二つのタンパク質がどれだけ近接しているかを測ることで、カプサイシンがAURKAとPHB2の相互作用をわずかに弱めることを確認しました。次に彼らは元の構造の“尾”と芳香族の“頭部”を修飾して16種類のカプサイシン由来分子を合成し、それぞれがミトコンドリア内でのAURKA–PHB2の結びつきにどのように影響するかを系統的に試験しました。
タンパク質同士を固定する分子“接着剤”の発見
修飾された分子は顕著に異なる効果を示しました。カプサイシン自体や化合物5のようなものはAURKAとPHB2をより分離させやすくしました。ほとんど影響を与えないものもありました。しかし一部、特に化合物13(後にHMBBと命名)はその逆の効果を示し、AURKAとPHB2の結合を著しく強化しました。計算によるドッキングシミュレーションがこの振る舞いを説明する手がかりを与えました。カプサイシンや化合物5はAURKAの活性部位に入り込み、PHB2と物理的な干渉を起こして両者を引き離すような位置取りをする傾向がありました。対照的に化合物12や13はAURKAの活性部位に収まりつつ、PHB2の既知の阻害ポケットにも同時に接触し、衝突を生じさせませんでした。むしろそれらの形状はAURKAとPHB2の間を橋渡しして複合体を安定化させる“分子接着剤”として働くことを可能にしました。
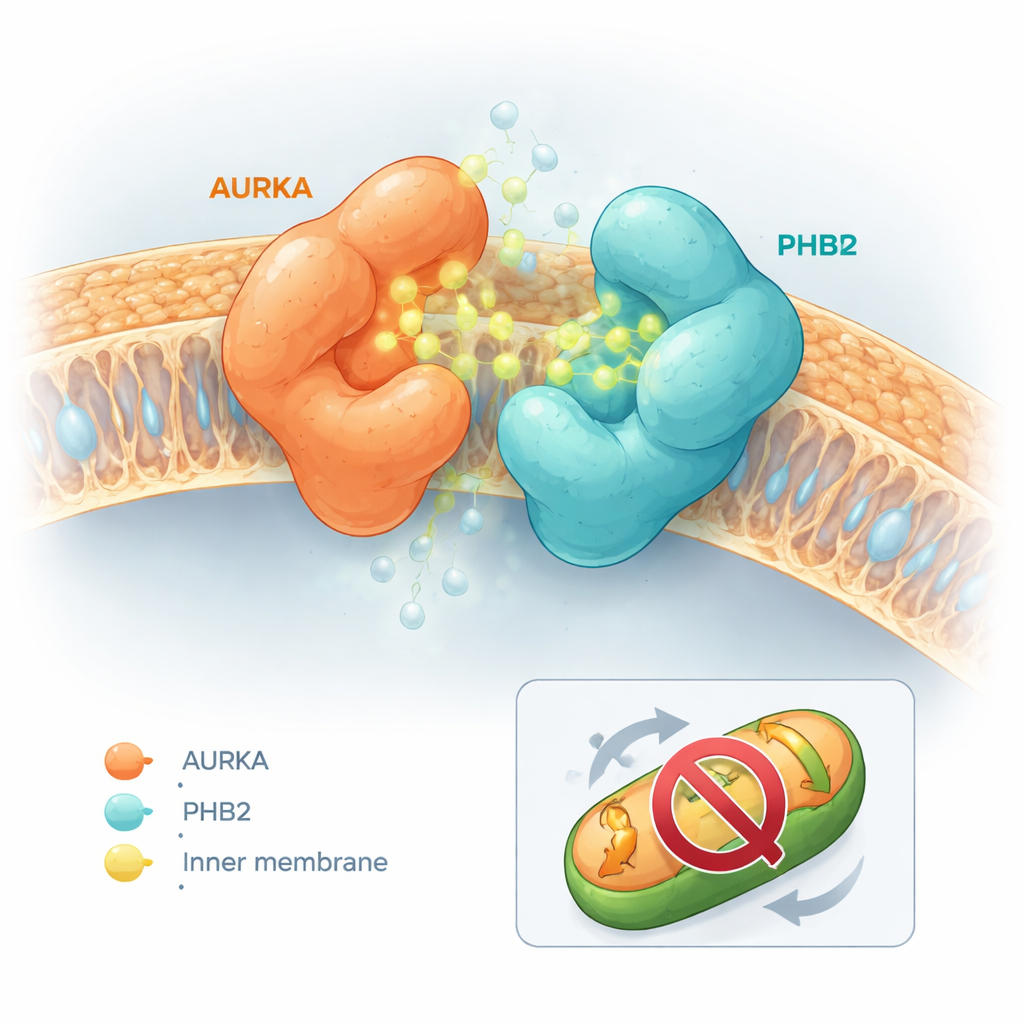
細胞の司令塔を止めずにミトコンドリアの清掃を阻む
重要な疑問は、この分子接着剤の働きが細胞内のどこでもAURKAを無効化してしまい広範な副作用を招くのか、それともより選択的に作用するのか、という点でした。紡錘体を組織する構造である中心体でのAURKA活性を報告する別の蛍光バイオセンサーを用いると、HMBBはこれらの部位でのAURKA活性を抑えないことが観察されました。それでもミトコンドリアのアッセイでは、HMBBは乳がん細胞でAURKAの過剰発現によって通常失われるミトコンドリア量の減少を逆転させました。AURKAを高レベルで産生する細胞ではHMBBはミトコンドリア量を増加させ、AURKA駆動のミトファジーが阻害されたことを示しました。一方、AURKAレベルが低い細胞ではHMBBの影響は小さく、その効果がAURKA–PHB2経路に依存していることが際立ちました。
将来のがん治療にとっての意義
総じて、結果は慎重に設計されたカプサイシン誘導体がミトコンドリア内でのAURKAとPHB2の相互作用を微調整できることを示しています。HMBBや関連化合物は分子接着剤として働き、AURKAとPHB2を通常のミトファジープログラムが進行できない配置で固定しますが、細胞の他の場所でのAURKAの重要な役割を停止させることはありません。一般読者向けに要点を述べれば、著者らはがん細胞が発電所を良好に保つ仕組みを選択的に妨げ得るプロトタイプ分子を作り出したということです。これによりがん細胞のエネルギー供給が弱まり得る一方で、正常な細胞機能は温存される可能性があります。これらの化合物はまだ初期の実験室段階にありますが、ミトコンドリア内の特定のタンパク質相互作用を小さな薬剤様分子で標的化し、多くの腫瘍が依存する代謝上の利点を損なうという有望な戦略を示しています。
引用: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
キーワード: ミトコンドリア, ミトファジー, Aurora kinase A, カプサイシン誘導体, がん代謝