Clear Sky Science · ja
膠芽腫幹細胞は転写的に相関した空間的配置を示す
脳腫瘍での細胞パターンが重要な理由
膠芽腫は最も攻撃性の高い脳腫瘍の一つで、生存率は数十年にわたりほとんど改善していません。多くの研究室は、治療後に腫瘍を再生させる能力を持つ特別な腫瘍細胞、いわゆる膠芽腫幹細胞を研究しています。本研究では、一見単純だが重要な問いが投げかけられました:これらの細胞がシャーレ上でどのように並ぶか――通常の顕微鏡で見えるパターン――は、細胞内でどの遺伝子が活性化しているかを示し、新しい治療法探索を加速できるだろうか?
見た目以上の情報を持つ画像
この考えを検証するため、研究チームは15系統の患者由来膠芽腫幹細胞を平坦なプラスチック培養皿で培養し、約1万7千枚のタイムラプス顕微鏡画像を収集しました。これらの画像は位相差顕微鏡で撮影された標準的なもので、多くの生物学研究室が日常的に得ているものに似ています。一見すると細胞がゆっくり皿を満たしていくだけの写真に見えますが、詳しく見ると細胞の配列に顕著な違いがありました:長く整列して同じ方向を向いた筋状の列を作る系統もあれば、よりランダムな配向や重なり合う層を伴う丸い塊として増殖する系統もありました。これらの視覚的パターンは、細胞の内部の“性格”が集団行動に反映されている可能性を示唆していました。

テクスチャを生物学に翻訳する
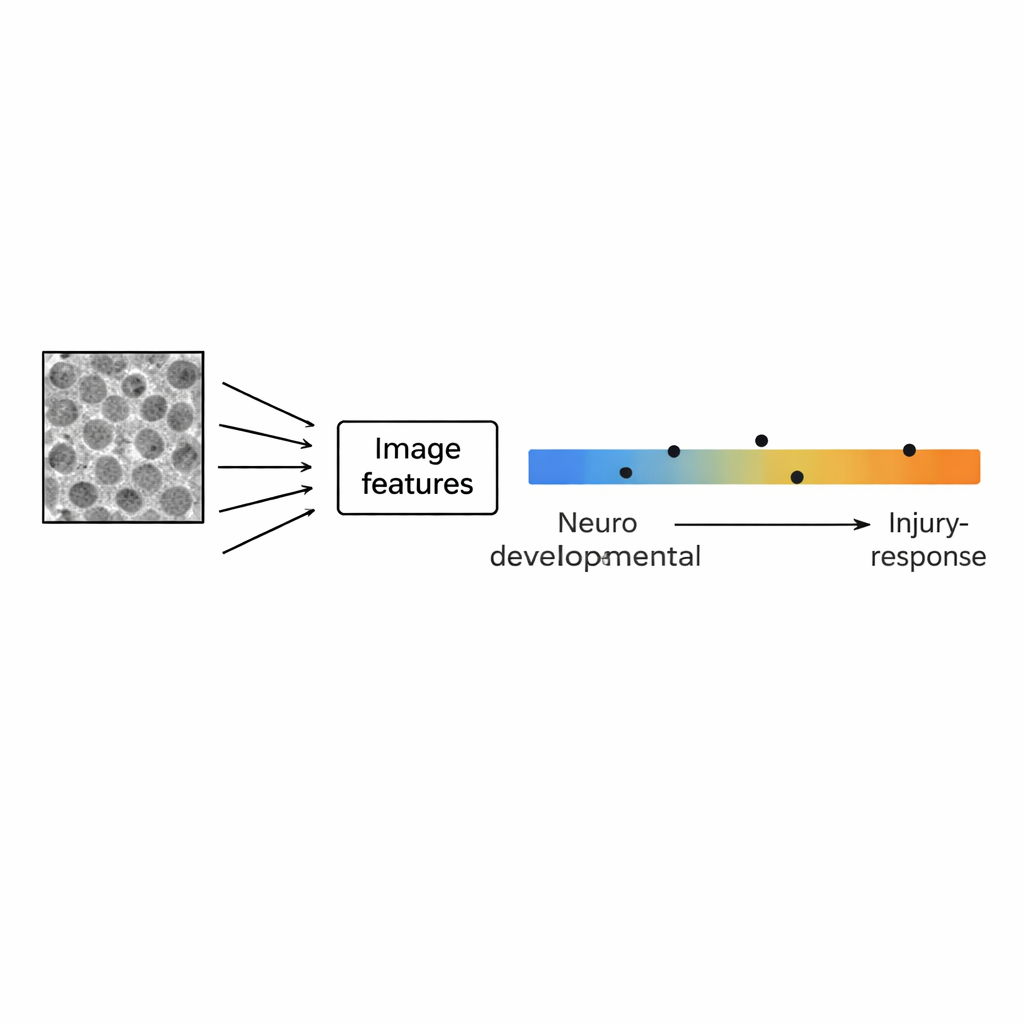
研究者は個々の細胞に注目する代わりに、各画像を全体のパターンとして扱いました。オープンソースのソフトウェアを用いて、各画像を29の数値的特徴に変換しました。これらの特徴は、異なるスケールでの粒状性、隣接ピクセルの類似性の頻度、異なる方向でのコントラストの強さなど、テクスチャや構造を記述するものです。次に、これらの画像ベースのフィンガープリントを同じ細胞系統から得られた遺伝子発現プロファイルと比較しました。比較に用いたのは、脳の発生、正常な脳細胞型、炎症関連状態を捉える111の遺伝子シグネチャです。主成分分析という統計手法により、画像パターンの変動の主軸が既知の生物学的勾配と一致することが明らかになりました:一端では正常な脳の発生に関連する遺伝子(ニューロン、幹細胞、支持性のグリア細胞)が発現し、もう一端では損傷・炎症およびより攻撃的とされる“間葉系(メセンキマル)”的な挙動に結びつく遺伝子が発現していました。
培養が成長しても持続するパターン
細胞画像の解釈における課題の一つは、培養がまばらな状態から高密度へ成長する過程で見た目が劇的に変わることです。著者らはこれに対処するため、画像を9つの細胞密度レベルに分類し、各レベルを別々に再解析しました。驚くべきことに、空間的パターンと遺伝子発現の結びつきはすべての成長段階で維持されていました:播種直後のまばらな皿でもほぼコンフルエントな皿でも、発生様式に似た系統の画像はより滑らかで均一なテクスチャを示す傾向があり、損傷応答寄りの系統はより不規則で不均一な構造を示しました。しかし、信号を担う具体的な画像特徴は密度に伴って変化しました。例えば、小スケールの粒状性を捉える指標は低密度で最も情報量が多く、細胞が混み合うにつれて対称性や均一性を示す特徴が重要性を増しました。これは、外見が変化しても基礎にある生物学がパターンの進化を制約していることを示唆します。
顕微鏡のスナップショットから分子予測へ
画像だけで細胞系統が発生―損傷の勾配上のどこに位置するかを予測できるかを検証するため、研究チームは29の画像特徴のみを入力とし、遺伝子発現に基づくスコアを“正解”とする単純な統計モデルを訓練しました。最も有益な特徴の組み合わせを自動選択するモデルは、元の15系統に対してその勾配を正確に再現し、さらに追加の4系統でも良好な一致を示しました。最も役立った画像特徴にはテクスチャ記述子と構造サイズを示す指標の両方が含まれており、パターン解析から浮かび上がった結果と一致していました。重要なのは、このモデルが標準的なラベルフリー画像、すなわち蛍光色素や特殊顕微鏡を必要としない画像で機能した点で、日常的なイメージングを迅速かつ低コストで細胞状態の指標に変える実用的な道筋を示しています。
今後の脳腫瘍研究への意味
専門外の読者にとっての主要な結論は、がん細胞がコミュニティとしてどのように見え、どのように配置されるかは、彼らが利用している遺伝子の窓口になり得るということです。膠芽腫幹細胞では、単純な明視野画像で、正常な発生脳に似た細胞と、損傷・炎症寄りの状態へシフトした細胞(しばしばより攻撃的な病態に結びつく)を識別するのに十分な情報が得られます。将来的には、この種の画像ベースの“フィンガープリンティング”が、RNAを毎回配列解析することなく、薬剤や遺伝学的変化がどのように細胞をこの勾配上で動かすかを観察することで、迅速にスクリーニングするのに役立つ可能性があります。より広く見れば、生きた細胞培養の構造は単に視覚的に興味深いだけでなく、適切な手法で解読すれば生物学的に意味のある情報を符号化していることを示唆しています。
引用: Ayyadhury, S., Sachamitr, P., Kushida, M.M. et al. Glioblastoma stem cells show transcriptionally correlated spatial organization. Commun Biol 9, 208 (2026). https://doi.org/10.1038/s42003-026-09566-2
キーワード: 膠芽腫幹細胞, 細胞イメージング, 空間的配置, 遺伝子発現, ハイスループットスクリーニング