Clear Sky Science · ja
放射性核種で刺激する動的療法は相補的な免疫原性ネクロプトーシスおよびアポトーシスによるがん細胞死経路を誘導する
がんのトリックを逆手に取る
がんはとくに全身へ広がる攻撃的な乳腺腫瘍において、我々の最良の治療をかわすことで悪名高い。本研究は、放射性トレーサーと光応答性ナノ粒子を用いてがん細胞を死滅させ、同時に免疫系を活性化するという独創的なアプローチ、放射性核種刺激動的療法(RaST)を検討している。既存の画像診断用ツールと賢い材料を再活用することで、一時的な腫瘍縮小ではなく、より長期にわたる免疫駆動のがん制御を実現できる可能性がある点で、本研究は意義深い。
腫瘍内部から光を灯す新しい方法
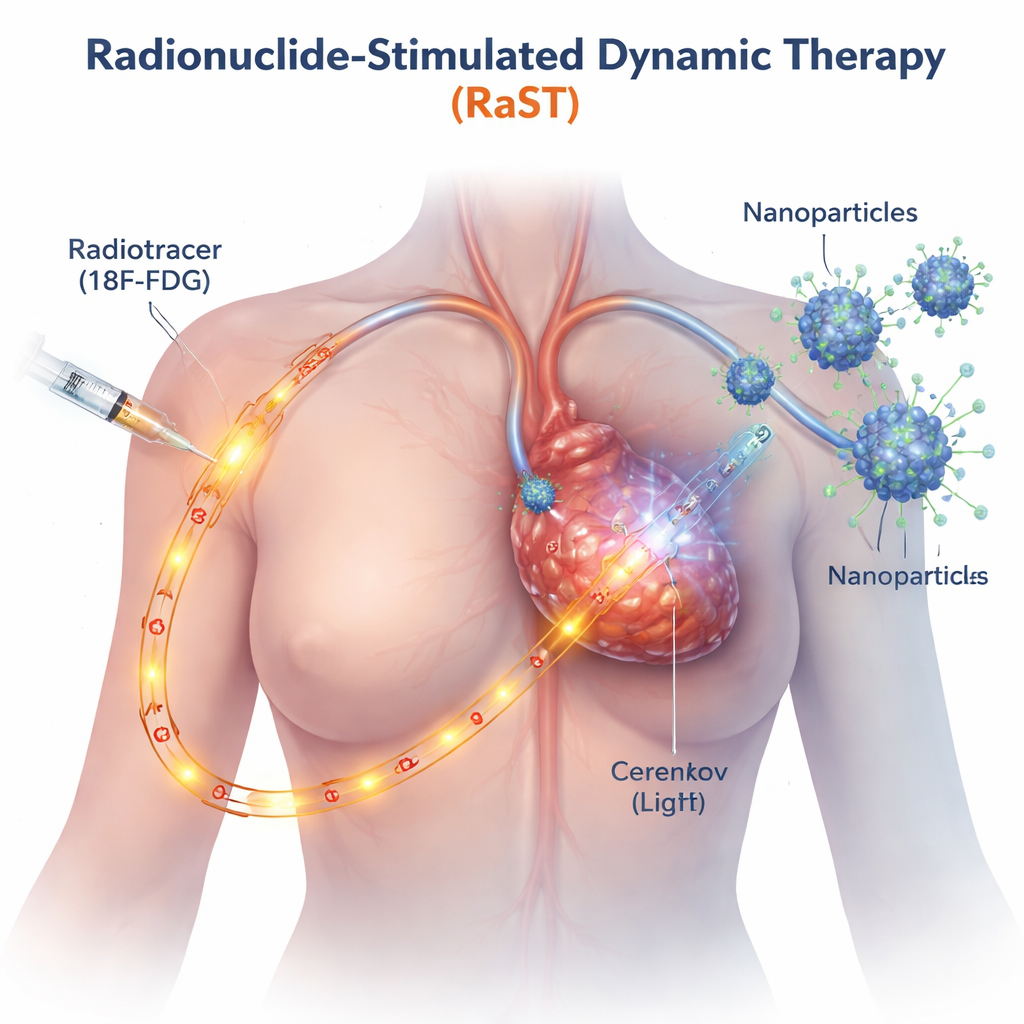
従来の光を用いるがん治療は、皮膚や表在性腫瘍など外部ビームが到達する場所でしか機能しない。RaSTは、この制約を回避するために、PET検査で既に使われているトレーサーに似た放射性の糖を利用し、増殖の速いがん細胞に自然に集積させる。このトレーサーが腫瘍内を移動するとき、チェレンコフ放射として知られる青白い微弱な光を放つ。研究者らは、チタン酸化物の微小なナノ粒子をがん標的化タンパクでコーティングして設計し、これらも腫瘍に局在するようにした。トレーサーとナノ粒子が出会うと、内部の光が粒子をスイッチオンし、そこから反応性酸素種が発生してがん細胞を内部から損傷させる。
2つの異なる細胞死経路の誘導
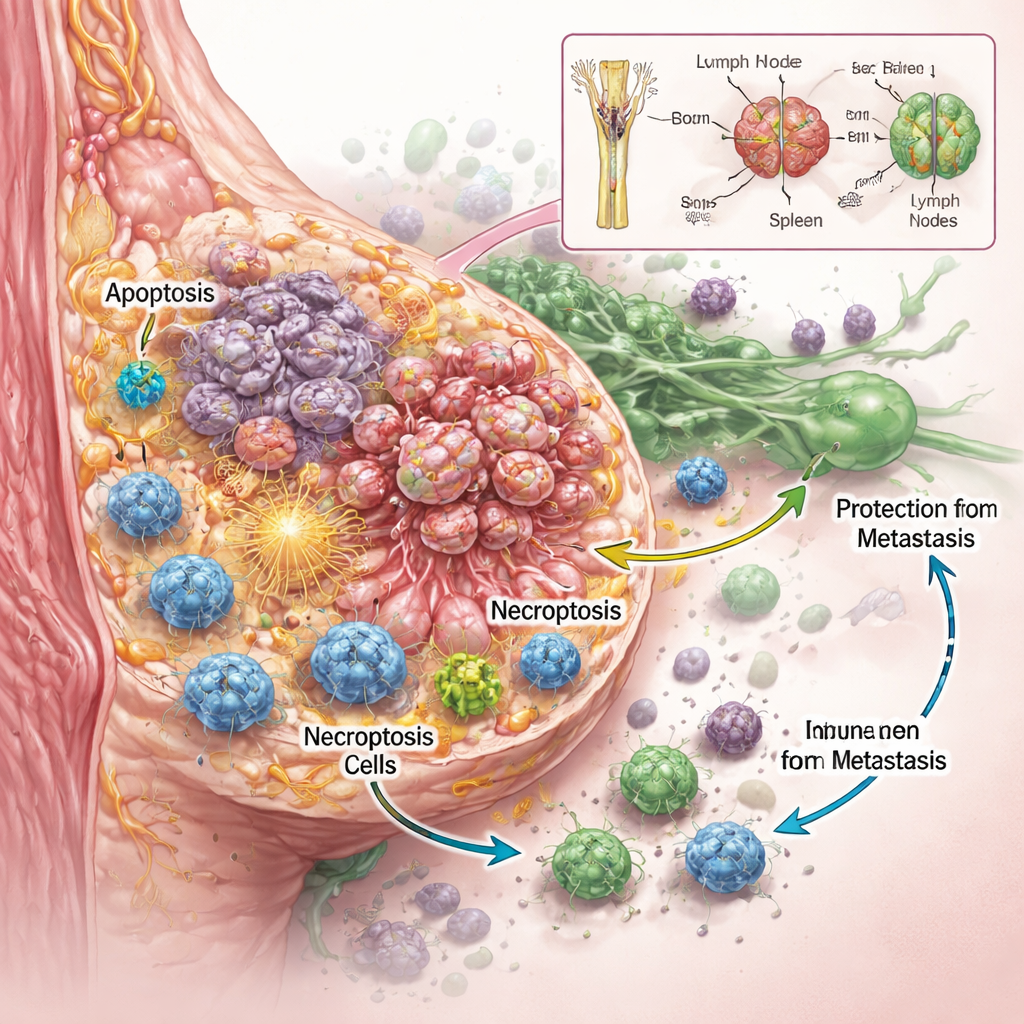
チームはRaSTが単にがん細胞を殺すかどうかだけでなく、そのメカニズムも明らかにしたかった。複数の攻撃的な乳がん細胞株を用いた実験で、放射性トレーサーとナノ粒子を慎重に調整した用量で併用すると、いずれか単独よりも効率的に腫瘍細胞を損傷することが分かった。詳細なイメージングとタンパク質解析により、RaSTが同時に2種類の制御された細胞死プログラムを活性化することが示された。一つはアポトーシスで、秩序立って細胞が自らを解体する“自殺”として説明されることが多い。もう一つはネクロプトーシスで、細胞が膨張して破裂し、分子レベルの「危険信号」を周囲に撒き散らすより爆発的な死である。これらの信号は損傷関連分子や炎症性サイトカインとして知られ、免疫細胞を引き寄せ活性化する発煙筒のように働く可能性がある。
持続的な制御のために免疫系を動員する
この炎症を伴う腫瘍破壊が生体内で重要かどうかを確かめるため、研究者らはRaSTを用いて乳がんマウスモデルで検証した。主要な免疫防御を欠くマウスでは、RaSTは局所的な細胞死を生じさせたにもかかわらず腫瘍増殖や肺への転移をほとんど抑えられなかった。しかし免疫が正常なマウスでは、同じ治療が部分的および完全な腫瘍反応を引き起こし、肺転移を防いだ。RaSTにさらされた腫瘍は免疫細胞で満たされ、とくにマクロファージや樹状細胞などの髄系細胞が死骸を貪食し、腫瘍断片をT細胞に提示するのに長けていた。血中では時間経過に沿って免疫刺激性および免疫調節性のシグナルが波状に現れ、RaSTがまずがんに対する攻撃を点火し、その後腫瘍が縮小または安定するにつれてより均衡のとれた状態に移行することを示唆した。
潜む残存病変の探索と再発防止
RaSTで完全に治癒したように見えたマウスでも、高感度のイメージング色素を用いるとリンパ節内に潜む小さな残存がん細胞のポケットが後になって明らかになった。驚くべきことに、これらの動物は何ヶ月にもわたって新たな腫瘍や遠隔転移を発症しなかった。化学分析は、当初は骨や肝臓に多く存在していたチタン酸化物ナノ粒子が徐々に脾臓やリンパ節へ再分配されることを示した—まさに免疫細胞が巡回する中枢である。こうした緩やかな移動は、免疫細胞に対して反応性酸素の局所的な供給源を維持し、隠れた残存がんを免疫が認識して再増殖や再転移の前に抑え込むのに役立っている可能性が高い。
今後のがん医療に意味すること
簡潔に言えば、本研究はRaSTが単なる腫瘍毒殺の別の手段以上であることを示している。放射性トレーサー、光応答性ナノ粒子、そして体の免疫防御を組み合わせることで、がん細胞を免疫系に大きく警告を発する二つのプログラム化された死へと導く。免疫能が保たれた動物では、これが攻撃的な乳腺腫瘍の持続的な制御と転移の遮断につながり、少数のがん細胞がリンパ節に残存していても効果を示した。臨床応用に向けてはまだ多くの課題が残るが、本研究は腫瘍を単に縮小させるのではなく、がん、細胞死、免疫の関係を再構築して長期にわたり体自身が病勢を抑える手助けをする治療の方向性を示している。
引用: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
キーワード: 乳がん, ナノ粒子, 免疫療法, 放射性医薬品療法, ネクロプトーシス