Clear Sky Science · ja
PAK4を標的にするとNLRP1/カスパーゼ-3/GSDME軸を介してジェムシタビン誘導性ピロトーシスが膵癌で促進される
がん細胞を「炎のように」殺すことが意味を持つ理由
膵臓がんは最も致死率の高いがんの一つであり、最良の化学療法薬でさえ腫瘍が耐性を獲得すると効果を失うことが多い。本研究は意外な側面を探る:同じ薬ジェムシタビンが、ある重要な分子ブレーキであるPAK4がオフになれば、より爆発的で炎症を伴う方式であるピロトーシスによってがん細胞を死に至らしめることができる。 このブレーキを理解し標的にすることで、既存の治療が多くの患者でより有効になる可能性がある。
治療をはね返す頑強ながん
膵管腺癌は診断が遅れがちで治療抵抗性が高いため、限界はありつつもジェムシタビンが基幹薬剤として残っている。ジェムシタビンは通常、秩序立った静かなプログラム死であるアポトーシスによって細胞を殺す。しかし、本研究で調べた膵腫瘍の半数以上がGSDMEというタンパク質を高発現しており、これが静かな死をピロトーシスに切り替え得ることが分かった。ピロトーシスは迅速で「破裂する」ような細胞死で、細胞膜を損ない炎症性シグナルを放出する。では、腫瘍がピロトーシスを起こし得るにもかかわらず、なぜ多くがジェムシタビンに抵抗するのかという重要な問いが浮かんだ。
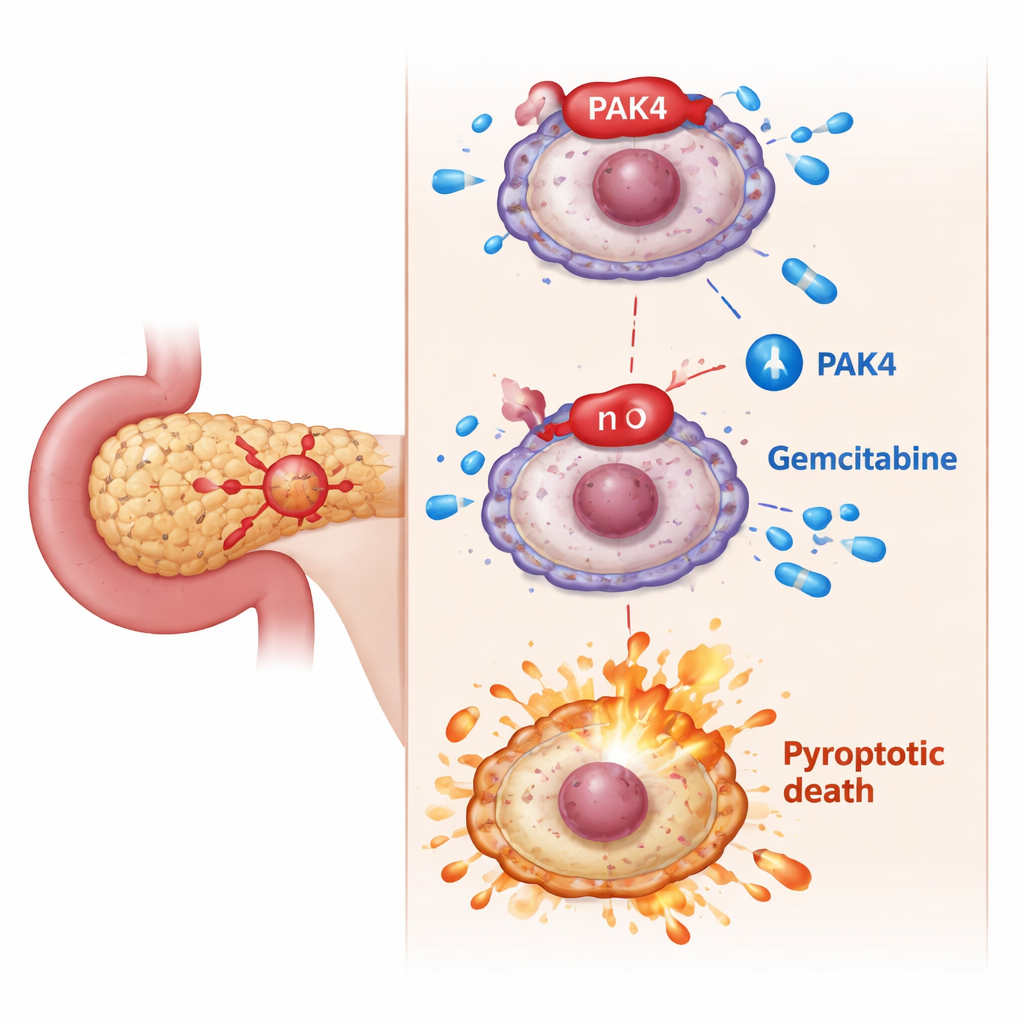
隠れたブレーキ:PAK4は炎のような細胞死を阻む
研究者らはPAK4に注目した。PAK4は成長促進性タンパク質で、膵臓がんで過剰に活性化しジェムシタビン不応に関連することが知られている。細胞実験では、PAK4が高い細胞ほどジェムシタビンで殺しにくかった。PAK4を減らすと、ジェムシタビンは突然はるかに致死的になり、細胞は腫脹、風船状の膨らみ、膜破裂、細胞内成分の大量放出など典型的なピロトーシスの特徴を示した。分子的には、この変化はGSDMEがカスパーゼ-3によって切断され活性断片になることに依存していた。カスパーゼ-3を阻害するとGSDMEがピロトーシスを引き起こすのを止め、PAK4が通常この死の経路を抑えていることが確認された。
PAK4はどうやって細胞の死のアラームを解体するか
さらに解析すると、PAK4はGSDMEを直接攻撃するのではなく、上流の「アラームセンサー」であるNLRP1を妨害していることがわかった。患者では高いNLRP1レベルが生存率の改善と関連し、NLRP1が腫瘍制御に寄与していることが示唆された。がん細胞でNLRP1を失わせると、ジェムシタビン誘導の細胞死とGSDME活性化が著しく低下し、NLRP1がピロトーシス機構に寄与していることが明らかになった。腫瘍サンプルではPAK4とNLRP1の発現は逆相関していた:PAK4が高いところでNLRP1は低かった。研究は、活性化したPAK4が別のタンパク質であるE3リガーゼMdm2を介してNLRP1に標的化シグナルを付け、細胞の廃棄システムでNLRP1を破壊させることを示した。こうしてNLRP1を標識することで、PAK4は通常カスパーゼ-9およびカスパーゼ-3を介する連鎖反応の活性化を防ぎ、最終的にGSDME駆動のピロトーシスへ至るのを妨げている。
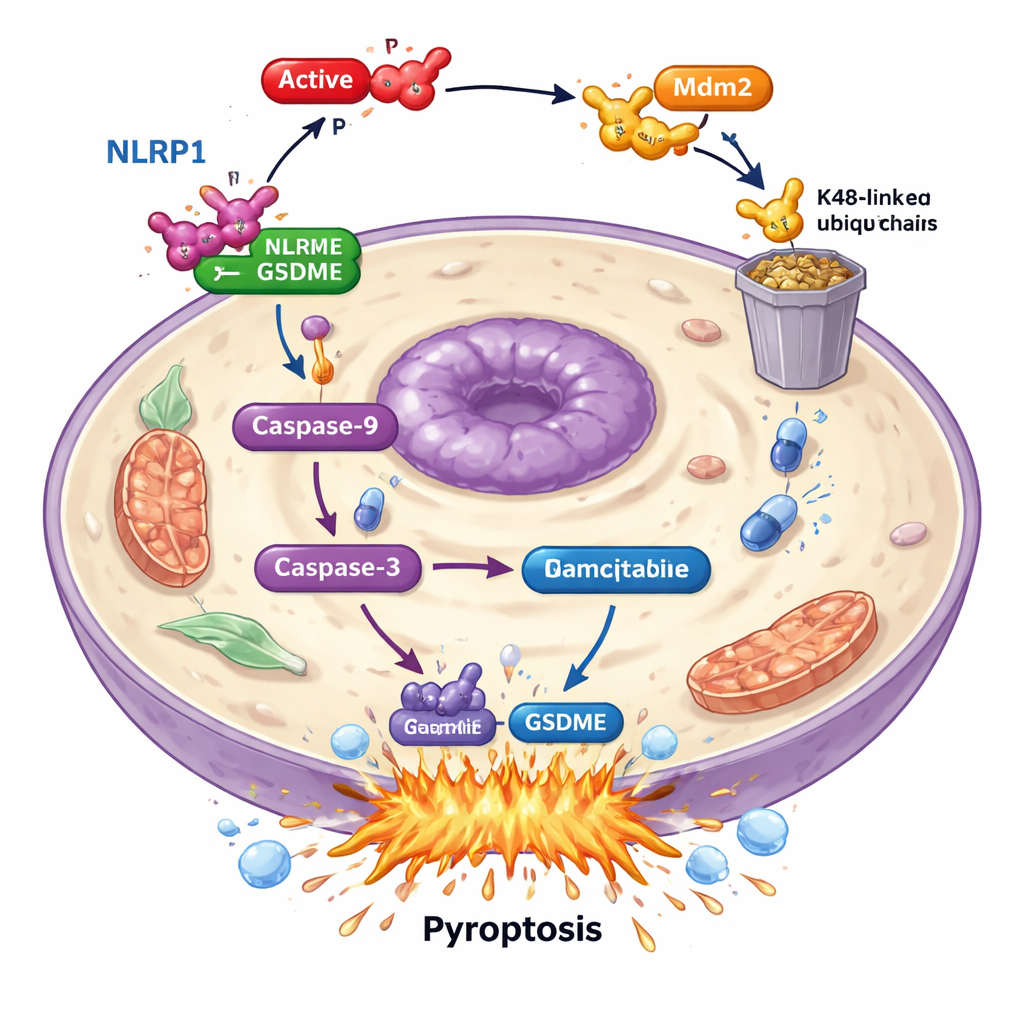
PAK4をオフにして化学療法を強化する
PAK4がピロトーシスのブレーキとして働くため、研究チームはその活性を阻害すればジェムシタビンの殺傷力を再覚醒できるかを検証した。彼らはPF-3758309という小分子PAK4阻害剤を用いた。単独でもこの阻害剤は膵がん細胞をピロトーシスへ傾け、カスパーゼ-3活性化、GSDME切断、細胞膜破裂を増加させた。ジェムシタビンと併用すると効果はさらに強まり、より多くの細胞がピロトーシスで死に、死の経路の分子マーカーも増加した。ヒト膵腫瘍を移植したマウスモデルでは、PAK4を低下させるかPAK4阻害剤で治療するとジェムシタビンによる腫瘍縮小がより効果的になり、腫瘍内のピロトーシスマーカーも増加した。
患者と将来の治療への意味
平たく言えば、本研究は化学療法下で膵がん細胞がより破壊的な方法で死ぬのを妨げる分子ロック、PAK4を明らかにした。PAK4を無効化することで、医師はジェムシタビン治療を受ける腫瘍をピロトーシスへ押し込み、薬剤の効果を高め、場合によっては免疫系を腫瘍に対して刺激できる可能性がある。患者由来モデルや臨床試験でのさらなる検証が必要だが、本研究は既存の薬剤をより賢く組み合わせて耐性腫瘍を応答性のある腫瘍へ変換するための明確なロードマップを提示している。
引用: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
キーワード: 膵臓がん, ジェムシタビン耐性, ピロトーシス, PAK4, 標的療法