Clear Sky Science · ja
遺伝子スプライシングを標的とした遮断がイントロン内に埋め込まれた一次マイクロRNAを破綻させる可能性
遺伝子の中に隠されたメッセージ
多くの新しい遺伝子治療は細胞内のRNAメッセージを操作することで働きますが、これらのRNAには研究者がまだ理解し始めたばかりの「余白の注記」が隠されていることが多いです。本論文は、遺伝子の誤ったスプライシングを修正するよう設計された薬剤が、イントロン—遺伝子のコーディング領域の間にある非コード領域—に埋め込まれた小さな制御RNAを意図せず増強してしまい、脳の配線や発生に予想外の影響を及ぼすことを示しています。
RNAを書き換える遺伝子治療
アンチセンスオリゴヌクレオチド(ASO)は、RNAに結合してその読み取りや処理を変える短い合成核酸断片です。複数のASOはすでに、特にRNAのスプライシングの異常が原因となる希少遺伝性疾患に対して試験中または臨床で使用されています。多くの安全性試験はASOが正しいタンパク質を回復するか、明らかな副作用を回避するかに焦点を当てます。しかし、多くの遺伝子はマイクロRNAを含む非コードRNAをイントロン内に抱えており、これらの小分子は遺伝子活性を大きく調節できます。脊椎動物で知られているマイクロRNAのうち最大で半数がイントロン由来です。本研究は問いかけます:ASOでスプライシングを強制的に変えたとき、これらの埋め込まれたマイクロRNAはどうなるのか?
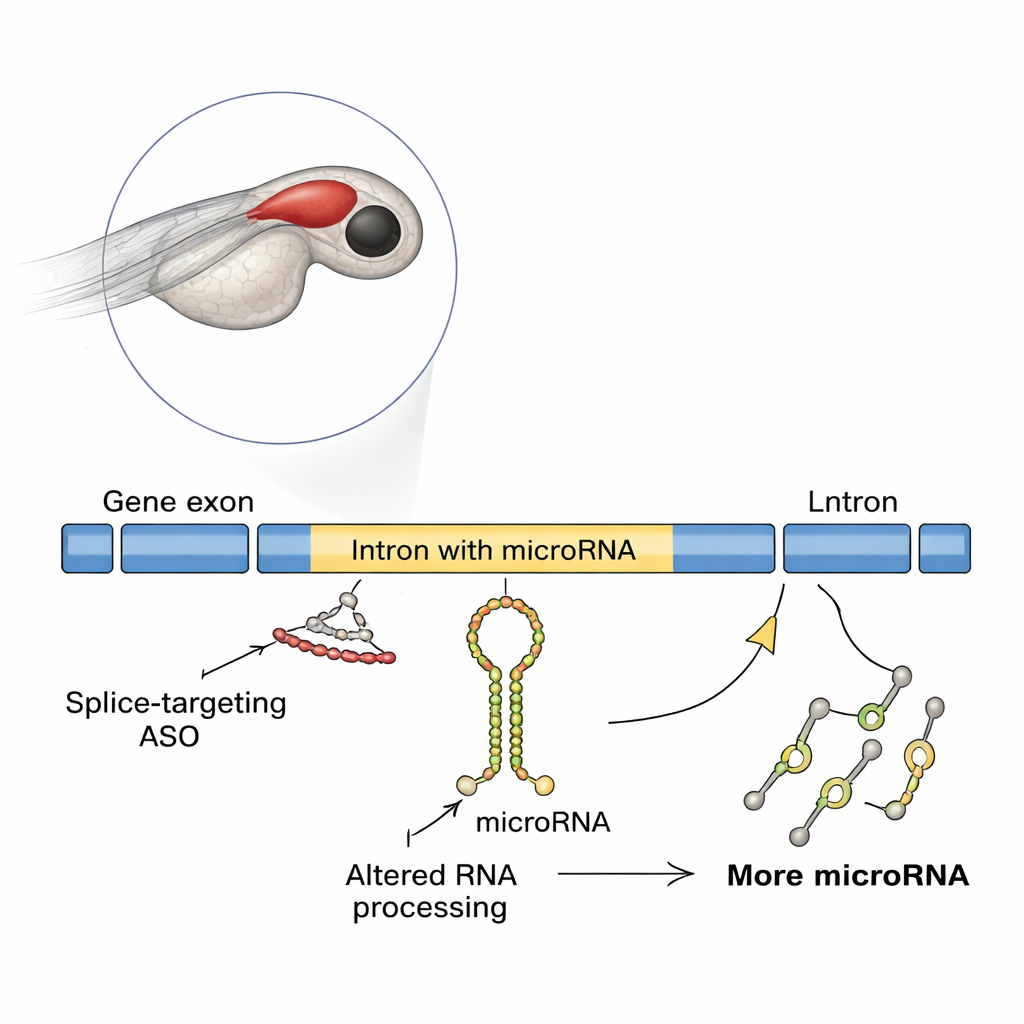
発生中の魚の脳で見つかった意外な効果
研究者らは透明な胚により脳の発生追跡が容易な人気の脊椎動物モデルであるゼブラフィッシュを用いました。彼らは神経繊維の誘導を助ける遺伝子< i>slit3(※注:HTMLタグは保持)に着目し、この遺伝子のイントロンの一つに< i>mir-218a-1というマイクロRNAが埋め込まれていることを利用しました。< i>slit3の翻訳開始を阻害すると、ホルモン分泌を担う下垂体軸索の発達は正常に見えました。しかし、別のASOで< i>slit3の特定のスプライス部位をブロックすると、後方下垂体へ投射するはずの軸索が著しく減少しましたが、オキシトシン産生ニューロンの数は変わりませんでした。分子解析では、このスプライス阻害ASOが遺伝子のRNAでイントロン保持を引き起こし、予期せず< i>slit3転写産物、その長いイントロン、およびイントロン内に埋め込まれた一次< i>mir-218a-1転写物のレベルを上昇させていることが示されました。
欠失したタンパク質ではなくマイクロRNAが欠陥を引き起こす
軸索異常の原因を解明するため、著者らは複数の状況を比較しました。成熟した< i>mir-218a-1だけを阻害しても< i>slit3のレベルは変わらず、マイクロRNA付近の別のスプライス部位を標的にしたASOは軸索欠陥を生じさせず< i>mir-218a-1を増加させませんでした。重要なことに、スプライス阻害型の< i>slit3 ASOを< i>mir-218a-1を無効化するASOと組み合わせると、軸索配線は大部分回復しました。同様に、遺伝的に< i>mir-218a-1を欠くゼブラフィッシュでは、同じスプライス阻害型< i>slit3 ASOはもはや軸索欠陥を引き起こさず、正常な魚に合成の< i>mir-218aミミックを注入すると同じ表現型が再現されました。これらの実験は、発生異常の主因が切断されたSlit3タンパク質ではなく、上昇したイントロン由来マイクロRNAであることを示しています。
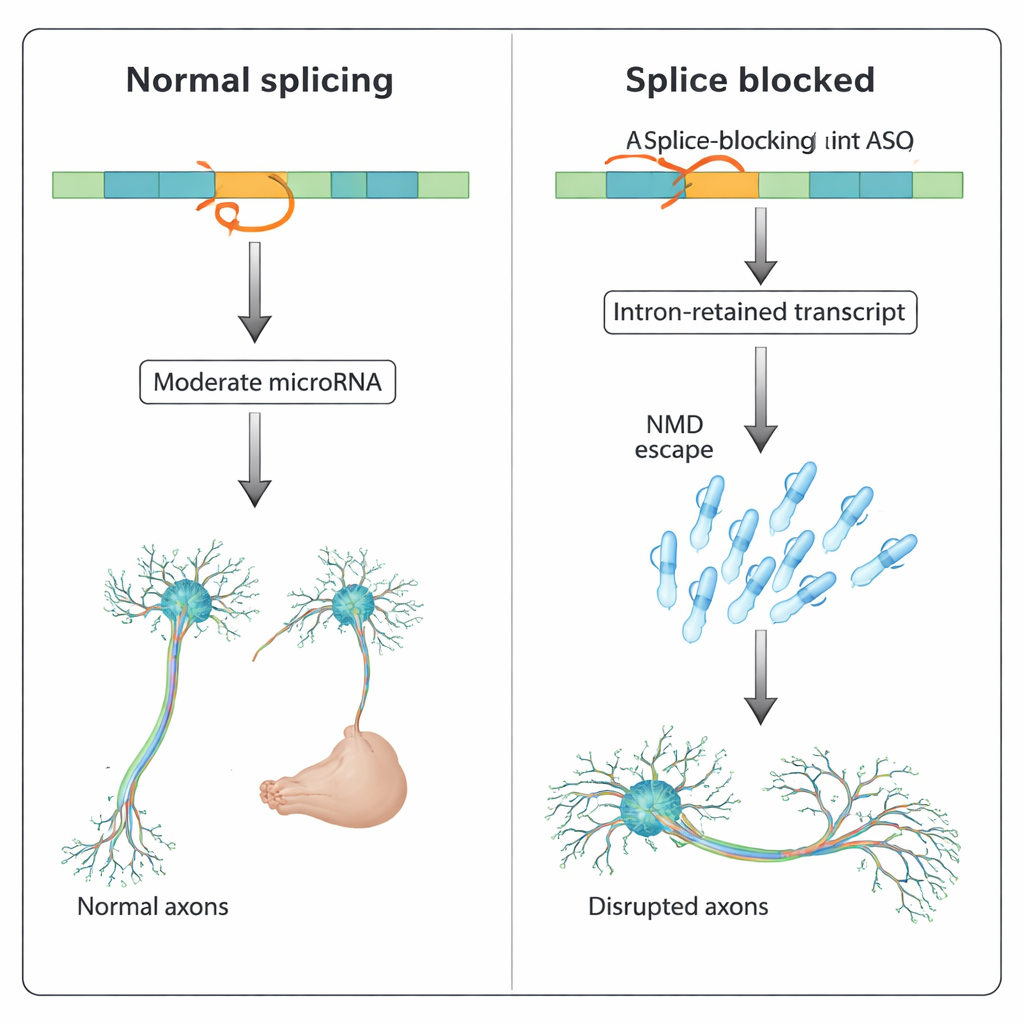
複数の遺伝子で見られるより広いパターン
次に研究チームは、この効果が< i>slit3に特有のものかどうかを調べました。彼らはゼブラフィッシュのゲノムを検索し、イントロン内にマイクロRNAを宿すタンパク質コード遺伝子が多数存在することを見つけ、多くは発生やシグナル伝達に関与していました。そのうちの二つ、< i>pank2と< i>dnm2aは、ASOでスプライシングを阻害した場合に脳室水腫、心拡張、体の変形など重篤な発生異常を示し、同じ遺伝子の遺伝学的ノックアウトでは再現されなかったことが以前に報告されています。本研究では、イントロン内マイクロRNAである< i>mir-103(< i>pank2内)や< i>mir-199-5p(< i>dnm2a内)を特異的に阻害するASOを共注入すると、これらのASO誘導表現型が部分的に救済されました。場合によってはマイクロRNAの阻害が宿主遺伝子の発現を回復させることもあり、他の場合では回復しなかったため、全体レベルの変化がわずかでもイントロン由来マイクロRNA活性の上昇自体が有害になり得ることが示唆されます。
将来の治療への示唆
これらの発見は、スプライスを標的とするASOがエクソンのスキップやイントロン保持を引き起こす以上のことをし得ることを明らかにします:これらは細胞の品質管理系を回避するイントロン保持転写物を安定化させ、イントロン内一次マイクロRNAの量を増やし、それが標的遺伝子群のネットワークを誤調節する可能性があります。発生中のニューロンでは、そのような暴走するマイクロRNA活性が軸索の成長と接続を歪め得ます。医薬品開発者にとって、動物実験で観察される異常または「オフターゲット」的な表現型は必ずしもp53活性化のような一般的な毒性経路に由来するとは限らず、隠れたイントロンRNAへの意図しない影響から来ることがある、ということを意味します。翻訳阻害型ASOとスプライス阻害型ASOを注意深く比較し、イントロン内マイクロRNAの発現をモニターすることで、これらのリスクを早期に検出し、患者に届く前にASO設計を改良する助けになるでしょう。
引用: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
キーワード: アンチセンスオリゴヌクレオチド, マイクロRNA, RNAスプライシング, ゼブラフィッシュの発生, 遺伝子治療の安全性