Clear Sky Science · ja
haCCA: スポット型空間トランスクリプトームとメタボロームのマルチモジュール統合
分子を“どこで”見るかが重要な理由
私たちの体は、それぞれ固有の活性化遺伝子や化学物質の組み合わせを持つ無数の小さな細胞の近隣から成り立っています。これまで、研究者は組織を粉砕して均一なペーストにし、その後で分子を解析する必要があり、「どこにあったか」という情報は失われていました。本論文は、haCCAと呼ばれる新しい計算手法を紹介します。これは二つの強力なイメージング手法をつなぎ合わせることで、組織や腫瘍内で遺伝子と低分子がどのように配置されているかを現場(in situ)で明らかにします。そうした地図は、隠れた病態パターンを浮かび上がらせ、より精密な治療の示唆を与える可能性があります。
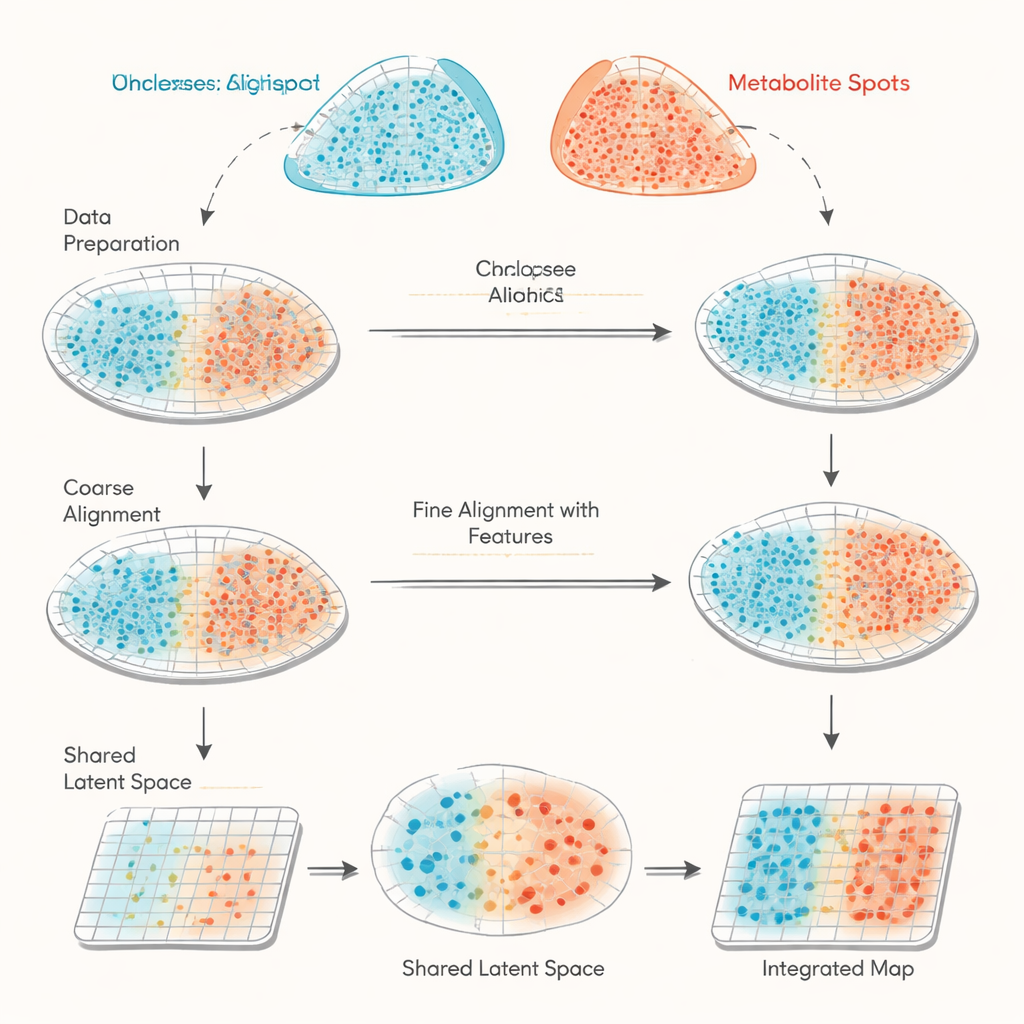
同一組織の二つの異なる見え方
本研究は、生物学でますます用いられる二つの空間的手法のデータを結合することに焦点を当てています。空間トランスクリプトミクスは、組織切片上の何千もの小さなスポットでどの遺伝子が発現しているかを記録します。MALDI質量イメージングは、代謝物や脂質など多くの低分子の量を同様に高密度のスポット格子で測定します。問題は、これら二つの装置が完全に同じ位置や同じ特徴セットを測定しているわけではない点で、そのデータは異なる凡例を持つ二つのずれた地図のようなものです。既存のアプローチは主に座標に基づいて組織断面の形状を一致させようとしますが、これは不正確になりやすく、アラインメントの良さを検証する手段に乏しいことがあります。
分子マップをより賢く整列させる方法
haCCA(階層的アンカー誘導正準相関解析の略)は、幾何学と生物学を組み合わせてこの課題に取り組みます。まず、二つの技術によるスポット格子を二段階の「形態学的アラインメント」で整えます。ヒトの専門家が組織画像上でいくつかの対応するランドマークを選び、大まかな平行移動や回転を補正し、その後自動化されたステップが裂け目や欠損の近くにある外れ値を微調整します。次に、空間的に近く、局所的に均一な領域にあるため同一領域を表す可能性が高い「アンカー」スポットのペアを探します。これらのアンカーから、haCCAはどの遺伝子と代謝物がともに変動するかを計算し、それらの最も強い共通パターンを捉える共有の低次元表現に集約します。
相関を統一された組織像に変換する
空間座標と共有の分子表現の両方を得た後、haCCAは各遺伝子スポットが各代謝物スポットとどれほど対応するかを決める最適化問題を解きます。このステップは、スポット同士が空間的に近いことを保ちながら、遺伝子–代謝物の結合プロファイルにおいても類似するよう設計されています。最終的に得られるのは、あるデータセットの各点を他方の最良の対応点に結ぶ「輸送計画」で、統合されたマルチモーダル地図を生み出します。真の対応関係が既知の慎重に作られたテストデータでは、著者らはワークフローの各ステージ(大まかな整列、精緻化された整列、特徴に基づくマッチング)が独立した三つの精度指標を着実に改善することを示しています。幾何学に主に依拠する他のツールと比べて、haCCAは一貫して高い整列精度と領域ラベルのより忠実な転写を達成します。
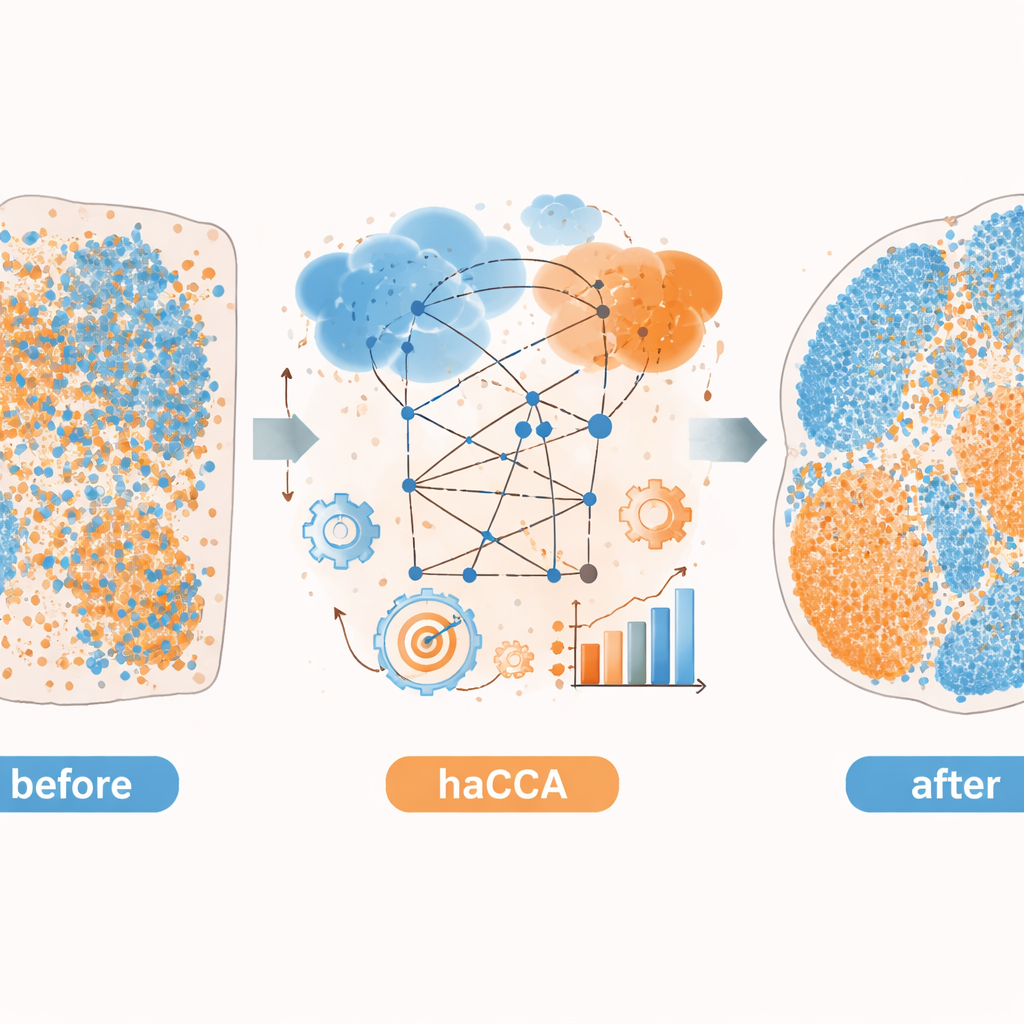
脳および肝がんで明かされた隠れた生物学
著者らは次に、haCCAを実際のマウス脳および肝腫瘍組織に適用します。脳の解析では、市販の空間トランスクリプトミクスデータを同一または近接切片から得られた代謝物イメージと統合しました。本手法は既知の代謝領域を保持し、例えばドーパミンとその主要酵素をコードする遺伝子の共局在など期待される重なりを再構成します。遺伝子と代謝物を共同でクラスタリングすることで、組み合わせたデータはどちらのモダリティ単独よりも微妙な組織亜領域を分離することがわかりました。肝内胆管癌の前臨床モデルでは、著者らはhaCCAを用いて好中球外罠(免疫細胞が放出する網状構造)を形成できる腫瘍とできない腫瘍を比較しました。統合地図は、これらの罠が存在する場合、Scd1という遺伝子とそれに関連する脂肪酸が悪性領域で濃縮していることを示し、腫瘍内で脂質代謝が変化している方向へのシフトを示唆しました。
今後の研究にとっての意義
日常的な比喩で言えば、haCCAは異なるカメラで撮られた航空写真を重ねるようなものです—一方は建物の輪郭に敏感で、もう一方は熱の特徴に敏感、こうして各街区で何が起きているかをより鮮明に捉えます。遺伝子がどこで活性化しているかと主要な代謝物がどこに蓄積しているかを正確に結合することで、このワークフローは細胞の振る舞いの両面、すなわち指示(遺伝子)と結果としての化学(代謝)を同時にプロファイリングする助けになります。本アプローチは従来のアラインメント手法より改良され、アクセスしやすいPythonツールとしてパッケージ化されており、ほかの空間技術にも拡張可能です。こうした統合地図がより日常的に使われるようになれば、腫瘍や他の組織がどのように代謝を組織化し、治療に応答し、時間とともに進化するかの理解を深める助けになるでしょう。
引用: Xu, J., Shen, XT., Zhang, C. et al. haCCA: multi-module Integration of spot-based spatial transcriptomes and metabolomes. Commun Biol 9, 248 (2026). https://doi.org/10.1038/s42003-026-09526-w
キーワード: 空間マルチオミクス, トランスクリプトミクス, メタボロミクス, 腫瘍代謝, データ統合