Clear Sky Science · ja
ニンボライドはNLRP3インフラマソーム活性化を阻害してARDSと潰瘍性大腸炎を改善する
暴走する炎症を抑える意義
命に関わる肺不全から痛みを伴う腸疾患まで、多くの重篤な病気は単に病原体や外傷によるものだけでなく、体自身の免疫系が過剰に反応することで引き起こされます。本研究は、ニームの木に由来する天然化合物ニンボライドが、免疫細胞内の強力な炎症装置の一つに対して「正確なブレーキ」として働けるかを検討し、急性呼吸窮迫症候群(ARDS)や潰瘍性大腸炎のような病態に対するより安全な治療法への道を探っています。
免疫細胞内のトラブルメーカーとなる警報装置
本題の中心にあるのはNLRP3インフラマソームと呼ばれる分子レベルの警報システムです。免疫細胞が感染、組織損傷、または結晶などの危険信号を感知すると、NLRP3(センサー)、ASC(アダプター)、カスパーゼ‑1(酵素)の三つの構成要素がレゴのように組み合わさって複合体を形成します。一旦組み立てられると、この複合体はIL‑1βやIL‑18といった強力なシグナル分子を活性化し、炎症性の細胞死であるパイロプトーシスを引き起こします。この反応は脅威を排除する助けになりますが、過剰に活性化されると関節炎、糖尿病合併症、アルツハイマー病、ARDS、炎症性腸疾患などの慢性・急性疾患に寄与します。製薬企業は合成化合物でNLRP3を抑えようとしてきましたが、多くの候補は毒性、副作用、体内での振る舞いの問題でつまずき、安全で選択的な阻害剤への明確なニーズが残っています。
強力な植物由来阻害剤の発見
研究者らは126種類の天然化合物をスクリーニングし、マウス免疫細胞からのIL‑1β放出を最もよく抑えるものを調べました。ニンボライドは顕著で、試験濃度でIL‑1β分泌を80%以上低下させました。さらなる実験では、マウスの骨髄由来マクロファージにおいてニンボライドがカスパーゼ‑1の活性化、IL‑1βの放出、およびパイロプトーシスを強く抑制し、その有効性は基準薬MCC950と同等のことが示されました。重要なのは、ニンボライドがIL‑6など他の免疫メディエーターの放出を阻害しなかったことで、これは免疫を単純にシャットダウンするのではなく、より焦点を絞った働き方をしていることを示唆します。ATP、ナイジェリシン、アルム結晶、イミキモドなどNLRP3を活性化するさまざまな刺激に対して、ニンボライドは一貫してインフラマソーム活性を低下させ、人のTHP‑1細胞でも同様の効果が見られました。対照的に、AIM2やNLRC4という関連インフラマソームは阻害せず、NLRP3に特異的であることが浮き彫りになりました。
ニンボライドが炎症装置をどう阻むか
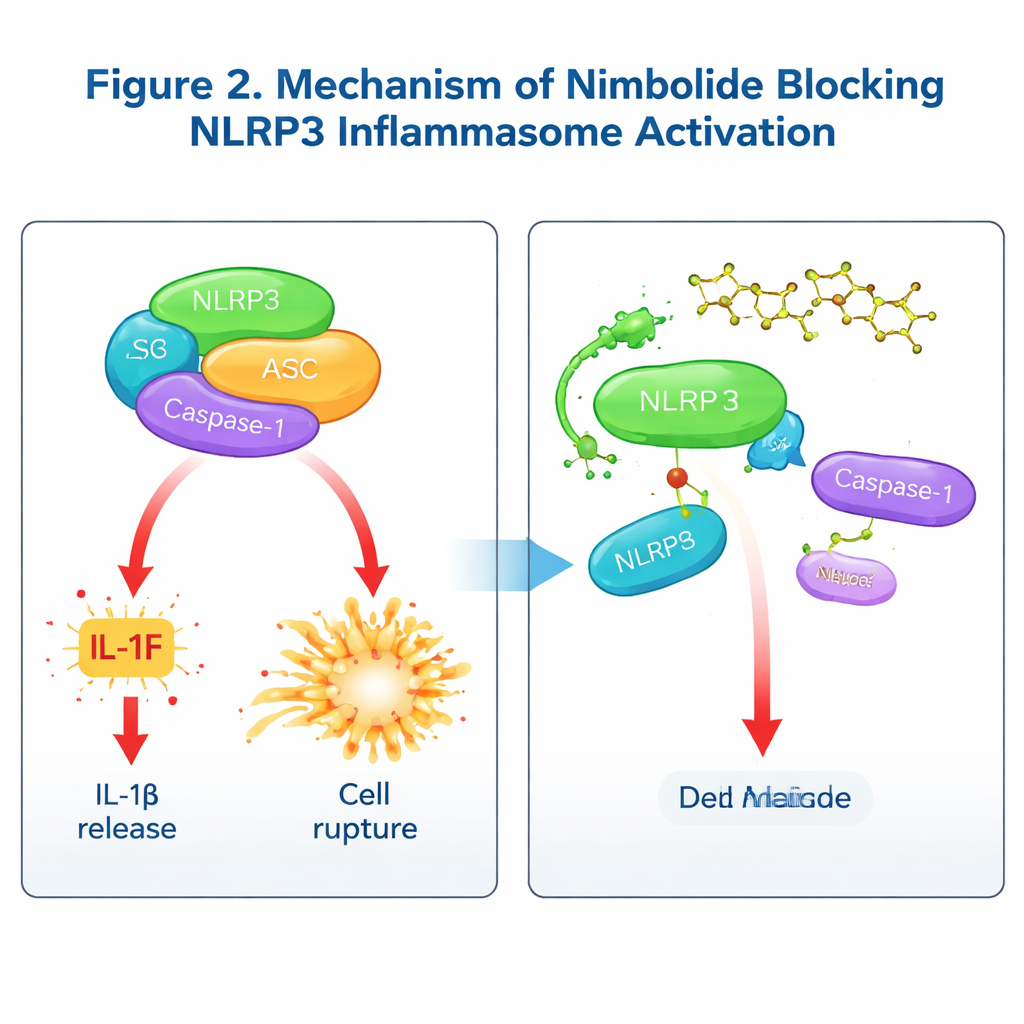
ニンボライドの作用機序を明らかにするため、研究チームはそれがNF‑κB経路で制御される初期の「プライミング」過程に干渉するのか、あるいはインフラマソームが物理的に組み立てられる後期段階に働くのかを調べました。プライミング後に短時間処理しても主要なプライミングシグナルや遺伝子発現には影響がなく、それでもIL‑1βとカスパーゼ‑1の活性化は抑えられたため、ニンボライドは主に組み立て段階に作用することが示されました。詳細な生化学的試験から、ニンボライドはカリウムやカルシウムの流出、ミトコンドリア損傷、あるいはNLRP3と補助タンパク質NEK7との相互作用を変えない一方で、NLRP3とASC間の重要な結合を妨げ、ASCのスピック形成を減少させ、NLRP3の高次オリゴマー化を阻止することが分かりました。結合アッセイと分子モデリングにより、ニンボライドはNLRP3のNACHT領域の特定のアミノ酸、リジン565(Lys565)に直接結合することが示されました。この部位を変異させると、ニンボライドはもはやNLRP3の分解から保護したりASCとの結合を断ち切ったりできなくなり、Lys565が主要なドッキングポイントであることが確認されました。注目すべきは、他の薬剤がしばしばNLRP3のATPase活性を標的にするのに対し、ニンボライドはATPの利用に影響を与えずに組み立てを阻害するという独特の作用様式を持つ点です。
肺と腸の疾患モデルでのニンボライドの検証
次に、こうした分子レベルの効果が疾患モデルで実際の保護に結びつくかを検証しました。細菌毒素を投与してARDSを誘導したマウスでは、侵襲前にニンボライドを処置すると肺組織の損傷、液体貯留、および気腔へのタンパク漏出が軽減されました。肺への侵入免疫細胞は減少し、肺組織と血中のIL‑1βレベルも低下しました。毒素を気道に直接投与するモデルでも同様の利益が観察されました。潰瘍性大腸炎の別モデルでは、結腸を損傷する化学物質を飲ませたマウスで、ニンボライドは体重減少を抑え、便の状態と出血スコアを改善し、結腸の長さを維持し、組織学的な炎症や侵食の所見を軽減し、結腸内のIL‑1βも低下させました。重要なことに、遺伝子改変でNLRP3を欠くマウスでは疾患が既に軽度であり、ニンボライドは付加的な利益を示さなかったため、その保護効果はNLRP3阻害に依存することが強く示されました。
将来の治療への示唆
専門外の読者にとっての要点は、ニンボライドが体内の最も強力な炎症スイッチの一つに対する賢いブレーキのように働くことです。NLRP3の特定の部位に結合してインフラマソームの組み立てを防ぐことで、肺や腸における過剰な炎症を落ち着かせつつ、免疫防御全体を幅広く抑え込むことは避けられます。ニンボライド自体は安定性や投与法など改良すべき点が残るため即座に薬になるわけではありませんが、本研究はニンボライドをNLRP3駆動性疾患(ARDSや潰瘍性大腸炎など)に対する次世代薬開発の有望な出発点かつ設計図として位置付けます。
引用: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
キーワード: ニンボライド, NLRP3インフラマソーム, 炎症, 急性呼吸窮迫症候群, 潰瘍性大腸炎